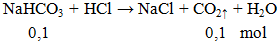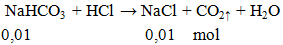Chúng tôi xin giới thiệu phương trình NaHCO3 + HCl → NaCl + CO2↑ + H2O gồm điều kiện phản ứng, cách thực hiện, hiện tượng phản ứng và một số bài tập liên quan giúp các em củng cố toàn bộ kiến thức và rèn luyện kĩ năng làm bài tập về phương trình phản ứng hóa học của Natri. Mời các bạn đón xem:
Phương trình NaHCO3 + HCl → NaCl + CO2↑ + H2O
1. Phương trình phản ứng hóa học:
NaHCO3 + HCl → NaCl + CO2↑ + H2O
2. Hiện tượng nhận biết phản ứng
- Có khí không màu thoát ra.
3. Điều kiện phản ứng
- điều kiện thường.
4. Bản chất của các chất tham gia phản ứng
a. Bản chất của NaHCO3 (Natri hidrocacbonat)
- NaHCO3 là một muối axit nhưng thể hiện tính axit yếu.
- NaHCO3 có thể tác dụng với axit mạnh hơn như H2SO4, HCl tạo thành muối, nước và giải phóng khí CO2.
b. Bản chất của HCl (Axit clohidric)
HCl là một axit mạnh tác dụng được với muối có gốc anion hoạt động yếu hơn.
5. Tính chất hóa học
5.1. Tính chất hóa học của NaHCO3 (Natri hidrocacbonat)
– Natri hiđrocacbonat là muối axit do có nguyên tử H linh động trong thành phần gốc axit, thể hiện tính axit yếu. Tuy nhiên vì NaHCO3 là muối của axit yếu (H2CO3) nên có thể tác dụng với axit mạnh hơn (ví dụ HCl…), giải phóng khí CO2, do đó NaHCO3 cũng thể hiện tính bazơ và tính chất này chiếm ưu thế hơn tính axit
Trong dung dịch nước thì NaHCO3 bị thủy phân tạo môi trường bazơ yếu
NaHCO3 + H2O → NaOH + H2CO3
– Môi trường này có thể làm đổi màu quỳ tím nhưng không đủ mạnh để làm đổi màu dung dịch phenolphtalein.
Tác dụng với axit mạnh tạo thành muối và nước, đồng thời giải phóng khí CO2
2NaHCO3 + H2SO4 → Na2SO4 + 2H2O + 2CO2
Tác dụng với bazơ tạo thành muối mới và bazơ mới
NaHCO3 + Ca(OH)2 → CaCO3 + NaOH + H2O
hoặc tạo thành hai muối mới:
2NaHCO3 + Ca(OH)2 → CaCO3 + Na2CO3 + 2H2O
5.2. Tính chất hóa học của HCl (Axit clohidric)
- Axit HCl làm đổi màu quỳ tím: Khi nhúng quỳ tím vào dung dịch axit sẽ có hiện tượng quỳ tím chuyển đỏ.
- Axit clohidric tác dụng với kim loại đứng trước H, tạo thành muối và hidro
Fe + 2HCl → FeCl2 + H2↑
- Axit clohidric tác dụng với oxit kim loại, tạo thành muối Clorua và nước
6HCl + Al2O3 →2AlCl3 + 3H2O
- Axit clohidric tác dụng với Bazơ, tạo thành muối Clorua và nước
3HCl + Al(OH)3 → AlCl3 + 3H2O
- Axit clohidric tác dụng với muối, tạo thành muối mới và axit mới
AgNO3 + 2HCl → AgCl↓ + HNO3
- Axit clohidric tác dụng với hợp chất có tính oxi hoá, thể hiện tính khử
6HCl + KClO3 → KCl + 3Cl2↑ + 3H2O
Lưu ý: Axit HCl sẽ không tác dụng với những kim loại đứng sau H trong dãy điện hoá, không tác dụng với các phi kim, axit, oxit kim loại, oxit phi kim.
6. Cách thực hiện phản ứng
- Nhỏ HCl vào ống nghiệm chứa NaHCO3.
7. Bạn có biết
- NaHCO3 phản ứng với các axit như H2SO4, HBr… đều giải phóng khí.
8. Bài tập liên quan
Ví dụ 1: Nhỏ HCl vào ống nghiệm chứa NaHCO3 thu được hiện tượng là
A. Có khí không màu thoát ra.
B. Có khí màu nâu đỏ thoát ra.
C. Có khí màu vàng lục thoát ra.
D. Không có hiện tượng gì.
Hướng dẫn giải
NaHCO3 + HCl → NaCl + CO2↑ + H2O
CO2: khí không màu.
Đáp án A.
Ví dụ 2: Thể tích khí ở dktc thoát ra khi cho 8,4g NaHCO3 phản ứng hoàn toàn với lượng dư HCl là
A. 1,12 lít.
B. 2,24 lít.
C. 3,36 lít.
D. 4,48 lít.
Hướng dẫn giải
V = 0,1.22,4 = 2,24 lít.
Đáp án B.
Ví dụ 3: Cho 0,84g NaHCO3 phản ứng hoàn toàn với lượng HCl, khối lượng muối có trong dung dịch thu được sau phản ứng là
A. 0,585 gam.
B. 0,745 gam.
C. 0,475 gam.
D. 1,00 gam.
Hướng dẫn giải
khối lượng muối = 0,01.58,5 = 0,585 gam.
Đáp án A.
9. Một số phương trình phản ứng hóa học khác của Natri và hợp chất:
NaHCO3 + HBr → NaBr + CO2↑ + H2O
NaHCO3 + HNO3 → NaNO3 + CO2↑ + H2O
2NaHCO3 + H2SO4 → Na2SO4 + 2CO2↑ + 2H2O
NaHCO3 + NaHSO4 → Na2SO4 + CO2↑ + H2O
2NaHCO3 + 2KHSO4 → K2SO4 + Na2SO4 + 2CO2↑ + 2H2O