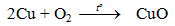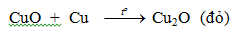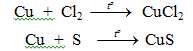Chúng tôi xin giới thiệu phương trình Cu + S → CuS gồm điều kiện phản ứng, cách thực hiện, hiện tượng phản ứng và một số bài tập liên quan giúp các em củng cố toàn bộ kiến thức và rèn luyện kĩ năng làm bài tập về phương trình phản ứng hóa học của Đồng. Mời các bạn đón xem:
Phương trình Cu + S → CuS
1. Phương trình phản ứng hóa học:
Cu + S → CuS
2. Hiện tượng nhận biết phản ứng
- Cu khi đốt chuyển thành màu đen
3. Điều kiện phản ứng
- Nhiệt độ.
4. Tính chất hoá học
- Là kim loại kém hoạt động, có tính khử yếu.
Tác dụng với phi kim:
- Cu phản ứng với oxi khi đun nóng tạo CuO bảo vệ nên Cu không bị oxi hoá tiếp tục.
- Khi tiếp tục đun nóng tới (800-1000oC)
- Tác dụng với Cl2, Br2, S...
Tác dụng với axit:
- Cu không tác dụng với dung dịch HCl, H2SO4 loãng.
- Khi có mặt oxi, Cu tác dụng với dung dịch HCl, nơi tiếp xúc giữa dung dịch axit với không khí.
2Cu + 4HCl + O2 → 2CuCl2 + 2 H2O
- Với HNO3, H2SO4 đặc :
Cu + 2H2SO4 đ → CuSO4 + SO2 + H2O
Cu + 4HNO3 đ → Cu(NO3)2 + 2NO2 + 2H2O
3Cu + 8HNO3 loãng → 3Cu(NO3)2 + 2NO + 4H2O
Tác dụng với dung dịch muối:
- Khử được ion kim loại đứng sau nó trong dung dịch muối.
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
5. Cách thực hiện phản ứng
- Trộn bột Cu với bột lưu huỳnh cho vào ống nghiệm sau đó đốt trên ngọn lửa đèn cồn.
6. Bạn có biết
- Hầu hết các kim loại như Fe, Al tác dụng với lưu huỳnh tạo thành muối sunfua.
7. Bài tập liên quan
Ví dụ 1: Đun nóng hỗn hợp gồm 0,64g bột đồng và 0,224 g bột lưu huỳnh trong ống nghiệm kín không có không khí. Hỗn hợp chất sau phản ứng là
A. Cu, CuS
B. CuS
C. CuS, S
D. S
Đáp án C
Hướng dẫn giải:
Ta có nCu = 0,01 mol, nS = 0,007 mol
PT: Cu + S → CuS
⇒ nCu > nS ⇒ Cu dư ⇒ Hỗn hợp chất sau phản ứng là Cu, CuS.
Ví dụ 2: Đun nóng hỗn hợp gồm 0,32g bột đồng và 0,224 g bột lưu huỳnh trong ống nghiệm kín không có không khí. Khối lượng của muối thu được là
A. 0,48g
B. 0,24g
C. 0,672g
D. 0,336g
Đáp án A
Hướng dẫn giải:
Ta có nCu = 0,005 mol; nS = 0.007 mol
PT: Cu + S → CuS
Ta có: nS > nCu ⇒ S dư, Cu hết
⇒ nCuS = nCu = 0,005 mol ⇒ mCuS = 0.48g
Ví dụ 3: Cho 1,1g hỗn hợp bột sắt và bột nhôm tác dụng vừa đủ với 1.28g bột lưu huỳnh. Phần trăm khối lượng của sắt trong hỗn hợp ban đầu là
A. 50,9%
B. 49,1%
C. 24,5%
D. 10,18%
Đáp án A
Hướng dẫn giải:
nS = 0,04 mol
Gọi số mol của Fe và Al lần lượt là x và y mol
Fe + S → FeS 2Al + 3S → Al2S3
x → x → x y → 1.5y
Ta có hệ phương trình: 56x + 27y = 1,1 và x + 1,5y = 0,04 mol
⇒ x = 0,01 mol và y = 0,02 mol
⇒ mFe = 0,02. 56 = 0,56g ⇒ %m Fe = 50,9%
8. Một số phương trình phản ứng hoá học khác của Đồng (Cu) và hợp chất:
2Cu + 4HCl + O2 → 2CuCl2 + 2H2O
2Cu + 2H2SO4 + O2 → 2CuSO4 + 2H2O
3Cu + 8HNO3 (loãng) → 3Cu(NO3)2 + 2NO + 4H2O