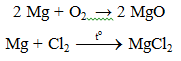Chúng tôi xin giới thiệu phương trình Mg + H2SO4 → MgSO4 + H2 gồm điều kiện phản ứng, cách thực hiện, hiện tượng phản ứng và một số bài tập liên quan giúp các em củng cố toàn bộ kiến thức và rèn luyện kĩ năng làm bài tập về phương trình phản ứng hóa học của Magie. Mời các bạn đón xem:
Phương trình Mg + H2SO4 → MgSO4 + H2
1. Phương trình phản ứng hóa học:
Mg + H2SO4 → MgSO4 + H2
2. Hiện tượng nhận biết phản ứng
Kim loại tan dần tạo thành dung dịch không màu đồng thời xuất hiện bọt khí thoát ra.
3. Điều kiện phản ứng
Không cần điều kiện
4. Bản chất của các chất tham gia phản ứng
a. Bản chất của Mg (Magie)
Mg là chất khử mạnh tác dụng với axit HCl, HNO3, H2SO4,..
b. Bản chất của H2SO4 (Axit sunfuric)
Axit sunfuric ở dạng loãng là một axit mạnh có đầy đủ tính chất thường gặp của một axit nên tác dụng với kim loại đứng trước H (trừ Pb) tạo thành muối sunfat.
5. Tính chất hóa học
5.1. Tính chất hóa học của Magie (Mg)
- Magie là chất khử mạnh:
Mg → Mg2+ + 2e
a. Tác dụng với phi kim
Lưu ý:
- Do Mg có ái lực lớn với oxi: 2Mg + CO2 → MgO. Vì vậy không dùng tuyết cacbonic để dập tắt đám cháy Mg.
b. Tác dụng với axit
- Với dung dịch HCl và H2SO4 loãng:
Mg + H2SO4 → MgSO4 + H2
- Với dung dịch HNO3:
4Mg + 10 HNO3 → 4 Mg(NO3)2 + NH4NO3 + 3 H2O
5.2. Tính chất hóa học của Axit sunfuric (H2SO4)
Axit sunfuric đặc có tính axit mạnh, oxi hóa mạnh với tính chất hóa học nổi bật như:
- Tác dụng với kim loại: Khi cho mảnh Cu vào trong H2SO4 tạo ra dung dịch có màu xanh và có khí bay ra với mùi sốc.
Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O
- Tác dụng với phi kim tạo thành oxit phi kim + H2O + SO2.
C + 2H2SO4 → CO2 + 2H2O + 2SO2 (nhiệt độ)
2P + 5H2SO4 → 2H3PO4 + 5SO2 + 2H2O
- Tác dụng với các chất khử khác.
2FeO + 4H2SO4 → Fe2(SO4)3 + SO2 + 4H2O
- H2SO4 còn có tính háo nước đặc trưng như đưa H2SO4 vào cốc đựng đường, sau phản ứng đường sẽ bị chuyển sang màu đen và phun trào với phương trình hóa học như sau.
C12H22O11 + H2SO4 → 12C + H2SO4.11H2O
6. Cách thực hiện phản ứng
Cho Mg tác dụng với dung dịch axit sunfuric loãng thu được muối magiesunfat
7. Bạn có biết
Kim loại tan dần tạo thành dung dịch không màu đồng thời xuất hiện bọt khí thoát ra.
8. Bài tập liên quan
Ví dụ 1: Phương trình hoá học nào sau đây sai?
A. Mg + H2SO4 → MgSO4 + H2
B. Al(OH)3 + 3HCl → AlCl3 +3H2O
C. FeO + 2HNO3 → Fe(NO3)2 + H2O
D. 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Hướng dẫn giải:
Đáp án C
3FeO + 10HNO3 → 3Fe(NO3)3 + 5H2O + NO2
Ví dụ 2: Cho kim loại X hóa trị II tác dụng vừa đủ với 3,2 g S đun nóng thu được 5,6 g muối. Kim loại X là:
A. Zn
B. Cu
C. Mg
D. Al
Hướng dẫn giải:
Đáp án C
Phương trình phản ứng : X + S → XS
nX = nS = 0,1 mol
Ta có: MX = (5,6-3,2)/0,1 = 24 ⇒ X là Mg
Ví dụ 3: Cho 6,4g hỗn hợp 2 kim loại Mg và Cu tác dụng với bột S dư trong điều kiện không có không khí thu được m g muối. Cho muối tác dụng với dung dịch H2SO4 loãng dư thu được 2,24 lít khí. Giá trị của m là
A. 8g
B. 9,6g
C. 16g
D. 1,6 g
Hướng dẫn giải:
Đáp án C
n SO42- = nH2S = 0,1 mol
mmuối = mKL + mSO42- = 6,4 + 0,1.96 = 16 g
9. Một số phương trình phản ứng hoá học khác của Magie và hợp chất:
3Mg + 2H3PO4 → Mg3(PO4)2 + 3H2
Mg + 4HNO3 → Mg(NO3)2 + 2NO2 + 2H2O
4Mg + 10HNO3 → 4Mg(NO3)2 + NH4NO3 + 3H2O
5Mg + 12HNO3 → 5Mg(NO3)2 + N2 + 6H2O
4Mg + 10HNO3 → 4Mg(NO3)2 + N2O + 5H2O