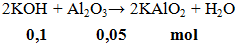Chúng tôi xin giới thiệu phương trình 2KOH + Al2O3 → 2KAlO2 + H2O gồm điều kiện phản ứng, cách thực hiện, hiện tượng phản ứng và một số bài tập liên quan giúp các em củng cố toàn bộ kiến thức và rèn luyện kĩ năng làm bài tập về phương trình phản ứng hóa học của Kali. Mời các bạn đón xem:
Phương trình 2KOH + Al2O3 → 2KAlO2 + H2O
1. Phương trình phản ứng hóa học:
2KOH + Al2O3 → 2KAlO2 + H2O
2. Hiện tượng nhận biết phản ứng
- Al2O3 tan dần, sau phản ứng thu được dung dịch trong suốt.
3. Điều kiện phản ứng
- Phản ứng xảy ra ở nhiệt độ thường.
4. Tính chất hóa học
- KOH là một bazo mạnh có khả năng làm thay đổi màu sắc các chất chỉ thị như khiến quỳ tím chuyển sang màu xanh, còn dung dịch phenolphtalein không màu thành màu hồng.
Ở điều kiện nhiệt độ phòng, KOH tác dụng với oxit axit như SO2, CO2
KOH + SO2 → K2SO3 + H2O
KOH + SO2 → KHSO3
- KOH tác dụng với axit tạo thành muối và nước
KOH(dd) + HCl(dd) → KCl(dd) + H2O
- KOH tác dụng với các axit hữu cơ để tạo thành muối và thủy phân este, peptit
RCOOR1 + KOH → RCOOK + R1OH
- KOH tác dụng với kim loại mạnh tạo thành bazo mới và kim loại mới
KOH + Na → NaOH + K
- KOH tác dụng với muối để tạo thành muối mới và axit mới
2KOH + CuCl2 → 2KCl + Cu(OH)2↓
- KOH là một bazo mạnh, trong nước phân ly hoàn toàn thành ion Na+ và OH-
Phản ứng với một số oxit kim loại mà oxit, hidroxit của chúng lưỡng tính như nhôm, kẽm,…
2KOH + 2Al + 2H2O → 2KAlO2 + 3H2↑
2KOH + Zn → K2ZnO2 + H2↑
- KOH phản ứng với một số hợp chất lưỡng tính
KOH + Al(OH)3 → KAlO2 + 2H2O
2KOH + Al2O3 → 2KAlO2 + H2O
5. Cách thực hiện phản ứng
- nhỏ từ từ KOH vào ống nghiệm chứa Al2O3.
6. Bạn có biết
- Các oxit ZnO, Cr2O3 cũng tác dụng với dung dịch KOH.
7. Bài tập liên quan
Ví dụ 1: KOH không thể phản ứng với oxit nào sau?
A. SO2.
B. Al2O3.
C. ZnO.
D. MgO.
Hướng dẫn giải
KOH không thể phản ứng với MgO.
Đáp án D.
Ví dụ 2: Chất nào sau đây không phản ứng với KOH ở điều kiện thường?
A. Al2O3,
B. ZnO.
C. Al(OH)3,
D. FeO.
Hướng dẫn giải
FeO không phản ứng với KOH ở điều kiện thường.
Đáp án D.
Ví dụ 3: Khối lượng Al2O3 cần dung để phản ứng vừa đủ với 100ml KOH 1M là
A. 5,1g.
B. 0,51g.
C. 10,2g.
D. 1,02g.
Hướng dẫn giải
m = 0,05.102 =5,1g.
Đáp án A.
8. Một số phương trình phản ứng hóa học khác của Kali và hợp chất:
KOH + NH4Cl -to→ KCl+ NH3+ H2O