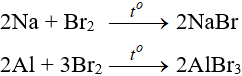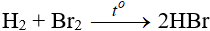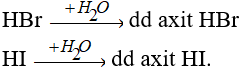Chúng tôi xin giới thiệu phương trình 2Ag + Br2 → 2AgBr ↓ gồm điều kiện phản ứng, cách thực hiện, hiện tượng phản ứng và một số bài tập liên quan giúp các em củng cố toàn bộ kiến thức và rèn luyện kĩ năng làm bài tập về phương trình phản ứng hóa học của Bạc. Mời các bạn đón xem:
Phương trình 2Ag + Br2 → 2AgBr ↓
1. Phương trình phản ứng hóa học:
2Ag + Br2 → 2AgBr ↓
2. Hiện tượng nhận biết phản ứng
- Xuất hiện kết tủa vàng nhạt
3. Điều kiện phản ứng
- ở nhiệt độ 150 - 200oC
4. Tính chất hoá học
a. Tính chất hoá học của Ag
- Bạc kém hoạt động. Ag → Ag+ + 1e
Tác dụng với phi kim
- Bạc không bị oxi hóa trong không khí dù ở nhiệt độ cao.
Tác dụng với ozon
2Ag + O3 → Ag2O + O2
Tác dụng với axit
- Bạc không tác dụng với HCl và H2SO4 loãng, nhưng tác dụng với các axit có tính oxi hóa mạnh, như HNO3 hoặc H2SO4 đặc, nóng.
3Ag + 4HNO3 (loãng) → 3AgNO3 + NO + 2H2O
2Ag + 2H2SO4 (đặc, nóng) → Ag2SO4 + SO2 + 2H2O
Tác dụng với các chất khác
- Bạc có màu đen khi tiếp xúc với không khí hoặc nước có mặt hidro sunfua:
4Ag + 2H2S + O2 (kk) → 2Ag2S + 2H2O
- Bạc tác dụng được với axit HF khi có mặt của oxi già:
2Ag + 2HF (đặc) + H2O2 → 2AgF + 2H2O
2Ag + 4KCN (đặc) + H2O2 → 2K[Ag(CN)2] + 2KOH
b. Tính chất hoá học của Br2
Tác dụng với kim loại
Sản phẩm tạo muối tương ứng
Tác dụng với hidro
Độ hoạt động giảm dần từ Cl → Br → I
Các khí HBr, HI tan vào nước tạo dung dịch axit.
Về độ mạnh axit thì lại tăng dần từ HCl < HBr < HI.
Tính khử của Br2, HBr
- Brom thể hiện tính khử khi gặp chất oxi hóa mạnh (như nước clo, …)
Br2 + 5Cl2 + 6H2O → 2HBrO3 (Axit bromic) + 10HCl
- Tính khử của HBr (ở trạng thái khí cũng như trong dd) mạnh hơn HCl. HBr khử được H2SO4 đặc thành SO2.
2HBr + H2SO4đ → Br2 + SO2 + 2H2O
- Dd HBr không màu, để lâu trong không khí trở nên có màu vàng nâu vì bị oxi hóa (dd HF và HCl không có phản ứng này):
4HBr + O2 → 2H2O + 2Br2
5. Cách thực hiện phản ứng
- Cho bạc tác dụng với dung dịch brom
6. Bạn có biết
- Ag là kim loại có tính khử yếu nên khi tác dụng với các chất có tính oxi hóa mạnh như Br2...ở nhiệt độ cao
7. Bài tập liên quan
Ví dụ 1: Khi cho bạc tác dụng với khí clo sẽ tạo thành màu gì ?
A. Kết tủa màu vàng nhạt
B. Kết tủa màu vàng cam
C. Kết tủa màu đen
D. Kết tủa màu trắng
Đáp án: A
Ví dụ 2: Cho 2,16 g bạc tác dụng với dung dịch brom thu được m g kết tủa vàng nhạt. Giá trị của m là:
A. 2,82 g
B. 3,76 g
C. 28,2 g
D. 5,64 g
Hướng dẫn:
Phương trình phản ứng: 2Ag + Br2 → 2AgBr
nAgBr = nAg = 0,02 mol ⇒ mAgBr = 0,02. 188 = 3,76 g
Đáp án: B
Ví dụ 3: Cho m (g) bạc tác dụng vừa đủ với dung dịch brom thu được 5,64 g kết tủa vàng nhạt. Giá trị của m là:
A. 2,16 g
B. 1,62 g
C. 1,08 g
D. 3,24 g
Hướng dẫn:
Phương trình phản ứng: 2Ag + Br2 → 2AgBr
nAg = nAgBr = 0,03 mol → mAg = 0,03 .108 = 3,24 g
Đáp án: D
8. Một số phương trình phản ứng hoá học khác của Bạc (Ag) và hợp chất: