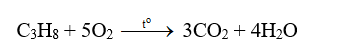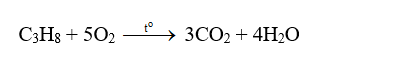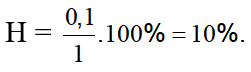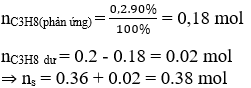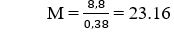Chúng tôi xin giới thiệu phương trình C3H8 → CH4 + C2H4 gồm điều kiện phản ứng, cách thực hiện, hiện tượng phản ứng và một số bài tập liên quan giúp các em củng cố toàn bộ kiến thức và rèn luyện kĩ năng làm bài tập về phương trình phản ứng hóa học. Mời các bạn đón xem:
Phương trình C3H8 → CH4 + C2H4
1. Phản ứng hóa học:
C3H8 → CH4 + C2H4
2. Điều kiện phản ứng
- Nhiệt độ cao.
- Xúc tác: Ni, Fe, Cr2O3, Pt...
3. Cách thực hiện phản ứng
- Dưới tác dụng của nhiệt cao và có xúc tác thích hợp C3H8 có thể bị phân hủy thành CH4 và C2H4
4. Hiện tượng nhận biết phản ứng
- Dẫn hỗn hợp sản phẩm thu được qua bình đựng dung dịch brom thấy dung dịch brom bị nhạt màu.
5. Phản ứng hóa học
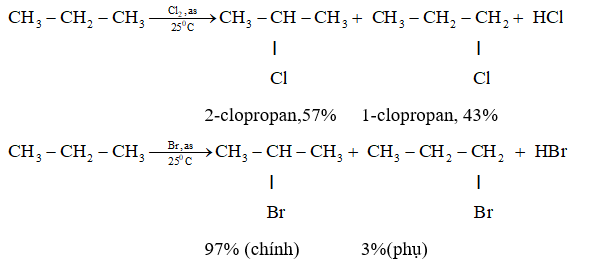
a. Phản ứng thế bởi halogen
- Khi chiếu sáng hoặc đốt nóng hỗn hợp propan và clo sẽ xảy ra phản ứng thế lần lượt các nguyên tử hidro bằng clo. Tương tự như metan.
- Phản ứng thế H bằng halogen thuộc loại phản ứng halogen hóa, sản phẩm hữu cơ có chứa halogen gọi là dẫn xuất halogen.
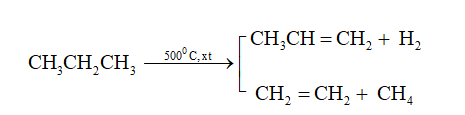
b. Phản ứng tách (gãy liên kết C-C và C-H )
- Dưới tác dụng của nhiệt và xúc tác (Cr2O3, Fe, Pt,...), các ankan không những bị tách hidro tạo thành các hidrocacbon không no mà còn bị gãy các liên kết C-C tạo ra các phân tử nhỏ hơn.
c. Phản ứng oxi hóa
- Khi đốt, propan bị cháy tạo ra CO2, H2O và tỏa nhiều nhiệt
- Nếu không đủ oxi, ankan bị cháy không hoàn toàn, khi đó ngoài CO2 và H2O còn tạo ra các sản phẩm như CO, than muội, không những làm giảm năng suất tỏa nhiệt mà còn gây độc hại cho môi trường.
6. Bạn có biết
- Phản ứng trên được gọi là phản ứng cracking, ngoài CH4 và C2H4 sản phẩm sinh ra có thể có cả H2 và C3H6.
- Dù phản ứng xảy ra theo hướng nào thì phản ứng không làm thay đổi khối lượng hỗn hợp: mtrước phản ứng = msau phản ứng.
- Phản ứng luôn làm tăng số mol khí: nsau > ntrước
7. Bài tập liên quan
Ví dụ 1: Crackinh C3H8 thu được hỗn hợp X gồm H2, C2H4, CH4, C3H6, C3H8 có dX/He = 10. Hiệu suất phản ứng là:
A. 10%
B. 80%.
C. 70%.
D. 60%
Hướng dẫn.
Cracking C3H8:
C3H8 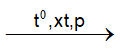
x x x mol
C3H8 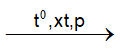
y y y mol
Ta thấy trong X còn lại 1 phần C3H8 chưa bị crackinh hết.
MX = MHe.10 = 4.10 = 40 g/mol
Giả sử có 1 mol C3H8.
Bảo toàn khối lượng có: mtrước = msau hay 1.44 = nx.40 → nx = 1,1 mol
Theo các PTHH có nC3H8pư = nsau - ntrước = 1,1 - 1 = 0,1 mol
Vậy
Đáp án A.
Ví dụ 2: Crackinh 8,8 gam propan thu được hỗn hợp A gồm H2, CH4, C2H4, C3H6 và một phần propan chưa bị craking. Biết hiệu suất phản ứng là 90%. Khối lượng phân tử trung bình của A là:
A. 39,6
B. 23,16
C. 2,315
D. 3,96
Hướng dẫn.
Cracking C3H8:
C3H8 → CH4 + C2H4
C3H8 → H2 + C3H6
Có thể nhận thấy cứ mất 1 mol C3H8 sẽ tạo thành 2 mol sản phẩm. Mà nC3H8 = 0.2 mol
Hiệu suất H = 90%
⇒ số mol sp tạo thành là: 0,2.90%.2 = 0.36 mol;
Bảo toàn khối lượng, tổng khối lượng các chất sau cracking vẫn là 8.8 gam
Do đó, khối lượng mol hỗn hợp sau là:
Đáp án B.
Ví dụ 3: Craking m gam propan thu được hợp A gồm H2, CH4, C2H4, C2H6 và một phần propan chưa bị craking. Đốt cháy hoàn toàn A thu được 9 gam H2O và 17,6 gam CO2. Giá trị của m là:
A. 4,4g
B. 6,6g
C. 8,8g
D. 11g
Hướng dẫn
Sản phẩm sinh ra khi đốt cháy A tương tự như đốt cháy propan
npropan = nH2O – nCO2 = 9/18 - 17,6/44 = 0,1 mol
⇒ mpropan = m = 0,1.44 = 4,4 gam
Đáp án A.
8. Một số phương trình phản ứng hoá học khác của Ankan và hợp chất: