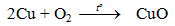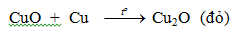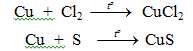Chúng tôi xin giới thiệu phương trình 3Cu + 8HNO3 (loãng) → 3Cu(NO3)2 + 2NO + 4H2O gồm điều kiện phản ứng, cách thực hiện, hiện tượng phản ứng và một số bài tập liên quan giúp các em củng cố toàn bộ kiến thức và rèn luyện kĩ năng làm bài tập về phương trình phản ứng hóa học của Đồng. Mời các bạn đón xem:
Phương trình 3Cu + 8HNO3 (loãng) → 3Cu(NO3)2 + 2NO + 4H2O
1. Phương trình phản ứng hóa học:
3Cu + 8HNO3 (loãng) → 3Cu(NO3)2 + 2NO + 4H2O
2. Hiện tượng nhận biết phản ứng
- Có khí không màu hóa nâu trong không khí.
3. Điều kiện phản ứng
- Nhiệt độ phòng.
4. Tính chất hoá học
- Là kim loại kém hoạt động, có tính khử yếu.
Tác dụng với phi kim:
- Cu phản ứng với oxi khi đun nóng tạo CuO bảo vệ nên Cu không bị oxi hoá tiếp tục.
- Khi tiếp tục đun nóng tới (800-1000oC)
- Tác dụng với Cl2, Br2, S...
Tác dụng với axit:
- Cu không tác dụng với dung dịch HCl, H2SO4 loãng.
- Khi có mặt oxi, Cu tác dụng với dung dịch HCl, nơi tiếp xúc giữa dung dịch axit với không khí.
2Cu + 4HCl + O2 → 2CuCl2 + 2 H2O
- Với HNO3, H2SO4 đặc :
Cu + 2H2SO4 đ → CuSO4 + SO2 + H2O
Cu + 4HNO3 đ → Cu(NO3)2 + 2NO2 + 2H2O
3Cu + 8HNO3 loãng → 3Cu(NO3)2 + 2NO + 4H2O
Tác dụng với dung dịch muối:
- Khử được ion kim loại đứng sau nó trong dung dịch muối.
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
5. Cách thực hiện phản ứng
- Cho mảnh Cu vào ống nghiệm sau đó cho dung dịch HNO3 loãng vào.
6. Bạn có biết
- Hầu hết các kim loại (trừ Au, Pt) tác dụng với HNO3 ( loãng) tạo thành muối nitrat và có khí NO là khí không màu hóa nâu trong không khí.
7. Bài tập liên quan
Ví dụ 1: Cho sơ đồ phản ứng Cu + HNO3 (l) → Cu(NO3)2 + NO + H2O. Tổng hệ số cân bằng của các chất trong phản ứng là:
A. 20
B. 21
C. 19
D. 18
Đáp án A
Hướng dẫn giải:
Vì
Cu → Cu2+ + 2e……x3
N+5 + 3e → N+2………x2
⇒ hệ số cân bằng của các chất trong pt lần lượt là 3, 8, 3, 2, 4.
3Cu + 8HNO3 (l) → 3Cu(NO3)2 + 2NO + 4H2O
Ví dụ 2: Cho phản ứng 3Cu + 8HNO3 (l) → 3Cu(NO3)2 + 2NO + 4H2O. Cu đóng vai trò
A. chất khử
B. chất oxi hóa
C. vừa là chất oxi hóa, vừa là chất khử
D. không là chất oxi hóa, không là chất khử
Đáp án A
Hướng dẫn giải:
Vì Cu có số OXH tăng từ 0 → + 2.
Ví dụ 3: Cho phản ứng 3Cu + 8HNO3 (l) → 3Cu(NO3)2 + 2NO + 4H2O. Tỉ lệ số e nhường : số e nhận là
A. 3:2
B. 2:3
C. 3:8
D. 8:3
Đáp án B
Hướng dẫn giải:
Vì Cu → Cu2+ + 2e ⇒ số e nhường là 2e
N+5 + 3e → N+2 ⇒ số e nhận là 3e
⇒ số e nhường : số e nhận là 2:3.
8. Một số phương trình phản ứng hoá học khác của Đồng (Cu) và hợp chất:
Cu + 4HNO3 (đặc, nóng) → Cu(NO3)2 + 2NO2 + 2H2O
Cu + 2H2SO4 (đặc, nóng) → CuSO4 + SO2 + 2H2O
3Cu + 8HCl + 8NaNO3 → 3Cu(NO3)2 + 2NO + 8NaCl + 4H2O
3Cu + 8HCl + 2NaNO3 → 3CuCl2 + 2NO + 2NaCl + 4H2O
3Cu + 8HCl + 8KNO3 → 3Cu(NO3)2 + 2NO + 8KCl + 4H2O