Chúng tôi xin giới thiệu phương trình Al2O3+ 6HCl → 2AlCl3+ 3H2O gồm điều kiện phản ứng, cách thực hiện, hiện tượng phản ứng và một số bài tập liên quan giúp các em củng cố toàn bộ kiến thức và rèn luyện kĩ năng làm bài tập về phương trình phản ứng hóa học của Nhôm. Mời các bạn đón xem:
Phương trình Al2O3+ 6HCl → 2AlCl3+ 3H2O
1. Phương trình phản ứng hóa học:
Al2O3 + 6HCl → 2AlCl3 + 3H2O
2. Hiện tượng nhận biết phản ứng
- Phản ứng hoà tan chất rắn nhôm oxit tạo dung dịch trong suốt.
3. Điều kiện phản ứng
- Phản ứng diễn ra mãnh liệt hơn khi tăng nhiệt độ.
4. Tính chất hoá học
a. Tính chất hoá học của Al2O3
- Al2O3 là oxit lưỡng tính.
+ Tác dụng với axit:
Al2O3 + 6HCl → 2AlCl3 + 3H2O
+ Tác dụng với dung dịch bazơ mạnh
Al2O3 + 2NaOH → NaAlO2 + H2O
hay
Al2O3 + 2NaOH + 3H2O → 2Na[Al(OH)4]
Al2O3 + 2OH- → 2AlO2- + H2O
- Al2O3 tác dụng với C
Al2O3 + 9C 
b. Tính chất hoá học HCl
- Dung dịch axit HCl có đầy đủ tính chất hoá học của một axit mạnh.
Tác dụng chất chỉ thị:
Dung dịch HCl làm quì tím hoá đỏ (nhận biết axit)
HCl → H+ + Cl-
Tác dụng với kim loại
Tác dụng với KL (đứng trước H trong dãy Bêkêtôp) tạo muối (với hóa trị thấp của kim loại) và giải phóng khí hidrô (thể hiện tính oxi hóa)
Fe + 2HCl 
2Al + 6HCl 
Cu + HCl → không có phản ứng
Tác dụng với oxit bazo và bazo:
Sản phẩm tạo muối và nước
NaOH + HCl → NaCl + H2 O
CuO + 2HCl 
Fe2 O3 + 6HCl
Tác dụng với muối (theo điều kiện phản ứng trao đổi)
CaCO3 + 2HCl → CaCl2 + H2O + CO2↑
AgNO3 + HCl → AgCl↓ + HNO3
(dùng để nhận biết gốc clorua )
Ngoài tính chất đặc trưng là axit , dung dịch axit HCl đặc còn thể hiện vai trò chất khử khi tác dụng chất oxi hoá mạnh như KMnO4, MnO2, K2 Cr2O7, MnO2, KClO3 ……
4HCl + MnO2 
K2 Cr2 O7 + 14HCl → 3Cl2 + 2KCl + 2CrCl3 + 7H2 O
Hỗn hợp 3 thể tích HCl và 1 thể tích HNO3 đặc được gọi là hỗn hợp nước cường toan ( cường thuỷ) có khả năng hoà tan được Au ( vàng)
3HCl + HNO3 → 2Cl + NOCl + 2H2O
NOCl → NO + Cl
Au + 3Cl → AuCl3
5. Cách thực hiện phản ứng
- Cho Al2O3 phản ứng với dung dịch axit HCl tạo muối tan AlCl3 và nước.
6. Bạn có biết
Al2O3 cũng
7. Bài tập liên quan
Ví dụ 1: Hòa tan 25,8 gam hỗn hợp gồm bột Al và Al2O3 trong dung dịch HCl dư. Sau phản ứng người ta thu được 0,6 gam khí Hidro. Khối lượng muối AlCl3 thu được là bao nhiêu?
A. 53,4 gam.
B. 43,5 gam.
C. 12,5 gam
D. 54,3 gam.
Hướng dẫn giải
Chọn A.
2Al + 6HCl → 2AlCl3 + 3H2↑ (1)
Al2O3 + 6HCl → 2AlCl3 + 3H2O (2)
nH2=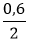
Theo phương trình (1) có nAl=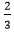
⇒ mAl=0,2.27=5,4 gam ⇒ mAl2O3=25,8-5,4=20,4 gam
⇒ nAl2O3=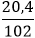
⇒ nAlCl3=0,2+0,2=0,4 mol
⇒ mAlCl3=0,4.133,5=53,4 gam
Ví dụ 2:Cho các chất: Al, Al2O3, Al2(SO4)3, ZnO, Sn(OH)2, Zn(OH)2, NaHS, KHSO3, KHSO4, Fe(NO3)2, (NH4)2CO3. Số chất đều phản ứng được với dung dịch HCl, dung dịch NaOH là:
A. 7
B. 9
C. 10
D. 8
Hướng dẫn giải
Chọn B.
Các chất đều phản ứng được với dung dịch HCl và dung dịch NaOH là: Al, Al2O3, ZnO, Sn(OH)2, Zn(OH)2, NaHS, KHSO3, Fe(NO3)2, (NH4)2CO3.
Ví dụ 3:Oxit nhôm không phản ứng với chất nào sau đây?
A. HCl
B. H2
C. Ca(OH)2
D. NaOH
Hướng dẫn giải
Chọn B.
Al2O3 + 6HCl → 2AlCl3 + 3H2O
Al2O3 + Ca(OH)2 → Ca(AlO2)2 + H2O
Al2O3 + 2NaOH → 2NaAlO2 + H2O
8. Một số phương trình phản ứng hoá học khác của Nhôm (Al) và hợp chất:
Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
Al2O3 + 6HNO3 → 2Al(NO3)3 + 3H2O
Al2O3 + Ca(OH)2 → H2O + Ca(AlO2)2

