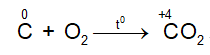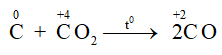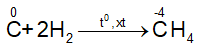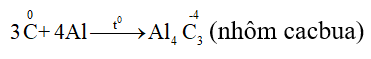Chúng tôi xin giới thiệu phương trình C + HNO3 → CO2 + NO2 + H2O gồm điều kiện phản ứng, cách thực hiện, hiện tượng phản ứng và một số bài tập liên quan giúp các em củng cố toàn bộ kiến thức và rèn luyện kĩ năng làm bài tập về phương trình phản ứng hóa học. Mời các bạn đón xem:
Phương trình C + HNO3 → CO2 + NO2 + H2O
1. Phương trình phản ứng hóa học:
C + 4HNO3 → CO2 + 4NO2 + 2H2O
2. Hiện tượng nhận biết phản ứng.
- Chất rắn màu đen (C) tan dần và xuất hiện khí nâu đỏ Nito dioxit (NO2) làm sủi bọt khí.
3. Điều kiện phản ứng
- nhiệt độ
4. Tính chất hóa học
- Trong các dạng tồn tại của C, C vô định hình hoạt động hơn cả về mặt hóa học.
- Trong các phản ứng hóa học C thể hiện hai tính chất: Tính oxi hóa và tính khử. Tuy nhiên tính khử vẫn là chủ yếu của C.
a. Tính khử
- Tác dụng với oxi
Ở nhiệt độ cao C lại khử CO2 theo phản ứng:
- Tác dụng với oxit kim loại:
+ C khử được oxit của các kim loại đứng sau Al trong dãy hoạt động hóa học của kim loại:
CuO + C → Cu + CO (tº)
Fe2O3 + 3C → 2Fe + 3CO (tº)
+ Với CaO và Al2O3:
CaO + 3C → CaC2 + CO (trong lò điện)
2Al2O3 + 9C → Al4C3 + 6CO (2000ºC)
- Tác dụng với các chất oxi hóa mạnh thường gặp H2SO4 đặc, HNO3, KNO3, KClO3, K2Cr2O7, ... trong các phản ứng này, C bị oxi hóa đến mức +4 (CO2).
C + 2H2SO4 đặc → CO2 + 2SO2 + 2H2O (tº)
C + 4HNO3 đặc → CO2 + 4NO2 + 2H2O (tº)
C + 4KNO3 → 2K2O + CO2 + 4NO2 (tº)
- Khi nhiệt độ cao, C tác dụng được với hơi nước:
C + H2O → CO + H2 (1000ºC)
C + 2H2O → CO2 + 2H2
b. Tính oxi hóa
- Tác dụng với hidro
- Tác dụng với kim loại
5. Cách thực hiện phản ứng
- Cho cacbon tác dụng với dung dịch HNO3
6. Bạn có biết
- Khi đun nóng, HNO3 đặc có thể oxi hoá được các phi kim như C, S, P
7. Bài tập liên quan
Câu 1. Cacbon có thể phản ứng với tất cả dãy chất hóa học nào sau đây
A. O2, CuO, Cl2, HNO3
B. O2, ZnO, HNO3, CO2
C. O2, Al, H2SO4 đặc, CO2
D. O2, ZnO, H2SO4 đặc, Al
Cacbon có thể phản ứng với tất cả dãy hóa chất sau: O2, ZnO, H2SO4 đặc, Al
Câu 2. C thể hiện tính khử ở phản ứng nào sau đây?
A. 2C + Ca CaC2
B. C + 2H2 CH4
C. C + CO2 2CO
D. 4Al+ 3C Al4C3
Câu 3. Phản ứng nào sau đây, cacbon thể hiện tính oxi hóa?
A. C + O2 → CO2
B. C + 2CuO → 2Cu + CO2
C. 3C + 4Al → Al4C3
D. C + H2O → CO + H2
Câu 4. Cho m gam than tác dụng với dng dịch HNO3 đặc nóng dư, thu được 5,6 lít hỗn hợp 2 khí (đktc). Giá trị của m là
A. 1,2
B. 0,6
C. 2,5
D. 3
nhỗn hợp khí = 0,1 mol
C + 4HNO3 → CO2 + 4NO2 + 2H2O
x x 4x
5x = 0,25 => x = 0,05 => m = 0,6 gam
Câu 5. Thực hiện các thí nghiệm sau:
(1) Sục khí CO2 vào dung dịch Ca(OH)2 dư
(2) Sục khí NH3 dư vào dung dịch AlCl3
(3) Sục khí CO2 dư vào dung dịch NaAlO2
(4) Cho dung dịch AgNO3 vào dung dịch FeCl3
(5) Cho dung dịch HCl vào dung dịch K2SiO3
(6) Cho ure vào dung dịch Ca(OH)2
Sau khi kết thúc thí nghiệm, số trường hợp thu được kết tủa là
A. 5
B. 3
C. 6
D. 4
Các thí nghiệm xảy ra các phản ứng:
(1). CO2 + Ca(OH)2 (dư) → CaCO3↓ + H2O
(2). 3NH3 + AlCl3 + 3H2O → Al(OH)3↓ + 3NH4Cl
(3). CO2 + 2NaAlO2 + 3H2O → 2Al(OH)3↓ + Na2CO3.
(4). 3AgNO3 + FeCl3 → 3AgCl↓ + Fe(NO3)3.
(5). 2HCl + K2SiO3 → H2SiO3↓ + 2KCl
(6). (NH2)2CO + Ca(OH)2 → CaCO3↓ + 2NH3.
⇒ cả 6 thí nghiệm đều thu được kết tủa
⇒ chọn đáp án A
Câu 6. Tính oxi hóa của cacbon thể hiện ở phản ứng nào trong các phản ứng sau:
A. C + O2 CO2
B. C + 4HNO3 → CO2 + 4NO2 + 2H2O
C. 2C + Ca CaC2
D. C + CO2 2CO
C thể hiện tính oxi hóa khi tác dụng với chất có tính khử như H2; hầu hết các kim loại (Na, Ca, Al, Zn…)
Câu 7. Cho luồng khí C dư qua hỗn hợp các oxit CuO, Fe2O3, ZnO, MgO nung nóng ở nhiệt độ cao. Sau phản ứng, hỗn hợp chất rắn còn lại là
C chỉ khử được các oxit kim loại đứng sau Al => C khử được CuO, Fe2O3, ZnO và không khử được MgO
Câu 8. Câu nào đúng trong các câu sau đây?
A. Kim cương là chất tinh thể trong suốt, không màu, dẫn điện, dẫn nhiệt
B. Than chì mềm do có cấu trúc lớp, các lớp lân cận liên kết với nhau bằng lực tương tác yếu.
C. Than gỗ, than xương chỉ có khả năng hấp phụ các chất khí.
D. Trong các hợp chất của cacbon, nguyên tố cacbon chỉ có các số oxi hoá -4 và +4.
A sai vì kim cương không dẫn điện
C sai vì than gỗ, than xương hấp phụ các chất khí và cả chất tan trong dung dịch
D sai còn có +2 ví dụ như CO
Câu 9. Cho các thí nghiệm sau:
(a) Cho dung dịch Al(NO3)3tác dụng với dung dịch NH3dư
(b) Cho dung dịch KOH dư vào dung dịch AlCl3
(c) Cho dung dịch HCl dư vào dung dịch NaAlO2
(d) Dẫn khí CO2 dư vào dung dịch KAlO2
Số thí nghiệm thu được kết tủa khi phản ứng kết thúc là :
A. 1
B. 2
C. 3
D. 4
Các phản ứng xảy ra:
(a) Al(NO3)3 + 3NH3 + 3H2O → Al(OH)3¯ + 3NH4NO3
(b) AlCl3 + 3NaOHdư → Al(OH)3¯ + 3NaCl ;
Al(OH)3 + NaOH →Na[Al(OH)4]
(c) NaAlO2 + HCl + H2O → Al(OH)3¯ + NaCl ;
Al(OH)3 + 3HCl → AlCl3 + 3H2O
(d) CO2 dư + KAlO2+ 2H2O → Al(OH)3¯ + KHCO3
Vậy có 2 phản ứng tạo kết tủa là (a), (d).
8. Một số phương trình phản ứng hoá học khác của Carbon (C) và hợp chất:
C + HNO3 → CO2 + NO2 + H2O