Chúng tôi xin giới thiệu phương trình C2H5OH + Na → C2H5ONa + H2 gồm điều kiện phản ứng, cách thực hiện, hiện tượng phản ứng và một số bài tập liên quan giúp các em củng cố toàn bộ kiến thức và rèn luyện kĩ năng làm bài tập về phương trình phản ứng hóa học. Mời các bạn đón xem:
Phương trình C2H5OH + Na → C2H5ONa + H2
1. Phương trình phản ứng hóa học
2C2H5OH + 2Na → 2C2H5ONa + H2
2. Hiện tượng nhận biết phản ứng.
- Có bọt khí thoái ra, mẩu natri tan dần.
3. Điều kiện phản ứng
- Điều kiện: Không có
4. Bản chất của C2H5OH (Ancol etylic) tham gia phản ứng
Trong phân tử ancol có liên kết C – OH, đặc biệt là liên kết O–H phân cực mạnh. Vì vậy nhóm – OH nhất là nguyên tử H sẽ dễ bị thay thế hoặc là tách ra trong các phản ứng hóa học. Đây là phản ứng đặc trưng của ancol, thế nguyên tử H của nhóm OH ancol.
5. Tính chất hóa học
5.1. Tính chất hóa học của C2H5OH
a. Etylic C2H5OH phản ứng với oxi
Rượu etylic dễ cháy, khi cháy không có khói và ngọn lửa có màu xanh da trời,toả nhiều nhiệt
C2H5OH + 3O2 2CO2 + 3H2O
b. Etanol C2H5OH tác dụng với Na, NaNH3
Etanol chỉ tác dụng với Na hay NaNH2
2C2H5OH + Na → 2C2H5ONa + H2↑
C2H5OH + NaNH2 → C2H5ONa + NH3
c. Etanol C2H5OH phản ứng với axit axetic
Tổng quát phản ứng este hóa
ROH + R’COOH ↔ R’COOR + H2O
Phản ứng được thực hiện trong môi trường axit và đun nóng.
Phản ứng có tính thuận nghịch nên chú ý đến chuyển dịch cân bằng.
C2H5OH + CH3COOH ↔ CH3COOC2H5 + H2O
5.2. Tính chất hóa học của Na
- Natri có tính khử rất mạnh: Na → Na+ + 1e
a. Tác dụng với phi kim
4Na + O2 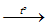
2Na + Cl2 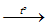
- Khi đốt trong không khí hay trong oxi, Na cháy tạo thành các oxit (oxit thường, peoxit và supeoxit) và cho ngọn lửa có màu vàng đặc trưng.
b. Tác dụng với axit
- Natri dễ dàng khử ion H+ trong dung dịch axit loãng (HCl, H2SO4 loãng...) thành hidro tự do.
2Na + 2HCl → 2NaCl + H2.
2Na + H2SO4 → Na2SO4 + H2.
c. Tác dụng với nước
- Natri đều tác dụng mãnh liệt với nước tạo thành dung dịch kiềm và giải phóng khí hidro.
2Na + 2H2O → 2NaOH + H2.
d. Tác dụng với hidro
- Natri tác dụng với hidro ở áp suất khá lớn và nhiệt độ khoảng 350 – 400oC tạo thành natri hidrua.
2Na (lỏng) + H2 (khí) 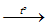
6. Cách thực hiện phản ứng
- Cho mẩu natri vào cốc (ống nghiệm) đựng rượu etylic
7. Bạn có biết
- Tương tự nước, rượu etylic tác dụng được với, giải phóng khí, đó là khí hidro.
8. Bài tập liên quan
Câu 1. Cho một mẫu natri vào ống nghiệm đựng rượu etylic. Hiện tượng quan sát được là
A. có bọt khí màu nâu thoát ra
B. mẫu natri tan dần không có bọt khí thoát ra
C. mẫu natri nằm dưới bề mặt chất lỏng và không tan
D. có bọt khí không màu thoát ra và natri tan dần
Lời giải:
Đáp án: D
Giải thích:
Cho một mẫu natri vào ống nghiệm đựng rượu etylic. Hiện tượng quan sát được là
Phương trình hóa học: 2C2H5OH + 2Na → 2C2H5ONa + H2↑.
có bọt khí không màu thoát ra và natri tan dần
Câu 2. Rượu etylic cháy trong không khí, hiện tượng quan sát được là
A. ngọn lửa màu đỏ, tỏa nhiều nhiệt.
B. ngọn lửa màu vàng, tỏa nhiều nhiệt.
C. ngọn lửa màu xanh, tỏa nhiều nhiệt.
D. ngọn lửa màu xanh, không tỏa nhiệt.
Lời giải:
Đáp án: C
Giải thích:
Rượu etylic cháy trong không khí, hiện tượng quan sát được là: ngọn lửa màu xanh, tỏa nhiều nhiệt.
Câu 3. Chọn nhận định sai khi nói về ancol.
A. Khi đốt cháy hoàn toàn ancol no, mạch hở thì thu được số mol CO2 nhỏ hơn số mol nước.
B. Các ancol đa chức có từ 2 nhóm -OH gắn ở 2 cacbon liên tiếp trên mạch có khả năng phản ứng hòa tan Cu(OH)2 tạo dung dịch xanh lam.
C. Ancol etylic tan vô hạn trong nước.
D. Ancol benzylic tác dụng với dung dịch NaOH tạo natri benzylat và nước.
Lời giải:
Đáp án: D
Câu 4. Cho chuỗi phản ứng sau:
A → C2H5OH → B → CH3COONa → C → C2H2
Chất A, B, C lần lượt là
A. C6H12O6, CH3COOH, CH4.
B. C6H6, CH3COOH, C2H4.
C. C6H12O6, C2H5ONa, CH4.
D. C2H4, CH3COOH, C2H5ONa.
Lời giải:
Đáp án: A
Giải thích:
C6H12O6→ 2C2H5OH + 2CO2
C2H5OH + O2 → CH3COOH + H2O
CH3COOH + NaOH → CH3COONa + H2O
CH3COONa + NaOH → CH4 + Na2CO3
2CH4 → C2H2↑ + H2↑
Câu 5. Phát biểu nào sau đây sai:
A. Axit axetic là chất lỏng không màu, vị chua tan vô hạn trong nước.
B. Axit axetic là nguyên liệu để điều chế dược phẩm, phẩm nhuộm, chất dẻo, tơ nhân tạo.
C. Giấm ăn là dung dịch axit axetic có nồng độ từ 5 đến 7%
D. Bằng cách oxi hóa butan với chất xúc tác thích hợp người ta thu được axit axteic.
Lời giải:
Đáp án: C
Câu 6. CTPT của ancol dạng C4H10O có bao nhiêu CTCT khác nhau?
A. 1
B. 2
C. 3
D. 4
Lời giải:
Đáp án: D
Giải thích:
Ancol no, đơn chức, mạch hở.
Công thức thỏa mãn:
(1) CH3-CH2-CH2-CH2-OH
(2) (CH3)2CH-CH2-OH
(3) CH3-CH2-CH(OH)-CH3
(4) (CH3)3C-OH
Câu 7. Để đốt cháy hoàn toàn 0,1 mol ancol có công thức CnH2n+1OH thì cần 10,08 lít khí oxi (đktc). CTPT của ancol là:
A. CH3OH
B. C2H5OH
C. C3H7OH
D. C4H9OH
Lời giải:
Đáp án: C
Giải thích:
nCnH2n+1OH = 0,1 mol
nO2 = 0,45 mol
CnH2n+1OH + 3n/2O2 → nCO2 + (n+1)H2O
1 3n/2
0,1 0,45
Ta có: 0,1.(3n/2) = 0,45.1 => n = 3
=> Công thức phân tử: C3H7OH.
Câu 8. Từ Ancol etylic người ta có thể điều chế được sản phẩm nào sau đây?
A. Axit axetic
B. Cao su tổng hợp
C. Etyl axetat
D. Cả ba đáp án trên đều đúng
Lời giải:
Đáp án: D
Giải thích:
Từ Ancol etylic người ta có thể điều chế được
Axit axetic
Cao su tổng hợp
Etyl axetat
Câu 9. Ancol etylic có lẫn một ít nước, có thể dùng chất nào sau đây để làm khan ancol?
A. CaO
B. H2SO4 đặc
C. CuSO4 khan
D. Cả ba đáp án trên
Lời giải:
Đáp án: B
Giải thích:
Có thể dùng CaO; CuSO4 khan (màu trắng) hoặc P2O5
Câu 10. Ancol etylic có khả năng tan tốt trong nước là do:
A. Ancol etylic tạo được liên kết hidro với nước
B. Ancol etylic uống được
C. Ancol etylic là chất lỏng
D. Ancol etylic chứa cacbon và hidro
Lời giải:
Đáp án: A
Giải thích:
Ancol etylic có khả năng tan tốt trong nước là do:
Ancol etylic tạo được liên kết hidro với nước
Câu 11. Đốt cháy hoàn toàn m gam rượu no, đơn chức, mạch hở, sau phản ứng thu được 26,4 gam CO2 và 16,2 gam nước. Công thức của rượu no, đơn chức là
A. C3H7OH.
B. C4H8OH.
C. C2H5OH.
D. CH3OH.
Lời giải:
Đáp án: C
Giải thích:
nCO2 = 26,4: 44 = 0,6 (mol)
nH2O = 16,2 : 18 = 0,9 (mol)
Đặt công thức của rượu no, đơn chức, mạch hở là: CnH2n+1OH
CnH2n+1OH → nCO2 + (n+1)H2O
Ta có: nCnH2n+1OH = nH2O - nCO2 = 0,9 - 0,6 = 0,3 (mol)
=> n = nCO2/nrượu = 0,6/0,3 = 2
=> Công thức của rượu là: C2H5OH
9. Một số phương trình phản ứng hoá học khác của Carbon (C) và hợp chất:
C2H5OH + Na → C2H5ONa + H2

