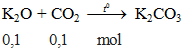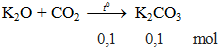Chúng tôi xin giới thiệu phương trình K2O + CO2 -to→ K2CO3 gồm điều kiện phản ứng, cách thực hiện, hiện tượng phản ứng và một số bài tập liên quan giúp các em củng cố toàn bộ kiến thức và rèn luyện kĩ năng làm bài tập về phương trình phản ứng hóa học của Kali. Mời các bạn đón xem:
Phương trình K2O + CO2 -to→ K2CO3
1. Phương trình phản ứng hóa học:
K2O + CO2 -to→ K2CO3
2. Hiện tượng nhận biết phản ứng
- K2O ban đầu có màu vàng nhạt, kết thúc phản ứng thu được chất rắn có màu trắng.
3. Điều kiện phản ứng
- Phản ứng xảy ra nhanh khi nung nóng.
4. Tính chất hóa học
- Tác dụng với nước
K2O + H2O → 2KOH
- Tác dụng với axit
K2O + 2HCl → 2KCl + H2O
- Tác dụng với oxit axit
K2O + CO2 → K2CO3
5. Cách thực hiện phản ứng
- Nung K2O dưới nhiệt độ cao trong luồng khí CO2.
6. Bạn có biết
- K2O có thể phản ứng với các oxit axit khác tạo thành muối, tương tự như phản ứng với CO2.
7. Bài tập liên quan
Ví dụ 1: Thể tích CO2 ở dktc cần dùng để phản ứng hoàn toàn với 0,1 mol K2O tạo muối cacbonat là
A. 1,12 lít.
B. 2,24 lít.
C. 3,36 lít.
D. 4,48 lít.
Hướng dẫn giải
V = 0,1.22,4 = 2,24 lít.
Đáp án B.
Ví dụ 2: Chất nào sau đây không tác dụng với CO2?
A. Na2O.
B. K2O.
C. Li2O.
D. SO2.
Hướng dẫn giải
SO2 không tác dụng với CO2.
Đáp án D.
Ví dụ 3: Cho 2,24 lít khí CO2 ở đktc phản ứng hoàn toàn với K2O tạo muối cabonat. Khối lượng muối thu được sau phản ứng là
A. 5,6 gam.
B. 13,8 gam.
C. 6,5 gam.
D. 8,3 gam.
Hướng dẫn giải
m = 0,1.138= 13,8 gam.
Đáp án B.
8. Một số phương trình phản ứng hóa học khác của Kali và hợp chất: