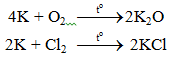Chúng tôi xin giới thiệu phương trình 2K + CuSO4 + 2H2O→ K2SO4 + H2 + Cu(OH)2 gồm điều kiện phản ứng, cách thực hiện, hiện tượng phản ứng và một số bài tập liên quan giúp các em củng cố toàn bộ kiến thức và rèn luyện kĩ năng làm bài tập về phương trình phản ứng hóa học của Kali. Mời các bạn đón xem:
Phương trình 2K + CuSO4 + 2H2O→ K2SO4 + H2 + Cu(OH)2
1. Phương trình phản ứng hóa học:
2K + CuSO4 + 2H2O → K2SO4 + H2 + Cu(OH)2
2. Hiện tượng nhận biết phản ứng
Kali tan dần trong dung dịch muối đồng sunfat, có kết tủa màu xanh tạo thành và có khí thoát ra.
3. Điều kiện phản ứng
- Không cần điều kiện.
4. Tính chất hóa học
- Kali là kim loại kiềm có tính khử rất mạnh.
K → K+ + 1e
a. Tác dụng với phi kim
b. Tác dụng với axit
2K + 2HCl → 2KCl + H2.
c. Tác dụng với nước
- K tác dụng mãnh liệt với nước và tự bùng cháy tạo thành dung dịch kiềm và giải phóng khí hidro.
2K + 2H2O → 2KOH + H2.
d. Tác dụng với hidro
- Kali tác dụng với hidro ở áp suất khá lớn và nhiệt độ khoảng 350 – 400oC tạo thành kali hidrua.
2K (lỏng) + H2 (khí) → 2KH (rắn)
5. Cách thực hiện phản ứng
- Cho kali tác dụng với dung dịch muối đồng sunfat.
6. Bạn có biết
K tham gia phản ứng với các dung dịch muối sẽ tham gia phản ứng với nước trước tạo hidroxit.
7. Bài tập liên quan
Ví dụ 1: Khi cho kim loại K vào dung dịch CuSO4 thì sẽ không xảy ra hiện tượng
A. xuất hiện kết tủa xanh.
B. kết tủa tan dần.
C. có sủi bọt khí.
D. dd trong suốt.
Đáp án B
Ví dụ 2: Sản phẩm thu được khi cho K tác dụng với dung dịch muối đồng sunfat là:
A. K2SO4, Cu
B. K2SO4, H2
C. K2SO4, H2, Cu(OH)2
D. K2SO4, Cu, H2
Đáp án C
Ví dụ 3: Cho kim loại 3,9 g K tác dụng với dung dịch CuSO4 thu được m g kết tủa. Giá trị của m là:
A. 9,8 g
B. 4,9 g
C. 2,45 g
D. 0,49 g
Đáp án D
Hướng dẫn giải:
Phương trình phản ứng: 2K + CuSO4 + 2H2O → K2SO4 + H2 + Cu(OH)2
nCu(OH)2 = nK/2 = 0,1/2 = 0,05 mol ⇒ mCu(OH)2 = 0,05.98 = 0,49 g
8. Một số phương trình phản ứng hóa học khác của Kali và hợp chất:
2K + FeSO4 + 2H2O → K2SO4 + H2 + Fe(OH)2
6K + Al2(SO4)3 + 6H2O → 3K2SO4 + 3H2 + 2Al(OH)3
2K + ZnSO4 + 2H2O → K2SO4 + H2 + Zn(OH)2
2K + PbSO4 + 2H2O → K2SO4 + H2 + Pb(OH)2
6K + Fe2(SO4)3 + 6H2O → 3K2SO4 + 3H2 + 2Fe(OH)3