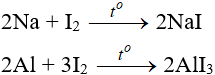Chúng tôi xin giới thiệu phương trình Mn + I2 → MnI2 gồm điều kiện phản ứng, cách thực hiện, hiện tượng phản ứng và một số bài tập liên quan giúp các em củng cố toàn bộ kiến thức và rèn luyện kĩ năng làm bài tập về phương trình phản ứng hóa học của Mangan. Mời các bạn đón xem:
Phương trình Mn + I2 → MnI2
1. Phương trình phản ứng hóa học:
Mn + I2 → MnI2
2. Hiện tượng nhận biết phản ứng
Xuất hiện chất rắn kết tinh màu hồng
3. Điều kiện phản ứng
Nhiệt độ < 200°C
4. Tính chất hoá học
a. Tính chất hoá học của Mangan
- Trạng thái ôxi hóa phổ biến của nó là +2, +3, +4, +6 và +7. Trạng thái ôxy hóa ổn định nhất là mangan +2.
- Mangan có tính khử khá mạnh
Tác dụng với phi kim
- Tác dụng trực tiếp được với nhiều phi kim.
Mn (bột) + O2→ MnO2. (tự bốc cháy)
Mn + Cl2 → MnCl2.
Tác dụng với axit
- Tác dụng với HCl và H2SO4 loãng:
Mn (bột) + 2HCl (loãng) → MnCl2 + H2
- Tác dụng với HNO3 và H2SO4 đặc:
Mn + 2H2SO4 (đặc) → MnSO4 + SO2 + 2H2O.
3Mn + 8HNO3 (loãng, nóng) → 3Mn(NO3)2 + 2NO + 4H2O.
Tác dụng với nước
Mn (bột) + 2H2O (hơi) → Mn(OH)2 + H2
b. Tính chất hoá học của I2
Tác dụng với kim loại
- Iot oxi hóa được nhiều kim loại nhưng chỉ xảy ra khi đun nóng hoặc có xúc tác.
Tác dụng với hidro
H2 + I2 → 2HI phản ứng xảy ra thuận nghịch.
- Hidro Iotua dễ tan trong nước tạo thành dd axit Iothidric, đó là 1 axit rất mạnh, mạnh hơn cả axit clohidric, bromhidric.
- Iot hầu như không tác dụng với H2O.
Iot có tính oxi hóa kém clo và brom:
Cl2 + 2NaI → 2NaCl + I2
Br2 + 2NaI → 2NaBr + I2
Tính khử của axit HI
- HI có tính khử mạnh có thể khử được axit H2SO4 đặc.
8HI + H2SO4 → 4I2 + H2S + 4H2O
2HI + 2FeCl3 → FeCl2 + I2 + 2HCl
Tính chất đặc trưng của Iot
- Iot có tính chất đặc trưng là tác dụng với hồ tinh bột tạo thành hợp chất có màu xanh.
5. Cách thực hiện phản ứng
Cho mangan tác dụng với iot
6. Bạn có biết
Mangan dễ dàng tham gia phản ứng với các chất có tính oxi hóa như Cl2 ; I2…
7. Bài tập liên quan
Ví dụ 1: Điều kiện để phản ứng xảy ra khi cho Mn tác dụng với iot là
A. nhiệt độ
B. xúc tác
C. áp suất
D. Cả A, B, C
Hướng dẫn giải:
Đáp án A
Ví dụ 2: Cho phản ứng : Mn + I2 → MnI2 . Trong phản ứng trên Mangan đóng vai trò là :
A. chất oxi hóa
B. chất khử
C. môi trường
D. Cả A, B, C
Hướng dẫn giải:
Đáp án B
Ví dụ 3: Cho 5,5 g Mn tác dụng vừa hết với m g iot phản ứng xảy ra hoàn toàn. Giá trị của m là:
A. 1,27g
B. 12,7 g
C. 2,54 g
D. 25,4 g
Hướng dẫn giải:
Đáp án D
Phương trình phản ứng: Mn + I2 → MnI2
nI2 = nMn = 5,5/55 = 0,1 mol → mI2 = 0,1 . 254 = 25,4 g
8. Một số phương trình phản ứng hoá học khác của Mangan (Mn) và hợp chất: