Chúng tôi giới thiệu Giải bài tập Hóa học lớp 12 Bài 1: Este chính xác, chi tiết nhất giúp học sinh dễ dàng làm bài tập Este lớp 12.
Bài giảng Hóa học 12 Bài 1: Este
Giải bài tập Hóa học 12 Bài 1: Este
Câu hỏi và bài tập (trang 7 sgk Hóa học lớp 12)
a) Este là sản phẩm của phản ứng giữa axit và ancol.
b) Este là hợp chất hữu cơ trong phân tử có nhóm COO-
c) Este no, đơn chức, mạch hở có công thức phân tử CnH2nO2, với n ≥ 2.
d) Hợp chất CH3COOC2H5 thuộc loại este.
e) Sản phẩm của phản ứng giữa axit và ancol là este.
Lời giải:a) S. Ví dụ phản ứng giữa axit vô cơ và ancol không phải là este
B) S. Vì phân tử este không có anion COO-
c) Đ
d) Đ
e) S. Ví dụ phản ứng giữa axit vô cơ và ancol không phải là este
A. 2 B. 3
C. 4 D. 5
Các đồng phân của C4H8O2 là:
CH3CH2COOCH3: metyl propionat
CH3COOCH2CH3: etyl axetat
HCOOCH2CH2CH3: propyl fomat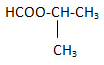 : isopropyl fomat
: isopropyl fomat
Đáp án C
A. HCOOC3H7. B. C2H5COOCH3.
C. CH3COOC2H5. D. HCOOC3H5.
- Từ CTCT của X => X là este no đơn chức, mạch hở
- Viết CTCT của Y => CTCT của X
X có công thức cấu tạo C4H8O2 nên X là este no, đơn chức, mạch hở
Y có CTCT là CH3COONa
Vậy X là CH3COOC2H5
Đáp án C
A. etyl axetat. B. metyl axetat.
C. metyl propionate D. propyl fomat.
- Từ CTPT của X => X là este no, đơn chức, mạch hở
- Viết PTHH
- Từ tỉ khối của Z => MZ => Z => X
RCOOR' + NaOH RCOONa + R'OH
- Vì Z có tỉ khối hơi so với H2 nên suy ra Z có thể ở dạng hơi. Do đó, Z là rượu.
CTPT của este X có dạng CnH2nO2 nên X là este no đơn chức mạch hở. Do đó, Z là rượu no đơn chức. Gọi CTPT của Z là CmH2m+2O
Ta có:
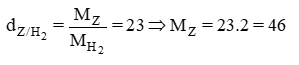
= 14m + 18 = 46 ⇒ m = 2
Do đó: Z:
Đáp án A
- Phản ứng thủy phân este trong môi trường axit là phản ứng thuận nghịch, este vẫn còn, nổi lên trên bề mặt dung dịch.
![]()
- Phản ứng thủy phân este trong môi trường kiềm là phản ứng một chiều, este phản ứng hết.Phản ứng này còn được gọi là phản ứng xà phòng hóa.
a) Xác định công thức phân tử của X.
b) Đun 7,4 gam X trong dung dịch NaOH vừa đủ đến khi phản ứng hoàn toàn thu được 3,2 gam ancol Y và một lượng muối Z. Viết công thức cấu tạo của X và tính khối lượng của Z.
Phương pháp giải:
- Từ số mol của CO2 và nước este no, đơn chức mạch hở Công thức tổng quát của este
- Có neste = CTPT của este CTCT của este Tên của este
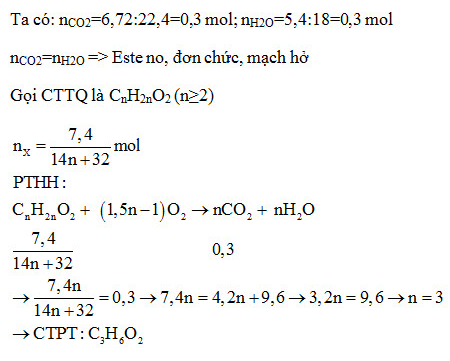
Do este là este đơn chức nên ta có nX = nY = 0,1 mol.
MY = 3,2/0,1 = 32g/mol => CTPT của Y : CH3OH
CTCT của X : CH3COOCH3
CH3COOCH3 + NaOH -> CH3COONa + CH3OH
0,1 0,1
mZ = 0,1.82 = 8,2g
Lý thuyết Bài 1: Este
I. KHÁI NIỆM:
VD: CH3COOH + C2H5OH CH3COOC2H5 + H2O
=> ĐN: Khi ta thay thế nhóm (-OH) trong phân tử axit bằng gốc (-OR') thì thu được este
RCOOH → R - COOR' (R' ≠ H)
Chú ý: Cách viết khác của este
R - COO - R' hoặc R' - OOC - R hoặc R' - OCO - R (R'≠ H)
R là gốc xuất phát từ axit, còn R' là gốc xuất phát từ ancol
II. PHÂN LOẠI
1. Este no, đơn chức:CnH2nO2 (n ≥ 2)
2. Este không no đơn chức:
- Este đơn chức, mạch hở, không no : CmH2m+2-2kO2 (k là số liên kết pi, k ≥ 2)
VD: Este đơn chức, mạch hở, không no và có chứa 1 liên kết đôi: CmH2m-2O2
3. Este đa chức:
- Este tạo bởi axit đơn chức và rượu đa chức có dạng: (RCOO)mR’
- Este tạo bởi rượu đơn chức và axit đa chức có dạng: R (COOR’)m
- Este tạo bời axit đa chức R(COOH)n và ancol đa chức R’(OH)m có dạng: Rm(COO)nmR’n
III. DANH PHÁP
Tên este = Tên gốc hidrocacbon R’ + tên anion gốc axit (thay đuôi ic bằng đuôi at)
- Tên một số gốc axit thường gặp:
HCOO-: Fomat CH3COO-: Axetat
CH2=CHCOO-: Acrylat C6H5COO-: Benzoat
- Tên một số gốc R’ thường gặp:
CH3-: metyl; C6H5- : phenyl
C2H5-: etyl; C6H5CH2- : benzyl
CH2=CH-: Vinyl
Ví dụ: CH3COOC6H5 : phenyl axetat
IV. TÍNH CHẤT VẬT LÍ
- Là chất lỏng hoặc chất rắn ở điều kiện thường, ít tan trong nước
- Có nhiệt độ sôi thấp hơn nhiều so với các axit có cùng khối lượng mol hoặc các phân tử có cùng số C, do trong este không có liên kết hidro
- Các este thường có mùi đặc trưng
Isoamyl axetat (CH3COOCH2CH2(CH3)2): mùi thơm của chuối.
Etyl isovalerat ((CH3)2CHCH2COOC2H5): mùi táo.
Etyl butirat (CH3CH2CH2COOC4H9): mùi dứa.
Geranyl axetat (CH3COOC10H17): mùi hoa hồng …
Benzyl propionat: CH3CH2COO-CH2C6H5: mùi hoa nhài.
V. TÍNH CHẤT HÓA HỌC
1. Phản ứng ở nhóm chức
a) Phản ứng thủy phân.
+ Trong môi trường axit :
RCOOR’ + H2O 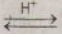 RCOOH + R’OH.
RCOOH + R’OH.
+ Trong môi trường bazơ : Phản ứng xà phòng hóa.
RCOOR' +NaOH RCOONa + R'OH.
* Một số phản ứng thủy phân đặc biệt của este:
- Este của phenol tham gia phản ứng xà phòng hóa sinh ra 2 muối: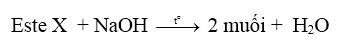
- Một số este có dạng đặc biệt thủy phân sinh ra andehit, xeton
RCOOCH=CH-R’ + NaOH → RCOONa + R’CH2-CHO + H2O
RCOOC(R’)=R’’ + NaOH → RCOONa + R’-CO-R’’ + H2O
- Este - axit, có công thức là HOOC–R–COOR’
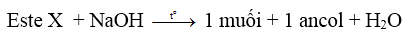
- Este vòng (được tạo bởi hiđroxi axit)
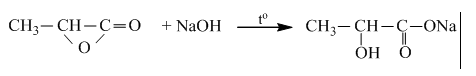
b) Phản ứng khử
Este bị khử bởi liti nhôm hiđrua (LiAlH4), khi đó nhóm RCO– (gọi là nhóm axyl) trở thành ancol bậc I: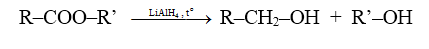
2. Phản ứng ở gốc hidrocacbon
Dựa vào đặc điểm của gốc hidrocacbon, este có thể tham gia được phản ứng thế, cộng, trùng hợp, …..
a) Phản ứng cộng vào gốc không no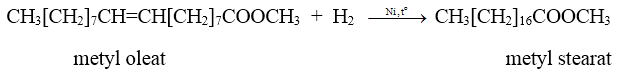
b) Phản ứng trùng hợp
Một số este đơn giản có liên kết C = C tham gia phản ứng trùng hợp giống như anken.
VI. ĐIỀU CHẾ
- Thường được điều chế bằng phản ứng este hóa
RCOOH + R’OH 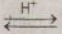 RCOOR’ + H2O
RCOOR’ + H2O
- Một số este có phương pháp điều chế riêng, ví dụ như vinyl axetat được điều chế qua phản ứng sau:
VII. ỨNG DỤNG
Được dùng làm dung môi để tách, chiết, sản xuất chất dẻo, làm hương liệu trong công nghiệp thực phẩm, mĩ phẩm...
VIII. NHẬN BIẾT ESTE
- Este của axit fomic có khả năng tráng gương.
- Các este của ancol không bền bị thủy phân tạo anđehit có khả năng tráng gương.
I. KHÁI NIỆM:
VD: CH3COOH + C2H5OH CH3COOC2H5 + H2O
=> ĐN: Khi ta thay thế nhóm (-OH) trong phân tử axit bằng gốc (-OR') thì thu được este
RCOOH → R - COOR' (R' ≠ H)
Chú ý: Cách viết khác của este
R - COO - R' hoặc R' - OOC - R hoặc R' - OCO - R (R'≠ H)
R là gốc xuất phát từ axit, còn R' là gốc xuất phát từ ancol
II. PHÂN LOẠI
1. Este no, đơn chức:CnH2nO2 (n ≥ 2)
2. Este không no đơn chức:
- Este đơn chức, mạch hở, không no : CmH2m+2-2kO2 (k là số liên kết pi, k ≥ 2)
VD: Este đơn chức, mạch hở, không no và có chứa 1 liên kết đôi: CmH2m-2O2
3. Este đa chức:
- Este tạo bởi axit đơn chức và rượu đa chức có dạng: (RCOO)mR’
- Este tạo bởi rượu đơn chức và axit đa chức có dạng: R (COOR’)m
- Este tạo bời axit đa chức R(COOH)n và ancol đa chức R’(OH)m có dạng: Rm(COO)nmR’n
III. DANH PHÁP
Tên este = Tên gốc hidrocacbon R’ + tên anion gốc axit (thay đuôi ic bằng đuôi at)
- Tên một số gốc axit thường gặp:
HCOO-: Fomat CH3COO-: Axetat
CH2=CHCOO-: Acrylat C6H5COO-: Benzoat
- Tên một số gốc R’ thường gặp:
CH3-: metyl; C6H5- : phenyl
C2H5-: etyl; C6H5CH2- : benzyl
CH2=CH-: Vinyl
Ví dụ: CH3COOC6H5 : phenyl axetat
IV. TÍNH CHẤT VẬT LÍ
- Là chất lỏng hoặc chất rắn ở điều kiện thường, ít tan trong nước
- Có nhiệt độ sôi thấp hơn nhiều so với các axit có cùng khối lượng mol hoặc các phân tử có cùng số C, do trong este không có liên kết hidro
- Các este thường có mùi đặc trưng
Isoamyl axetat (CH3COOCH2CH2(CH3)2): mùi thơm của chuối.
Etyl isovalerat ((CH3)2CHCH2COOC2H5): mùi táo.
Etyl butirat (CH3CH2CH2COOC4H9): mùi dứa.
Geranyl axetat (CH3COOC10H17): mùi hoa hồng …
Benzyl propionat: CH3CH2COO-CH2C6H5: mùi hoa nhài.
V. TÍNH CHẤT HÓA HỌC
1. Phản ứng ở nhóm chức
a) Phản ứng thủy phân.
+ Trong môi trường axit :
RCOOR’ + H2O ![]() RCOOH + R’OH.
RCOOH + R’OH.
+ Trong môi trường bazơ : Phản ứng xà phòng hóa.
RCOOR' +NaOH RCOONa + R'OH.
* Một số phản ứng thủy phân đặc biệt của este:
- Este của phenol tham gia phản ứng xà phòng hóa sinh ra 2 muối: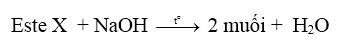
- Một số este có dạng đặc biệt thủy phân sinh ra andehit, xeton
RCOOCH=CH-R’ + NaOH → RCOONa + R’CH2-CHO + H2O
RCOOC(R’)=R’’ + NaOH → RCOONa + R’-CO-R’’ + H2O
- Este - axit, có công thức là HOOC–R–COOR’
![]()
- Este vòng (được tạo bởi hiđroxi axit)
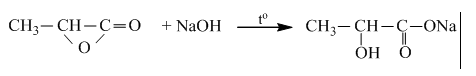
b) Phản ứng khử
Este bị khử bởi liti nhôm hiđrua (LiAlH4), khi đó nhóm RCO– (gọi là nhóm axyl) trở thành ancol bậc I:![]()
2. Phản ứng ở gốc hidrocacbon
Dựa vào đặc điểm của gốc hidrocacbon, este có thể tham gia được phản ứng thế, cộng, trùng hợp, …..
a) Phản ứng cộng vào gốc không no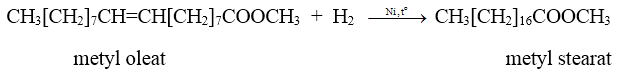
b) Phản ứng trùng hợp
Một số este đơn giản có liên kết C = C tham gia phản ứng trùng hợp giống như anken.
VI. ĐIỀU CHẾ
- Thường được điều chế bằng phản ứng este hóa
RCOOH + R’OH ![]() RCOOR’ + H2O
RCOOR’ + H2O
- Một số este có phương pháp điều chế riêng, ví dụ như vinyl axetat được điều chế qua phản ứng sau:
VII. ỨNG DỤNG
Được dùng làm dung môi để tách, chiết, sản xuất chất dẻo, làm hương liệu trong công nghiệp thực phẩm, mĩ phẩm...
VIII. NHẬN BIẾT ESTE
- Este của axit fomic có khả năng tráng gương.
- Các este của ancol không bền bị thủy phân tạo anđehit có khả năng tráng gương.
Phương pháp giải một số bài tập
* Một số lưu ý cần nhớ:
- Cách đọc tên este có dạng RCOOR’
=> Tên R’ + Tên gốc axit (đổi đuôi ic thành đuôi at)
* Lưu ý: nhớ một số gốc R, R’ thường gặp (xem lại phần lý thuyết)
Este có công thức R’OOCR trùng với công thức R’OCOR là este được tạo bởi axit RCOOH và ancol R’OH.
* Một số ví dụ điển hình:
Ví dụ 1: Có các nhận định sau : (1) Este là sản phẩm của phản ứng giữa axit cacboxylic và ancol ; (2) Este là hợp chất hữu cơ trong phân tử có nhóm -COO- ; (3) Este no, đơn chức, mạch hở có công thức phân tử CnH2nO2, với n ≥ 2 ; (4) Hợp chất CH3COOC2H5 thuộc loại este. Các nhận định đúng là :
A. (1), (2), (3), (4).
B. (1), (3), (4).
C. (1), (2), (4).
D. (2), (3), (4).
Hướng dẫn giải chi tiết:
(1) đúng (định nghĩa về este)
(2) sai, không phải chỉ có este mới có nhóm –COO-, axit cacboxylic cũng có nhóm này
(3) đúng
(4) đúng
Đáp án B
Ví dụ 2: Este no, đơn chức, mạch hở có công thức tổng quát là :
A. CnH2nO2 (n ≥ 2).
B. CnH2n - 2O2 (n2).
C. CnH2n + 2O2 (n2).
D. CnH2nO (n2).
Hướng dẫn giải chi tiết:
Este no, đơn chức mạch hở có công thức tổng quát là: CnH2nO2 (n ≥ 2)
Đáp án A
Ví dụ 3: Este vinyl axetat có công thức là :
A. CH3COOCH=CH2.
B. CH3COOCH3.
C. CH2=CHCOOCH3.
D. HCOOCH3.
Hướng dẫn giải chi tiết:
Este vinyl axetat có công thức phân tử là: CH3COOCH=CH2.
Đáp án A.
Ví dụ 4: : Đun nóng este CH2=CHCOOCH3 với một lượng vừa đủ dung dịch NaOH, sản phẩm thu được là :
A. CH2=CHCOONa và CH3OH.
B. CH3COONa và CH3CHO.
C. CH3COONa và CH2=CHOH.
D. C2H5COONa và CH3OH.
Hướng dẫn giải chi tiết:
Ta có phương trình:
CH2=CHCOOCH3 + NaOH → CH2=CHCOONa + CH3OH.
Đáp án A
Ví dụ 5: Phát biểu nào sau đây không đúng ?
A. Phản ứng este hoá xảy ra hoàn toàn.
B. Khi thuỷ phân este no, mạch hở trong môi trường axit sẽ cho axit và ancol.
C. Phản ứng giữa axit và ancol là phản ứng thuận nghịch.
D. Khi thuỷ phân este no mạch hở trong môi trường kiềm sẽ cho muối và ancol.
Hướng dẫn giải chi tiết:
Phản ứng este hóa xảy ra thuận nghịch, không hoàn toàn.
Đáp án A
Dạng 2: Phản ứng thủy phân este
* Một số lưu ý cần nhớ:
Este đơn chức
- Este tạo bởi axit và ancol thủy phân (môi trường axit hoặc kiềm) sẽ sinh ra ancol tương ứng:
RCOOR’ + NaOH → RCOONa + R’OH
CH3COOC2H5 + NaOH → CH3COONa + C2H5OH
- Este tạo bởi axit và akin thủy phân sẽ sinh ra andehit hoặc ancol
RCOOCH2=R’ + NaOH → RCOONa + R’CHO
RCOOCH(R’)=R’’ + NaOH → RCOONa + R’-CO-R’’
- Este tạo bởi axit và phenol khi thủy phân trong môi trường kiềm sẽ sinh ra muối phenolat và nước
RCOOC6H5 + 2NaOH → RCOONa + C6H5ONa + H2O.
* Este đa chức
Một số phản ứng của este đa chức:
R(COOR’)n + nH2O R(COOH)n + nR’OH
R(OOCR’)n + nNaOH → nR’COONa + R(OH)n
* Một số ví dụ điển hình:
Ví dụ 1: Muốn thuỷ phân 5,6 gam hỗn hợp etyl axetat và etyl fomiat (etyl fomat) cần 25,96 ml NaOH 10%, (D = 1,08 g/ml). Thành phần % khối lượng của etyl axetat trong hỗn hợp là :
A. 47,14%.
B. 52,16%.
C. 36,18%.
D. 50,20%.
Hướng dẫn giải chi tiết:
Gọi số mol của CH3COOC2H5, HCOOC2H5 lần lượt là x, y.
Ta có phương trình phản ứng:
CH3COOCH2H5 + NaOH → CH3COONa + C2H5OH (1)
x x (mol)
HCOOC2H5 + NaOH → HCOONa + C2H5OH (2)
y y (mol)
m dd NaOH = V.D = 25,96 . 1,08 = 28 (gam)
m ct NaOH = m dd * C% = 28 * 10% = 2,8 (gam)
n NaOH = 2,8 : 40 = 0,07 (mol)
Từ (1), (2) => n NaOH = n este = 0,07 mol
=> x + y = 0,07 (I)
Mặt khác, khối lượng 2 este bằng 5,36 gam
=> 88x + 74y = 5,6 (II)
Từ (I) và (II)
=> x = 0,03 ; y = 0,04
%m CH3COOC2H5 = 47,14%.
Đáp án A
Ví dụ 2: Cho 13,6 gam phenyl axetat tác dụng với 200 ml dung dịch NaOH 1,5M đun nóng. Sau khi phản ứng xảy ra hoàn toàn thu được dung dịch X. Cô cạn X thu được a gam chất rắn khan. Giá trị của a là :
A. 12,2 gam.
B. 16,2 gam.
C. 19,8 gam.
D. 23,8 gam.
Hướng dẫn giải chi tiết:
Ta có phương trình hóa học:
CH3COOC6H5 + 2NaOH → CH3COONa + C6H5ONa + H2O (1)
n CH3COOC6H5 = m : M = 13,6 : 136 = 0,1 (mol)
n NaOH = 0,2 . 1,5 = 0,3 (mol)
Từ (1) => n NaOH dư sau phản ứng, tính theo este
(1) n NaOH phản ứng = 2 n este = 0,2 mol
=> n NaOH dư = 0,3 – 0,2 = 0,1 mol
n CH3COONa = n C6H5ONa = n este = 0,1 mol
=> Khối lượng chất rắn khan bằng:
m NaOH dư + m CH3COONa + m C6H5ONa
= 0,1 * 40 + 0,1 * 82 + 0,1 * 116 = 23,8 gam
Đáp án D
Ví dụ 3: Xà phòng hoá hoàn toàn 17,6 gam hỗn hợp 2 este là etyl axetat và metyl propionatbằng lượng vừa đủ V (ml) dung dịch NaOH 0,5M. Giá trị V đã dùng là :
A. 400 ml.
B. 500 ml.
C. 200 ml.
D. 600 ml.
Hướng dẫn giải chi tiết:
2 Este trên có CTCT là: CH3COOC2H5, C2H5COOCH3 đều có CTPT là C4H8O2.
n C4H8O2 = m : M = 17,6 : 88 = 0,2 (mol)
n NaOH = n este = 0,2 mol
=> V NaOH = n : CM = 0,2 : 0,5 = 0,4 lít = 400 ml
Đáp án A.
Dạng 3: Bài toán về phản ứng đốt cháy este
* Một số lưu ý cần nhớ:
Este no, đơn chức mạch hở có dạng CnH2nO2
Ta có phương trình đốt cháy:
CnH2nO2 + (3n-2)/2 O2 → nCO2 + nH2O
=> n H2O = n CO2
=> n este = 1,5 n CO2 – n O2
* Một số ví dụ điển hình:
Ví dụ 1: Đốt cháy hoàn toàn 7,4 gam este X đơn chức thu được 6,72 lít khí CO2 (đktc) và 5,4 gam nước. Xác định công thức phân tử của X.
Hướng dẫn giải chi tiết:
n CO2 = 6,72 : 22,4 = 0,3 mol
n H2O = 5,4 : 18 = 0,3 mol
n CO2 = n H2O => X là este no, đơn chức mạch hở.
Gọi CTPT của X là CnH2nO2
Ta có phương trình: CnH2nO2 + (3n-2)/2 O2 → nCO2 + nH2O
=> n este = (0,3 : n) * n CO2 = 0,09 : n (mol)
=> Khối lượng mol của X là: 7,4 : (0,3 : n) = 74/3 n
=> 14n + 32 = 74/3 n => n = 3
=> CTPT của X là: C3H6O2
Ví dụ 2: Đốt cháy hoàn toàn m gam hỗn hợp các este no, đơn chức, mạch hở. Sản phẩm cháy được dẫn vào bình đựng dung dịch nước vôi trong dư thấy khối lượng bình tăng 6,2 gam. Số mol H2O sinh ra và khối lượng kết tủa tạo ra là :
A. 0,1 mol ; 12 gam.
B. 0,1 mol ; 10 gam.
C. 0,01 mol ; 10 gam.
D. 0,01 mol ; 1,2 gam.
Hướng dẫn giải chi tiết:
Hỗn hợp trên là các este no, đơn chức mạch hở.
=> Khi đốt cháy sẽ thu được n CO2 = n H2O
Gọi n CO2 = n H2O = a (mol)
Khi sục hỗn hợp khí và hơi trên vào dung dịch Ca(OH)2 thì khối lượng bình tăng lên 6,2 gam
=> m CO2 + m H2O = 6,2
=> 44a + 18a = 6,2 => a = 0,1 mol
=> n H2O = 0,1 mol
Ta có phương trình hóa học:
CO2 + Ca(OH)2 → CaCO3 + H2O
=> n CaCO3 = n CO2 = 0,1 mol
=> m CaCO3 = 0,1 * 100 = 10 gam
Đáp án B
Dạng 4: Bài toán về điều chế este (phản ứng este hóa)
* Một số lưu ý cần nhớ:
ROH + R’COOH RCOOR’ + H2O
R(OH)n + nR’COOH R(OOCR’)n + nH2O
R(COOH)n + nR’OH R(COOR’)n + nH2O
=> Đây là phản ứng thuận nghịch nên hiệu suất luôn nhỏ hơn 100%
* Một số ví dụ điển hình
Ví dụ 1: Thực hiện phản ứng este hóa m gam CH3COOH bằng một lượng vừa đủ C2H5OH thu được 0,02 mol este. Hiệu suất phản ứng H = 60%. Gía trị của m ?
Hướng dẫn giải chi tiết:
Ta có phương trình hóa học:
CH3COOH + C2H5OH CH3COOC2H5 + H2O
0,02 → 0,02
Theo lý thuyết khối lượng CH3COOH cần dùng là : 60 * 0,02 = 1,2 gam
Mặt khác H = 60%
=> Khối lượng axit đã dùng là:
m = (1,2 . 100) : 60 = 2 gam
Ví dụ 2: Đun nóng 6,0 gam CH3COOH với 6,0 gam C2H5OH ( có H2SO4 làm xúc tác, hiệu suất phản ứng este hoá bằng 50%). Khối lượng este tạo thành là:
A.6,0 gam B.4,4 gam
C.8,8 gam D.5,2 gam.
Hướng dẫn giải chi tiết
Ta có phương trình hóa học:
CH3COOH + C2H5OH CH3COOC2H5 + H2O
n CH3COOH = 6 : 60 = 0,1 mol
n C2H5OH = 6 : 46 = 0,13 (mol)
=> Sau phản ứng, C2H5OH dư, bài toán tính theo CH3COOH
(1) n CH3COOC2H5 = n CH3COOH = 0,1 mol
Mặt khác, hiệu suất của quá trình này là 60%
=> Số mol este thực tế thu được là: 0,1 * 50% = 0,05 mol
=> m este = 0,05 * 88 = 4,4 gam
Đáp án B.
Ví dụ 3: Hỗn hợp X gồm axit HCOOH và CH3COOH (tỉ lệ mol 1:1). Hỗn hợp Y gồm hai ancol CH3OH và C2H5OH (tỉ lệ mol 3 : 2). Lấy 11,13 gam hỗn hợp X tác dụng với 7,52 gam hỗn hợp Y (có xúc tác H2SO4 đặc) thu được m gam hỗn hợp este (hiệu suất các phản ứng đều bằng 80%). Giá trị m là :
A. 11,616.
B. 12,197.
C. 14,52.
D. 15,246.
* Hướng dẫn giải chi tiết:
Đặt công thức trung bình của hai axit trong X là .
=>
Đặt công thức trung bình của hai ancol trong Y là
=>
Do đó axit dư, hiệu suất phản ứng tính theo ancol.
+ + H2O
mol: 0,2.80% ↔ 0,2.80% ↔ 0,2.80%
Vậy khối lượng este thu được là :
[(53+37,6) – 18].0,2.80% = 11,616 gam.
Đáp án A.

