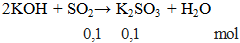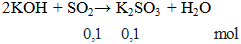Chúng tôi xin giới thiệu phương trình 2KOH + SO2 → K2SO3 + H2O gồm điều kiện phản ứng, cách thực hiện, hiện tượng phản ứng và một số bài tập liên quan giúp các em củng cố toàn bộ kiến thức và rèn luyện kĩ năng làm bài tập về phương trình phản ứng hóa học của Kali. Mời các bạn đón xem:
Phương trình 2KOH + SO2 → K2SO3 + H2O
1. Phương trình phản ứng hóa học:
2KOH + SO2 → K2SO3 + H2O
2. Hiện tượng nhận biết phản ứng
- Quan sát sự chuyển màu của chỉ thị phù hợp trước và sau phản ứng.
3. Điều kiện phản ứng
- Phản ứng xảy ra ngay điều kiện thường.
4. Tính chất hóa học
- KOH là một bazo mạnh có khả năng làm thay đổi màu sắc các chất chỉ thị như khiến quỳ tím chuyển sang màu xanh, còn dung dịch phenolphtalein không màu thành màu hồng.
Ở điều kiện nhiệt độ phòng, KOH tác dụng với oxit axit như SO2, CO2
KOH + SO2 → K2SO3 + H2O
KOH + SO2 → KHSO3
- KOH tác dụng với axit tạo thành muối và nước
KOH(dd) + HCl(dd) → KCl(dd) + H2O
- KOH tác dụng với các axit hữu cơ để tạo thành muối và thủy phân este, peptit
RCOOR1 + KOH → RCOOK + R1OH
- KOH tác dụng với kim loại mạnh tạo thành bazo mới và kim loại mới
KOH + Na → NaOH + K
- KOH tác dụng với muối để tạo thành muối mới và axit mới
2KOH + CuCl2 → 2KCl + Cu(OH)2↓
- KOH là một bazo mạnh, trong nước phân ly hoàn toàn thành ion Na+ và OH-
Phản ứng với một số oxit kim loại mà oxit, hidroxit của chúng lưỡng tính như nhôm, kẽm,…
2KOH + 2Al + 2H2O → 2KAlO2 + 3H2↑
2KOH + Zn → K2ZnO2 + H2↑
- KOH phản ứng với một số hợp chất lưỡng tính
KOH + Al(OH)3 → KAlO2 + 2H2O
2KOH + Al2O3 → 2KAlO2 + H2O
5. Cách thực hiện phản ứng
- Dẫn khí SO2 vào ống nghiệm chứa KOH và vài giọt chất chỉ thị.
6. Bạn có biết
- KOH phản ứng với SO2 tùy theo tỉ lệ về số mol mà sản phẩm thu được có thể là muối cabonat trung hòa hoặc muối axit hoặc hỗn hợp cả hai muối.
- KOH phản ứng với SO2 chỉ thu được muối K2SO3 khi T = 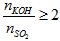
7. Bài tập liên quan
Ví dụ 1: Cho 2,24 lít khí SO2 ở đktc phản ứng với lượng dư dung dịch KOH thu được dung dịch X. Khối lượng muối tan có trong X là
A. 15,8 gam.
B. 13,8 gam.
C. 11,8 gam.
D. 10,8 gam.
Đáp án A.
Hướng dẫn giải
Do KOH dư nên có phản ứng
mmuối = 0,1.158 = 15,8 gam.
Ví dụ 2: Cho SO2 tác dụng với lượng dư dung dịch KOH thu được dung dịch X. Chất tan có trong dung dịch X là
A. K2SO3.
B. K2SO3 và KHSO3.
C. KHSO3.
D. K2SO3 và KOH.
Đáp án D.
Hướng dẫn giải
Do KOH dư nên có phản ứng
2KOH + SO2 → K2SO3 + H2O
Chất tan có trong dung dịch X là K2SO3 và KOH dư.
Ví dụ 3: Cho 2,24 lít khí SO2 ở đktc phản ứng với dung dịch chứa 0,3 mol KOH. Khối lượng muối tan có trong dung dịch sau phản ứng là
A. 15,8 gam.
B. 13,8 gam.
C. 11,8 gam.
D. 10,8 gam.
Đáp án A.
Hướng dẫn giải
Có T = 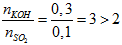
mmuối = 0,1.158 = 15,8 gam.
Ví dụ 4: Hấp thụ 2,24 lít khí SO2 (đktc) vào 200 ml dung dịch KOH aM. Tính a biết sau phản ứng chỉ thu được muối trung hòa.
A. 0,5
B. 0,25
C. 0,1
D. 1
Đáp án A
Hướng dẫn giải
nSO2 = 0,1 mol
Vì đề cho chỉ tạo muối trung hòa nên chỉ xảy ra phản ứng
SO2 + 2KOH → K2SO3 + H2O
0,1 → 0,2
VKOH = 200 ml = 0,2 lít
→ a = CMKOH = 0,1/0,2 = 0,5M
Ví dụ 5: Dẫn V lít (đktc) khí SO2 vào 100 ml dung dịch KOH 1M thu được 6 gam muối KHSO3. Vậy V có giá trị là:
A. 2,24 lit
B. 3,36 lít
C. 4,48 lit
D. 1,68 lit
Đáp án D
Hướng dẫn giải
Các phương trình phản ứng xảy ra:
SO2 + KOH → KHSO3
0,05 → 0,05 → 0,05 mol
SO2 + 2KOH → K2SO3 + H2O
0,025 → 0,05 mol
Tổng số mol SO2 = 0,075 mol
→ V = 1,68 lit
Ví dụ 6: Khi dẫn khí SO2 vào dung dịch KOH dư thì giai đoạn đầu tiên sẽ xảy ra phản ứng gì?
A. SO2 + KOH → KHSO3
B. SO2 + 2KOH → K2SO3 + H2O
C. SO2 + K2SO3 + H2O → 2KHSO3
D. SO2 + H2O → H2SO3
Đáp án B
Ví dụ 7: Nhóm chất tác dụng với nước và với dung dịch HCl là:
A. Na2O, SO3, CO2.
B. K2O, P2O5, CaO
C. BaO, SO3, P2O5
D. CaO, BaO, Na2O
Đáp án D
Hướng dẫn giải
Nhóm chất tác dụng với nước và với dung dịch HCl là: CaO, BaO, Na2O
Phương trình phản ứng minh họa
CaO + H2O → Ca(OH)2
CaO + 2HCl → CaCl2 + H2O
BaO + 2HCl → BaCl2 + H2O
BaO + H2O → Ba(OH)2
Na2O + 2HCl → 2NaCl + H2O
Na2O + H2O → 2NaOH
Ví dụ 8: Cho các chất sau: SO2, CO2, KOH, CaO, CuCl2 số cặp chất tác dụng được với nhau là
A. 2
B. 3
C. 4
D. 5
Đáp án D
Hướng dẫn giải
Phương trình phản ứng minh họa
SO2 + CaO → CaCO3
SO2+ KOH → K2SO3 + H2O
CO2 + CaO → CaCO3
CO2 + KOH → K2CO3 + H2O
CuCl2 + KOH → Cu(OH)2 + KCl
Ví dụ 9: Sục từ từ SO2 đến dư vào dung dịch Ba(OH)2 hiện tượng quan sát thấy được là
A. xuất hiện kết tủa, lượng kết tủa tăng dần, kết tủa không tan
B. không có hiện tượng gì trong suốt quá trình thực hiện phản ứng
C. ban đầu không thấy hiện tượng khi phản ứng, sau đó dân dần kết tủa xuất hiện
D. xuất hiện kết tủa, lượng kết tủa tăng dần, sau đó kết tủa tan ra
Đáp án D
Hướng dẫn giải
Dẫn từ từ SO2 đến dư vào dung dịch Ba(OH)2 xảy ra phản ứng:
Phương trình phản ứng minh họa
SO2 + Ba(OH)2 → BaSO3 + H2O
SO2+ BaSO3 + H2O → Ba(HSO3)2
Dung dịch xuất hiện kết tủa trắng tăng dần đến cực đại, sau đó kết tủa tan dần đến hết.
8. Một số phương trình phản ứng hóa học khác của Kali và hợp chất: