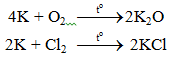Chúng tôi xin giới thiệu phương trình 2K + 2H2O → 2KOH + H2 gồm điều kiện phản ứng, cách thực hiện, hiện tượng phản ứng và một số bài tập liên quan giúp các em củng cố toàn bộ kiến thức và rèn luyện kĩ năng làm bài tập về phương trình phản ứng hóa học của Kali. Mời các bạn đón xem:
Phương trình 2K + 2H2O → 2KOH + H2
1. Phương trình phản ứng hóa học:
2K + 2H2O → 2KOH + H2
2. Hiện tượng nhận biết phản ứng
Mẫu K tan dần cho đến hết, có bọt khí H2 bay ra, phản ứng toả nhiều nhiệt.
3. Điều kiện phản ứng
- Không cần điều kiện
4. Tính chất hóa học
- Kali là kim loại kiềm có tính khử rất mạnh.
K → K+ + 1e
a. Tác dụng với phi kim
b. Tác dụng với axit
2K + 2HCl → 2KCl + H2.
c. Tác dụng với nước
- K tác dụng mãnh liệt với nước và tự bùng cháy tạo thành dung dịch kiềm và giải phóng khí hidro.
2K + 2H2O → 2KOH + H2.
d. Tác dụng với hidro
- Kali tác dụng với hidro ở áp suất khá lớn và nhiệt độ khoảng 350 – 400oC tạo thành kali hidrua.
2K (lỏng) + H2 (khí) → 2KH (rắn)
5. Cách thực hiện phản ứng
- Cho kali tác dụng với nước thu được kalihidroxit
6. Bạn có biết
Với lượng lớn Natri cũng cho phản ứng với nước có thể gây nổ rất nguy hiểm
7. Bài tập liên quan
Ví dụ 1: Cho 3,9 g K tác dụng với H2O thu được V lít khí đktc. Giá trị của V là
A. 1,12 lít
B. 11,2 lít
C. 2,24 lít
D. 5,6 lít
Đáp án A
Hướng dẫn giải:
Phương trình phản ứng: 2K + 2H2O → 2KOH + H2
nH2 = nK/2 = 0,05 mol ⇒ VH2 = 0,05.22,4 = 1,12 lít
Ví dụ 2: Cho dãy các kim loại: Na, Ca, Cu, Fe, K. Số kim loại trong dãy tác dụng với H2O tạo dung dịch bazơ là:
A. 4
B. 3
C. 2
D. 1
Đáp án B
Hướng dẫn giải:
Phương trình phản ứng:
2Na + 2H2O → 2NaOH + H2
2K + 2H2O → 2KOH + H2;
Ca + H2O → Ca(OH)2 + H2.
Ví dụ 3: Khi cho K tác dụng với nước thu được dung dịch A. Nhúng quỳ tím vào dung dịch A, quỳ tím chuyển sang màu
A. màu xanh
B. màu hồng
C. không màu
D. màu tím.
Đáp án A
Hướng dẫn giải:
Phương trình hóa học: 2K + 2H2O → 2KOH + H2
bazo KOH làm quỳ tím chuyển sang màu xanh
Ví dụ 4: Khi cho quỳ tím vào dung dịch axit, quỳ tím chuyển màu gì:
A. Đỏ
B. Xanh
C. Tím
D. Không màu
Đáp án A
Hướng dẫn giải:
Khi cho quỳ tím vào dung dịch axit, quỳ tím chuyển màu đỏ
Ví dụ 5: Cho mẩu K vào nước thấy có 4,48 lít (đktc) khí bay lên. Tính khối lượng K
A. 9,2 g
B. 15,6 g
C. 7,8 g
D. 9,6 g
Đáp án B
Hướng dẫn giải:
nH2 = 4,48/22,4 = 0,2 mol
Phương trình phản ứng hóa học xảy ra
2K + 2H2O → 2KOH + H2
0,4 ← 0,2 mol
mK = 0,4.39 = 15,6 gam
Ví dụ 6: Cho quỳ tím vào nước vôi trong, hiện tượng xảy ra là
A. Quỳ tím chuyển màu đỏ
B. Quỳ tím không đổi màu
C. Quỳ tím chuyển màu xanh
D. Không có hiện tượng
Đáp án C
Hướng dẫn giải:
Cho quỳ tím vào nước vôi trong, hiện tượng xảy ra là Quỳ tím chuyển màu xanh
Ví dụ 7: Nhỏ từ từ từng giọt đến hết 30 ml dung dịch HCl 1M vào 100 ml dung dịch chứa K2CO3 0,2M và KHCO3 0,2M. Sau khi phản ứng kết thúc, thể tích khí CO2 thu được là
A. 224 ml.
B. 336 ml.
C. 672 ml.
D. 448 ml.
Đáp án A
Hướng dẫn giải:
nHCl= 0,03 (mol)
nK2CO3 = 0,1.0,2 = 0,02 (mol);
nKHCO3 = 0,1.0,2 = 0,02 (mol)
Khi nhỏ từ từ H+ vào dd hỗn hợp CO32- và HCO3- xảy ra phản ứng:
H+ + CO32- → HCO3- (1)
H+ + HCO3- → CO2 + H2O (2)
=> nCO2(2) = ∑nH+ - nCO32- = 0,03 – 0,02 = 0,01 (mol)
=> VCO2 (đktc) = 0,01.22,4 = 0,224 (l) = 224 (ml)
Ví dụ 8: Dãy gồm các kim loại đều phản ứng với nước ở nhiệt độ thường tạo ra dung dịch có môi trường kiềm là
A. Na, Ba, K
B. Be, Na, Ca
C. Na, Fe, K
D. Na, Cr, K
Đáp án A
Hướng dẫn giải:
2A + 2H2O → 2AOH + H2 (A là kim loại kiềm)
B + 2H2O → B(OH)2 + H2(B là kim loại kiềm thổ, trừ Be)
2Na + 2H2O → 2NaOH + H2
Ba + 2H2O → Ba(OH)2 + H2
2K + 2H2O → 2KOH + H2
Ví dụ 9: Nhận định nào sau đây không đúng về kim loại kiềm?
A. Đều có cấu tạo mạng tinh thể giống nhau: lập phương tâm khối
B. Là những nguyên tố mà nguyên tử có 1 e ở phân lớp p
C. Dễ bị oxi hóa
D. Năng lượng ion hóa thứ nhất của các nguyên tử kim loại kiềm thấp hơn so với các nguyên tố khác trong cùng chu kì
Đáp án B
Ví dụ 10: Nhận định nào sau đây là đúng:
A. Bari là nguyên tố có tính khử mạnh nhất trong dãy kim loại kiềm thổ
B. Tất cả các kim loại kiềm thổ đều tan trong nước ở nhiệt độ thường
C.Kim loại kiềm thổ có tính khử mạnh hơn kim loại kiềm
D. Tính khử của các kim loại kiềm thổ tăng dần từ Be đến Ba.
Đáp án D
Hướng dẫn giải:
Mg và Be không phản ứng với nước ở điều kiện thường B sai.
Đi từ đầu nhóm IIA đến cuối nhóm theo chiều tăng dần điện tính hạt nhân tính kim loại (tính khử) tăng dần => Kim loại mạnh nhất là Ra; yếu nhất là Be. => A sai, D đúng.
Nhóm Kim loại kiềm có tính khử mạnh nhất => C sai.
Ví dụ 11: Cặp chất nào dưới đây không xảy ra phản ứng
A. H2SO4 và KHCO3.
B. MgCO3 và HCl.
C. Ba(OH)2 và K2CO3.
D. NaCl và K2CO3.
Đáp án D
Hướng dẫn giải:
Cặp chất không xảy ra phản ứng là NaCl và K2CO3
Loại đáp án A, B, C vì các cặp chất phản ứng với nhau.
A. H2SO4 và KHCO3.
H2SO4 + 2 KHCO3 → 2 CO2 + 2 H2O + K2SO4
B. MgCO3 và HCl.
MgCO3 + 2HCl → MgCl2 + CO2 ↑ + H2O
C. Ba(OH)2 và K2CO3.
Ba(OH)2 + K2CO3 → 2KOH + BaCO3↓
8. Một số phương trình phản ứng hóa học khác của Kali và hợp chất: