Chúng tôi xin giới thiệu phương trình Al(OH)3 + NaOH → NaAlO2 + H2O gồm điều kiện phản ứng, cách thực hiện, hiện tượng phản ứng và một số bài tập liên quan giúp các em củng cố toàn bộ kiến thức và rèn luyện kĩ năng làm bài tập về phương trình phản ứng hóa học. Mời các bạn đón xem:
Phương trình Al(OH)3 + NaOH → NaAlO2 + H2O
1. Phương trình phản ứng hóa học
Al(OH)3 + NaOH → NaAlO2 + 2H2O
2. Hiện tượng nhận biết phản ứng
- Sản phẩm thu được chất rắn màu trắng.
3. Điều kiện phản ứng
- Nhiệt độ: 1000°C.
4. Bản chất của các chất tham gia phản ứng
4.1. Bản chất của Al(OH)3 (Nhôm hidroxit)
Al(OH)3 là một hidroxit lưỡng tính nên có thể tác dụng được với axit mạnh và dung dịch có tính kiềm mạnh.
4.2. Bản chất của NaOH (Natri hidroxit)
NaOH là một bazơ mạnh nên tác dụng được với hợp chất lưỡng tính như Al(OH)3 hoặc Al2O3.
5. Tính chất hóa học
5.1. Tính chất hóa học của Al(OH)3
Kém bền với nhiệt: Khi đun nóng Al(OH)3 phân hủy thành Al2O3.
2Al(OH)3 Al2O3 + 3H2O
- Là hiđroxit lưỡng tính
Tác dụng với axit mạnh:
Al(OH)3 + 3HCl → AlCl3 + 3H2O
Tác dụng với dung dịch kiềm mạnh:
Al(OH)3 + KOH → KAlO3 + 2H3O
Al(OH)3 + KOH → K[Al(OH)4]
5.2. Tính chất hóa học của NaOH
NaOH Là một bazơ mạnh nó sẽ làm quỳ tím chuyển màu xanh, còn dung dịch phenolphtalein thành màu hồng. Một số phản ứng đặc trưng của Natri Hidroxit được liệt kê ngay dưới đây.
Phản ứng với axit tạo thành muối + nước:
NaOHdd + HCldd→ NaCldd + H2O
Phản ứng với oxit axit: SO2, CO2…
2 NaOH + SO2→ Na2SO3 + H2O
NaOH + SO2→ NaHSO3
Phản ứng với axit hữu cơ tạo thành muối và thủy phân este, peptit:
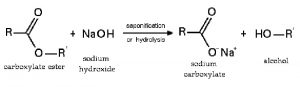
Phản ứng với muối tạo bazo mới + muối mới (điều kiện: sau phản ứng phải tạo thành chất kết tủa hoặc bay hơi):
2 NaOH + CuCl2→ 2NaCl + Cu(OH)2↓
Tác dụng với kim loại lưỡng tính:
2 NaOH + 2Al + 2H2O→ 2NaAlO2 + 3H2↑
2NaOH + Zn → Na2ZnO2 + H2↑
Tác dụng với hợp chất lưỡng tính:
NaOH + Al(OH)3 → NaAl(OH)4
2NaOH + Al2O3 → 2NaAlO2 + H2O
6. Cách thực hiện phản ứng
- Cho dung dịch Al(OH)3 từ từ và ống nghiệm chứa sẵn dung dịch NaOH.
7. Bạn có biết
- Zn(OH)2, Cr(OH)3 cũng có phản ứng tương tự
8. Bài tập liên quan
Câu 1. Nhỏ từ từ cho đến dư dung dịch NaOH vào dung dịch AlCl3 hiện tượng xảy ra là
A. Có kết tủa keo trắng, sau đó kết tủa tan.
B. Chỉ có kết tủa keo trắng.
C. Có kết tủa keo trắng và khí bay lên.
D. Không có kết tủa, có khí bay lên.
Lời giải:
Nhỏ từ từ cho đến dư dung dịch NaOH vào dung dịch AlCl3, ban đầu có kết tủa keo trắng xuất hiện.
3NaOH + AlCl3→ Al(OH)3 ↓ + 3NaCl
Sau đó kết tủa keo trắng tan trong NaOH dư tạo dung dịch trong suốt (vì Al(OH)3 có tính lưỡng tính tan được trong dung dịch axit dư, và kiềm dư)
NaOH + Al(OH)3 → NaAlO2+ 2H2O
Câu 2. Các đồ vật bằng nhôm bền trong không khí và nước là do:
A. Có một lớp Al(OH)3 bên ngoài bảo vệ
B. Có một lớp Al2O3 bên ngoài bảo vệ
C. Nhôm không tan trong nước
D. Nhôm bền, không bị oxi hóa
Lời giải:
Nhôm bền trong môi trường không khí và nước là do có màng oxit Al2O3 bền vững bảo vệ
Khi nhôm tác dụng chậm với oxi và hơi nước, chúng tạo thành một lớp nhôm oxit (Al2O3).
Lớp nhôm oxit này bám rất chắc vào bề mặt nhôm. Và ngăn chặn hoàn toàn không cho oxi tác dụng trực tiếp với nhôm. Do đó, nhôm bền trong môi trường không khí là nhờ lớp bảo vệ nhôm oxit ngay cả khi đun nóng
Câu 3. Chất nào dưới đây có thể tác dụng được với HCl và dung dịch NaOH
A. CuO
B. Fe(OH)3
C. Al(OH)3
D. Al(NO3)3
Lời giải:
Phương trình phản ứng xảy ra
Al(OH)3 + NaOH → NaAlO2 + 2H2O
Al(OH)3 + 3HCl → AlCl3+ 3H2O
Câu 4. Dãy các chất đều phản ứng được với kim loại nhôm là:
A. O2, Cl2, NaOH
B. O2, Cl2, Mg(OH)2
C. O2, S, HNO3 đặc, nguội
D. O2, S, MgCl2
Lời giải:
Câu 5. Dãy chất nào dưới đây phản ứng được NaOH?
A. Al2O3; Al(OH)3; NaNO3
B. Al2O3; Fe, Al(OH)3
C. Al(NO3)3, HCl, CO2
D. FeCl3, Ag, CO2
Lời giải:
Phương trình phản ứng liên quan
Al(NO3)3 + 3NaOH → Al(OH)3 + 3NaNO3
NaOH + HCl → NaCl + H2O
CO2 + NaOH → Na2CO3 + H2O
Câu 6. Thổi V lít khí CO2 (đktc) vào 100ml dd Ca(OH)2 1M thu được 6 gam kết tủa. Lọc kết tủa đun nóng dd lại thấy có kết tủa nữa. Tìm V?
A. 1,08 lít
B. 3,136 lít
C. 2,24 lít
D. 3,36 lít
Lời giải:
nkết tủa = = 0,06 mol
Vì đun nóng lại thu được kết tủa nên dd thu được 2 muối: CaCO3; Ca(HCO3)2.
Phương trình hóa học
CO2+ Ca(OH)2 → CaCO3 + H2O
0,06
2CO2 + Ca(OH)2 → Ca(HCO3)2.
0,08 0,04
→ n(CO2) = 0,06 + 0,08 = 0,14. → V = 3,136 lít.
Câu 7. Phát biểu nào dưới đây là sai ?
A. Cho từng viên Na vào dung dịch AlCl3, xảy ra hiện tượng Natri tan, sủi bọt khí, có xuất hiện kết tủa keo trắng, sau đó kết tủa tan
B. Al(OH)3, Al2O3, Al đều là các chất lưỡng, tính
C. Nhôm là kim loai nhẹ và có khả năng dẫn điện Iot
D. Từ Al2O3 có thế điều chế được Al.
Lời giải:
A đúng vì đầu tiên Na tác dụng với nước, tan và tạo bọt khí, sau đó tạo kết tủa Al(OH)3, khi Na dư kết tủa sẽ tan
B Sai vì chỉ có Al(OH)3, Al2O3, là các chất lưỡng, tính còn Al không phải là chất lưỡng tính
C. Đúng
D đúng
Câu 8. Cho sơ đồ phản ứng sau: Al → X → Y → Al(OH)3. Trong sơ đồ trên, mỗi mũi tên là một phản ứng, các chất X, Y lần lượt là
A. NaAlO2 và Al(OH)3
B. Al2O3 và Al(NO3)3
C. Al(OH)3 và Al2O3
D. Al(OH)3 và Al(NO3)3
Lời giải:
Phương trình phản ứng hóa học
4Al + 3O2 → 2Al2O3
Al2O3 + 6HNO3 → 2Al(NO3)3 + 3H2O
Al(NO3)3 + 3NH3+ 3H2O → Al(OH)3 + 3NH4NO3
Câu 9. Phát biểu nào dưới đây đúng trong các câu sau:
A. Nhôm là kim loại lưỡng tính.
B. Al(OH)3 là một bazo lưỡng tính có thể tác dụng HCl và NaOH
C. Al(OH)3 là một hidroxit lưỡng tính có thể tác dụng HCl và NaOH
D. Al2O3 là oxit trung tính.
Lời giải:
A sai vì Nhôm không phải là kim loại lưỡng tính.
B sai Al(OH)3 là một hidroxit lưỡng tính có thể tác dụng HCl và NaOH
C đúng
D sai Al2O3 là oxit lưỡng tính
Câu 10. Nhôm bị thụ động trong dung dịch nào sau đây
A. H2SO4 đặc nóng
B. HNO3 đặc nguội
C. H2SO4 loãng
D. HNO3 đặc nóng
Lời giải:
Nhôm bị thụ động trong dung dịch: HNO3 đặc nguội
Câu 11. Criolit (còn gọi là băng thạch) có công thức phân tử Na3AlF6, được thêm vào Al2O3 trong quá trình điện phân Al2O3 nóng chảy để sản xuất nhôm. Cho các tác dụng sau:
(1) Bảo vệ điện cực khỏi bị ăn mòn.
(2) Làm tăng độ dẫn điện của Al2O3 nóng chảy
(3) Làm giảm nhiệt độ nóng chảy của Al2O3
(4) Tạo lớp ngăn cách để bảo vệ Al nóng chảy
Tác dụng của Criolit là đúng
A. (1), (2), (3), (4)
B. (1), (2), (3)
C. (2), (3), (4)
D. (1), (2), (4)
Lời giải:
(2) Làm tăng độ dẫn điện của Al2O3 nóng chảy
(3) Làm giảm nhiệt độ nóng chảy của Al2O3
(4) Tạo lớp ngăn cách để bảo vệ Al nóng chảy
9. Một số phương trình phản ứng hoá học khác của Nhôm (Al) và hợp chất:
Al(OH)3 + NaOH → NaAlO2 + H2O

