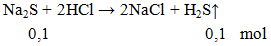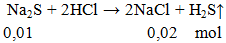Chúng tôi xin giới thiệu phương trình Na2S + 2HCl → 2NaCl + H2S ↑ gồm điều kiện phản ứng, cách thực hiện, hiện tượng phản ứng và một số bài tập liên quan giúp các em củng cố toàn bộ kiến thức và rèn luyện kĩ năng làm bài tập về phương trình phản ứng hóa học của Natri. Mời các bạn đón xem:
Phương trình Na2S + 2HCl → 2NaCl + H2S ↑
1. Phương trình phản ứng hóa học:
Na2S + 2HCl → 2NaCl + H2S ↑
2. Hiện tượng nhận biết phản ứng
- Có khí không màu, mùi trứng thôi thoát ra.
3. Điều kiện phản ứng
- điều kiện thường,
4. Tính chất hóa học
- Phản ứng với thuốc thử vô cơ
S2- + H2O → HS- + OH-
- Phản ứng oxy hóa khi tiến hành đun nóng Na2S với natri cacbonat với lưu huỳnh dioxit
2Na2S + 3O2 + 2CO2 → 2NA2CO3 + 2SO2
- Phản ứng oxy hóa cùng với hidro peroxit
Na2S + 4H2O2 → 4H2O + Na2SO4
- Cho lưu huỳnh phản ứng với natri sunfua tạo thành polysulfides
2Na2S + S8 → 2Na2S5
- Natri sunfua + HCl sinh ra H2S – một loại khí độc với mùi hôi thối
Na2S + 2HCl → 2NaCl + H2S
5. Cách thực hiện phản ứng
- Nhỏ HCl vào ống nghiệm chứa Na2S
6. Bạn có biết
- Na2S phản ứng với các axit như H2SO4, HBr… đều giải phóng khí.
7. Bài tập liên quan
Ví dụ 1: Nhỏ HCl vào ống nghiệm chứa Na2S thu được hiện tượng là
A. Có khí không màu, mùi trứng thối thoát ra.
B. Có khí màu nâu đỏ thoát ra.
C. Có khí màu vàng lục, mùi xốc thoát ra.
D. Không có hiện tượng gì.
Hướng dẫn giải
Na2S + 2HCl → 2NaCl + H2S ↑
H2S: khí không màu, mùi trứng thối.
Đáp án A.
Ví dụ 2: Thể tích khí ở dktc thoát ra khi cho 7,8g Na2S phản ứng hoàn toàn với lượng dư HCl là
A. 1,12 lít.
B. 2,24 lít.
C. 3,36 lít.
D. 4,48 lít.
Hướng dẫn giải
V = 0,1.22,4 = 2,24 lít.
Đáp án B.
Ví dụ 3: Cho 0,78g Na2S phản ứng hoàn toàn với lượng HCl, khối lượng muối có trong dung dịch thu được sau phản ứng là
A. 1,17 gam.
B. 0,745 gam.
C. 0,475 gam.
D. 1,49 gam.
Hướng dẫn giải
khối lượng muối = 0,02.58,5 = 1,17 gam.
Đáp án A.
8. Một số phương trình phản ứng hóa học khác của Natri và hợp chất: