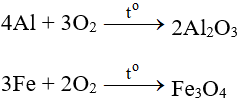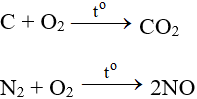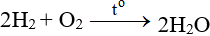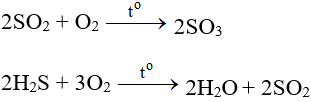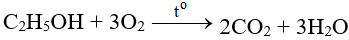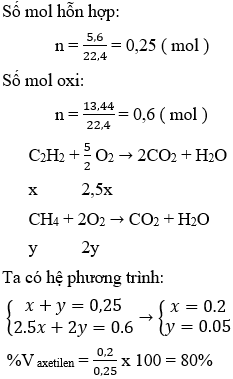Chúng tôi xin giới thiệu phương trình 2C2H2 + 5O2 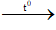
Phương trình 2C2H2 + 5O2 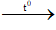
1. Phản ứng hóa học:
2C2H2 + 5O2 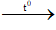
2. Điều kiện phản ứng
- Nhiệt độ cao.
3. Cách thực hiện phản ứng
- Đốt cháy axetilen trong oxi ở điều kiện nhiệt độ cao.
4. Hiện tượng nhận biết phản ứng
- Khi đốt cháy axetilen trong oxi ở điều kiện nhiệt độ cao thì thấy có khí không màu thoát ra (CO2).
5. Tính chất hóa học
5.1. Tính chất hóa học của C2H2
a. Phản ứng cộng
Phản ứng cộng halogen (phản ứng halogen hóa)
- Cộng brom
CH ≡ CH + Br - Br → Br-CH = CH - Br
Sản phẩm sinh ra có liên kết đôi trong phân tử nên có thể cộng tiếp với môt phân tử brom nữa:
Br-CH = CH - Br + Br - Br → Br2CH-CH-Br2
- Cộng clo
C2H2+ Cl2 → C2H2Cl2
- Phản ứng cộng hiđro (phản ứng hiđro hóa)
C2H2 + H2→ C2H6
Điều kiện phản ứng xảy ra C2H2 và H2: Nhiệt độ, xúc tác Niken
Lưu ý: Ngoài ra khi cho C2H2 tác dụng với H2 ở điều kiện nhiệt độ chất xúc tác khác nhau cho sản phẩm khác nhau
C2H2 + H2 → C2H4
- Phản ứng cộng axit
C2H2 + HCl → C2H3Cl (Nhiệt độ và xúc tác HgCl2)
- Phản ứng cộng nước (phản ứng hiđrat hóa
C2H2 + H2O → CH3CHO (Nhiệt độ: 80 độ C Xúc tác: Hg2+ Dung môi: H2SO4)
b. Phản ứng đime hóa và trime hóa
Hai phân tử axetilen có thể cộng hợp với nhau tạo thành vinylaxetilen
Đime hóa:
2CH≡CH → CH2=CH−C≡CH (Nhiệt độ xúc tác)
(Vinyl axetilen)
Trime hóa:
3CH≡CH → C6H6
c. Phản ứng oxi hóa
Phản ứng oxi hóa
Axetilen là hiđrocacbon, vì vậy khi đốt, axetilen sẽ cháy tạo ra cacbon Đioxit và nước, tương tự metan và etilen.
Axetilen cháy trong không khí với ngọn lửa sáng, tỏa nhiều nhiệt.
C2H2 + 5/2O2 → 2CO2 + H2O
5.2. Tính chất hóa học của O2
Khi tham gia phản ứng, nguyên tử O dễ dàng nhận thêm 2e. Nguyên tử oxi có độ âm điện lớn (3,44), chỉ kém flo (3,98).
Do vậy, oxi là nguyên tố phi kim hoạt động hoá học, có tính oxi hoá mạnh. Trong các hợp chất (trừ hợp chất với flo), nguyên tố oxi có số oxi hoá là -2.
Oxi tác dụng với hầu hết các kim loại (trừ Au, Pt, ...) và các phi kim (trừ halogen). Oxi tác dụng với nhiều hợp chất vô cơ và hữu cơ.
a. Tác dụng với kim loại
Tác dụng với hầu hết kim loại (trừ au và Pt), cần có to tạo oxit:
b. Tác dụng với phi kim
Tác dụng với hầu hết phi kim (trừ halogen), cần có to tạo oxit:
ĐB: Tác dụng với H2 nổ mạnh theo tỉ lệ 2:1 về số mol:
c. Tác dụng với hợp chất
- Tác dụng với các chất có tính khử:
- Tác dụng với các chất hữu cơ:
6. Bạn có biết
- Phản ứng trên là phản ứng oxi hóa hoàn toàn.
- Phản ứng cháy của axetilen tỏa nhiều nhiệt.
- Số mol CO2 > H2O và số mol ankin phản ứng bằng hiệu số mol của CO2 và H2O.
7. Bài tập liên quan
Ví dụ 1: Đốt cháy hoàn toàn 5,6 lít hỗn hợp metan và axetilen cần 13,44 lít oxi. Phần trăm thể tích axetilen trong hỗn hợp là?
A. 20%
B. 40%
C. 60%
D. 80%
Hướng dẫn:
Đáp án D
Ví dụ 2: Đốt cháy hoàn toàn khí axetilen rồi sục hỗn hợp khí thu được qua dung dịch nước vôi trong. Hiện tượng thu được là gì?
A. Kết tủa trắng
B. Có khí thoát ra
C. Không có hiện tượng
D. Dung dịch nước vôi có màu vàng
Hướng dẫn:
2C2H2 + 5O2 → 4CO2 + 2H2O
CO2 + Ca(OH)2 → CaCO3↓ + H2O
Đáp án A
Ví dụ 3: Ứng dụng trong phản ứng cháy của axetilen dùng để làm gì?
A. Làm nguyên liệu sản xuất trong công nghiệp
B. Làm dung môi
C. Hàn cắt kim loại
D. Không có ứng dụng
Hướng dẫn: Vì phản ứng cháy của axetilen tỏa nhiều nhiệt nên được sử dụng trong các đèn xì để hàn cắt kim loại.
Đáp án C.
8. Một số phương trình phản ứng hoá học khác của Ankin và hợp chất: