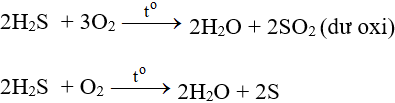Chúng tôi xin giới thiệu phương trình H2S + NaOH → Na2S + H2O gồm điều kiện phản ứng, cách thực hiện, hiện tượng phản ứng và một số bài tập liên quan giúp các em củng cố toàn bộ kiến thức và rèn luyện kĩ năng làm bài tập về phương trình phản ứng hóa học. Mời các bạn đón xem:
Phương trình H2S + NaOH → Na2S + H2O
1. Phương trình phản ứng hóa học
H2S + 2NaOH → Na2S + 2H2O
2. Hiện tượng nhận biết phản ứng.
- Quan sát sự chuyển màu của chỉ thị phù hợp trước và sau phản ứng.
3. Điều kiện phản ứng
- Phản ứng xảy ra ngay điều kiện thường.
4. Bản chất của các chất tham gia phản ứng
a. Bản chất của H2S (Hidro sunfua)
Dung dịch H2S có tính axit yếu ở 2 nấc nên khi tác dụng với dung dịch kiềm thì có thể tạo muối axit hoặc tạo muối trung hoà.
b. Bản chất của NaOH (Natri hidroxit)
NaOH là một bazo mạnh phản ứng với axit tạo thành muối và nước.
5. Tính chất hóa học
5.1. Tính chất hóa học của H2S
a. Tính axit yếu
Hiđro sunfua tan trong nước tạo thành dung dịch axit rất yếu (yếu hơn axit cacbonic), có tên là axit sunfuhiđric (H2S).
Axit sunfuhiđric tác dụng với kiềm tạo nên 2 loại muối: muối trung hòa, như Na2S chứa ion S2- và muối axit như NaHS chứa ion HS−.
H2S + NaOH → NaHS + H2O
H2S + 2NaOH → Na2S + 2H2O
b. Tính khử mạnh
Là chất khử mạnh vì trong H2S lưu huỳnh có số oxi hoá thấp nhất (-2).
Khi tham gia phản ứng hóa học, tùy thuộc vào bản chất và nồng độ của chất oxi hóa, nhiệt độ,...mà nguyên tố lưu huỳnh có số oxi hóa −2 (S-2) có thể bị oxi hóa thành (S0), (S+4), (S+6).
Tác dụng với oxi có thể tạo S hoặc SO2 tùy lượng ôxi và cách tiến hành phản ứng.
Ở nhiệt độ cao, khí H2S cháy trong không khí với ngọn lửa xanh nhạt, H2S bị oxi hóa thành SO2:
Tác dụng với clo có thể tạo S hay H2SO4 tùy điều kiện phản ứng.
H2S + 4Cl2 + 4H2O → 8HCl + H2SO4
H2S + Cl2 → 2HCl + S (khí clo gặp khí H2S)
5.2. Tính chất hóa học của NaOH
NaOH Là một bazơ mạnh nó sẽ làm quỳ tím chuyển màu xanh, còn dung dịch phenolphtalein thành màu hồng. Một số phản ứng đặc trưng của Natri Hidroxit được liệt kê ngay dưới đây.
Phản ứng với axit tạo thành muối + nước:
NaOHdd + HCldd→ NaCldd + H2O
Phản ứng với oxit axit: SO2, CO2…
2 NaOH + SO2→ Na2SO3 + H2O
NaOH + SO2→ NaHSO3
Phản ứng với axit hữu cơ tạo thành muối và thủy phân este, peptit:
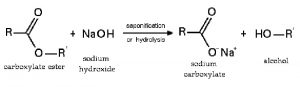
Phản ứng với muối tạo bazo mới + muối mới (điều kiện: sau phản ứng phải tạo thành chất kết tủa hoặc bay hơi):
2 NaOH + CuCl2→ 2NaCl + Cu(OH)2↓
Tác dụng với kim loại lưỡng tính:
2 NaOH + 2Al + 2H2O→ 2NaAlO2 + 3H2↑
2NaOH + Zn → Na2ZnO2 + H2↑
Tác dụng với hợp chất lưỡng tính:
NaOH + Al(OH)3 → NaAl(OH)4
2NaOH + Al2O3 → 2NaAlO2 + H2O
6. Cách thực hiện phản ứng
- Dẫn khí H2S vào ống nghiệm chứa NaOH và vài giọt chất chỉ thị.
7. Bạn có biết
- NaOH phản ứng với H2S tùy theo tỉ lệ về số mol mà sản phẩm thu được có thể là muối sunfua trung hòa hoặc muối axit hoặc hỗn hợp cả hai muối.
NaOH phản ứng với H2S chỉ thu được muối NaHS khi T = 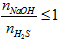
8. Bài tập liên quan
Câu 1. Dẫn từ từ đến dư H2S vào dung dịch NaOH thu được dung dịch X. Muối tan có trong dung dịch X là
A. Na2S.
B. Na2S và NaHS.
C. NaHS.
D. Na2S và NaOH.
Lời giải:
Đáp án: C
Giải thích:
Do H2S dư nên có phản ứng
NaOH + H2S → NaHS + H2O
Muối tan có trong dung dịch X là NaHS.
Câu 2. Thực hiện các thí nghiệm sau ở điều kiện thường
(a) Sục khí H2S vào dung dịch NaOH.
(b) Cho kim loại Na và nước.
(c) Sục khí Cl2 vào dung dịch Ca(OH)2.
(d) Trộn dung dịch NH4Cl với dung dịch NaOH.
(e) Cho bột Zn vào dung dịch HNO3.
(f) Trộn dung dịch FeCl2 với dung dịch AgNO3 dư.
Số thí nghiệm xảy ra phản ứng oxi hóa – khử là :
A. 3
B. 4
C. 2
D. 5
Lời giải:
Đáp án: B
Giải thích:
(b) Cho kim loại Na và nước.
(c) Sục khí Cl2 vào dung dịch Ca(OH)2
(e) Cho bột Zn vào dung dịch HNO3.
(f) Trộn dung dịch FeCl2 với dung dịch AgNO3 dư
Câu 3. Cho khí H2S lội qua dung dịch CuSO4 thấy có kết tủa màu xám đen xuất hiện, chứng tỏ:
A. Có phản ứng oxi hoá - khử xảy ra.
B. Có kết tủa CuS tạo thành, không tan trong axit mạnh.
C. Axit sunfuhiđric mạnh hơn axit sunfuric.
D. Axit sunfuric mạnh hơn axit sunfuhiđric.
Lời giải:
Đáp án: B
Giải thích:
Phương trình phản ứng
H2S + CuSO4 → CuS↓ (kết tủa đen) + H2SO4
=> Có kết tủa CuS tạo thành, không tan trong axit mạnh.
Câu 4. Trong các câu sau đây, câu nào sai?
A. Khi sục H2S vào dung dịch NaOH, Nếu 1 < nNaOH/nH2S < 2: xảy ra cả 2 phản ứng cả NaOH và H2S đều hết phản ứng hết
B. H2S vừa có tính oxi hóa, vừa có tính khử
C. SO2 vừa có tính oxi hóa, vừa có tính khử.
D. H2S làm mất màu dung dịch brom.
Lời giải:
Đáp án: B
Câu 5. Phát biểu nào sau đây sai?
A. H2S tan trong nước tạo thành dung dịch axit mạnh, có tính khử mạnh
B. SO2 là chất vừa có tính oxi hóa, vừa có tính khử
C. Ở nhiệt độ thường, SO3 là chất lỏng không màu, tan vô hạn trong nước
D. Trong công nghiệp, SO2 đực sản xuất bằng cách đốt S hoặc FeS
Lời giải:
Đáp án: A
9. Một số phương trình phản ứng hoá học khác của Lưu huỳnh (S) và hợp chất:
H2S + NaOH → Na2S + H2O