Chọn phương án sai.
A - sai vì: Đẳng quá trình là quá trình trong đó 1 thông số trạng thái của chất khí được giữ không đổi
B, C, D - đúng
Quá trình biến đổi trạng thái trong đó nhiệt độ được giữ không đổi gọi là quá trình
Quá trình đẳng nhiệt là quá trình biến đổi trạng thái trong đó nhiệt độ được giữ không đổi.
Trong quá trình đẳng nhiệt của một lượng khí nhất định, thể tích của lượng khí
Ta có: Định luật Bôilơ - Mariốt:
Trong quá trình đẳng nhiệt của một lượng khí nhất định, áp suất tỉ lệ nghịch với thể tích.
\(p \sim \dfrac{1}{V} \to pV = h/s\)
Hay nói cách khác thể tích của khí tỉ lệ nghịch với áp suất khí
Phát biểu nào sau đây là đúng khi nói về quá trình đẳng nhiệt của một lượng khí xác định?
Ta có: Định luật Bôilơ - Mariốt:
Trong quá trình đẳng nhiệt của một lượng khí nhất định, áp suất tỉ lệ nghịch với thể tích.
\(p \sim \dfrac{1}{V} \to pV = h/s\)
=> Các phương án:
A, D – sai vì: áp suất tỉ lệ nghịch với thể tích
B – sai vì: Tích của áp suất và thể tích là một hằng số chứ không phải thương
C - đúng
Hệ thức nào sau đây không đúng của định luật Bôi-lơ – Ma-ri-ốt là:
A, B, D - đúng
C - sai vì: \(pV = const\)
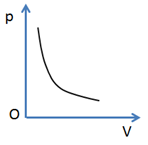
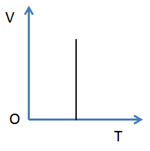
Đồ thị nào sau đây không biểu diễn đúng định luật Bôi-lơ – Ma-ri-ốt trong các hệ tọa độ?
A, C, D – đúng
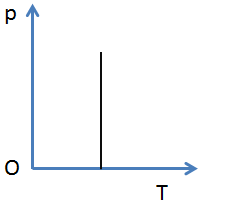
B – sai vì: đồ thị (p,T) của quá trình đẳng nhiệt có dạng:
Một khối lượng khí lí tưởng xác định có áp suất \(2atm\) được làm tăng áp suất lên đến \(8atm\) ở nhiệt độ không đổi thì thể tích biến đổi một lượng là \(3\) lít. Thể tích ban đầu của khối khí là
+ Trạng thái 1: \(\left\{ \begin{array}{l}{V_1} = ?\\{p_1} = 2atm\end{array} \right.\)
+ Trạng thái 2: \(\left\{ \begin{array}{l}{V_2} = {V_1} - 3\\{p_2} = 8atm\end{array} \right.\)
Ta có, trong quá trình biến đổi trạng thái nhiệt độ của khí không đổi
=> Áp dụng định luật Bôi lơ – Ma ri ốt, ta có:
\(\begin{array}{l}{p_1}{V_1} = {p_2}{V_2}\\ \Leftrightarrow {p_1}{V_1} = {p_2}\left( {{V_1} - 3} \right)\\ \Leftrightarrow 2{V_1} = 8\left( {{V_1} - 3} \right)\end{array}\)
\( \Rightarrow {V_1} = 4\) lít
Biết ở điều kiện tiêu chuẩn, khối lượng riêng của Oxi là \(1,43kg/{m^3}\). Khối lượng khí Oxi đựng trong một bình kín có thể tích \(15\) lít dưới áp suất \(150atm\) ở nhiệt độ \({0^0}C\) bằng
+ Ở điều kiện tiêu chuẩn: \(\left\{ \begin{array}{l}{p_0} = 1atm\\{V_0}\\{\rho _0} = 1,43kg/{m^3}\\t = {0^0}C\end{array} \right.\) lại có \(m = {\rho _0}{V_0}\)
+ Ở áp suất \(150atm\): \(\left\{ \begin{array}{l}p = 150atm\\V\\\rho = \dfrac{m}{V}\\t = {0^0}C\end{array} \right.\)
Ta có nhiệt độ của khí không thay đổi, theo định luật Bôi lơ – Ma ri ốt, ta có:
\(\begin{array}{l}{p_0}{V_0} = pV\\ \Leftrightarrow {p_0}\dfrac{m}{{{\rho _0}}} = p\dfrac{m}{\rho }\\ \Rightarrow \rho = {\rho _0}\dfrac{p}{{{p_0}}} = 1,43.\dfrac{{150}}{1} = 214,5kg/{m^3}\end{array}\)
Ta có: \(V = 15l = {15.10^{ - 3}}{m^3}\)
=> Khối lượng \(m = \rho V = 214,{5.15.10^{ - 3}} = 3,22kg\)
Nếu áp suất của một lượng khí lí tưởng xác định tăng \(1,{5.10^5}Pa\) thì thể tích biến đổi \(3\) lít. Nếu áp suất của lượng khí đó tăng \({3.10^5}Pa\) thì thể tích biến đổi \(5\) lít. Biết nhiệt độ không đổi, áp suất và thể tích ban đầu của khí là:
Gọi \(\left\{ \begin{array}{l}{p_0}\\{V_0}\end{array} \right.\) là áp suất và thể tích khí ban đầu
+ Khi áp suất tăng \(1,{5.10^5}Pa\) \(\left\{ \begin{array}{l}{p_1} = {p_0} + 1,{5.10^5}\\{V_1} = {V_0} - 3\end{array} \right.\)
+ Khi áp suất tăng \({3.10^5}Pa\) \(\left\{ \begin{array}{l}{p_2} = {p_0} + {3.10^5}\\{V_1} = {V_0} - 5\end{array} \right.\)
Nhiệt độ không đổi => Quá trình đẳng nhiệt
Áp dụng định luật Bôi lơ – Ma ri ốt cho 3 trạng thái trên, ta có:
\(\begin{array}{l}{p_0}{V_0} = {p_1}{V_1} = {p_2}{V_2}\\ \Leftrightarrow {p_0}{V_0} = \left( {{p_0} + 1,{{5.10}^5}} \right)\left( {{V_0} - 3} \right) = \left( {{p_0} + {{3.10}^5}} \right)\left( {{V_0} - 5} \right)\\ \Rightarrow \left\{ \begin{array}{l}{p_0} = {6.10^5}Pa\\{V_0} = 15l\end{array} \right.\end{array}\)
Một quả bóng da có dung tích \(2,5\) lít. Người ta bơm không khí ở áp suất \({10^5}Pa\) vào bóng. Mỗi lần bơm được \(125c{m^3}\) không khí. Biết trước khi bơm, trong bóng có không khí ở áp suất \({10^5}Pa\) và nhiệt độ không đổi trong thời gian bơm. Áp suất không khí trong quả bóng sau \(20\) lần bơm bằng: (coi quả bóng trước khi bơm không có không khí).
Ta có:
Thể tích khí bơm được sau 20 lần bơm là \(20.0,125\) lít
+ Thể tích của không khí trước khi bơm vào bóng: \({V_1} = 20.0,125 + 2,5 = 5l\) (Bao gồm thể tích khí của 20 lần bơm và thể tích khí của khí có sẵn trong bóng)
+ Sau khi bơm khí vào trong bóng thể tích lượng khí chính bằng thể tích của bóng: \({V_2} = 2,5l\)
Do nhiệt đọ không đổi, theo định luật Bôi lơ – Ma ri ốt, ta có:
\(\begin{array}{l}{p_1}{V_1} = {p_2}{V_2}\\ \Leftrightarrow {10^5}.5 = {p_2}.2,5\\ \Rightarrow {p_2} = {2.10^5}Pa\end{array}\)
Một lượng khí ở nhiệt độ không đổi 200 C, thể tích 3m3, áp suất 2atm. Nếu áp suất giảm còn 1atm thì thể tích khối khí là bao nhiêu?
Áp dụng phương trình trạng thái khí lí tưởng \(\frac{{p.V}}{T} = \frac{{{p_0}.{V_0}}}{{{T_0}}}\)
Đổi :
\({T_0} = {t_0} + 273 = 20 + 273 = 293{\rm{ }}K\)
Áp dụng phương trình trạng thái khí lí tưởng :
\(\frac{{p.V}}{T} = \frac{{{p_0}.{V_0}}}{{{T_0}}} \Rightarrow \frac{{1.V}}{{293}} = \frac{{2.3}}{{293}} \Rightarrow V = 6{m^3}\)
Một xilanh chứa \(100c{m^3}\) khí ở \(2atm\). Pit-tông nén khí trong xilanh xuống còn \(80c{m^3}\). Coi nhiệt độ của quá trình nén khí không thay đổi, áp suất của khí trong xilanh khi đó là:
Áp dụng định luật Bôi-lơ-ma-ri-ốt cho hai trạng thái ta có:
\({p_1}{V_1} = {p_2}{V_2} \Rightarrow {p_2} = \dfrac{{{p_1}{V_1}}}{{{V_2}}} = \dfrac{{2.100}}{{80}} = 2,5atm\)
Nén khí đẳng nhiệt từ thể tích 25l đến thể tích 4l thì áp suất của khí:
Ta có: \({p_1}{V_1} = {p_2}{V_2} \Rightarrow \dfrac{{{p_2}}}{{{p_1}}} = \dfrac{{{V_1}}}{{{V_2}}} = \dfrac{{25}}{4} = 6,25\)
Người ta điều chế khí hiđrô và chứa vào một bình lớn dưới áp suất 1,5 atm, ở nhiệt độ 250C. Tính thể tích khí phải lấy từ bình lớn ra để nạp vào một bình nhỏ thể tích 30 lít dưới áp suất 15 atm. Coi nhiệt độ không đổi.
Áp dụng định luật Bôilơ – Mariốt ta có:
\({p_1}{V_1} = {p_2}{V_2} \Rightarrow {V_1} = \dfrac{{{p_2}{V_2}}}{{{p_1}}} = \dfrac{{15.30}}{{1,5}} = 300l\)
Phương án nào sau đây không phải là thông số trạng thái của một lượng khí
Ta có: Trạng thái của một lượng khí được xác định bằng các thông số: V (thể tích), p (áp suất) và T (nhiệt độ tuyệt đối).
=> Khối lượng không phải là thông số trạng thái của khí lí tưởng
Trạng thái của một lượng khí được xác định bởi các thông số:
Trạng thái của một lượng khí được xác định bằng các thông số: V (thể tích), p (áp suất) và T (nhiệt độ tuyệt đối).
Chọn phương án đúng.
A- đúng
B, C, D - sai vì:
+ Áp suất không đổi: Quá trình đẳng áp
+ Thể tích không đổi: Quá trình đẳng tích
+ Nhiệt độ không đổi: Quá trình đẳng nhiệt
Quá trình đẳng nhiệt là:
Quá trình đẳng nhiệt là quá trình biến đổi trạng thái trong đó nhiệt độ được giữ không đổi.
Khi nén khí đẳng nhiệt thì số phân tử trong một đơn vị thể tích
Ta có:
+ Số phân tử trong một đơn vị thể tích: \(n = \dfrac{N}{V}\) với N - số phân tử, V - thể tích
+ Khi nén khí đẳng nhiệt\(\left( {T = h/{\rm{s}}} \right)\): Theo định luật Bôilơ - Mariốt, ta có: \(p \sim \frac{1}{V}\)
Ta suy ra: \(p \sim n = \dfrac{N}{V}\)
=>Khi nén khí đẳng nhiệt thì số phân tử trong một đơn vị thể tích tăng tỉ lệ thuận với áp suất
Phát biểu nào sau đây là không đúng khi nói về quá trình đẳng nhiệt của một lượng khí xác định?
Ta có: Định luật Bôilơ - Mariốt:
Trong quá trình đẳng nhiệt của một lượng khí nhất định, áp suất tỉ lệ nghịch với thể tích.
\(p \sim \frac{1}{V} \to pV = h/s\)
=> Các phương án:
A, B, C - đúng
D - sai