Trường hợp nào sau đây tạo ra kim loại?
A. 4FeS2 + 11O2 $\xrightarrow{{{t^ \circ }}}$ 2Fe2O3 + 8SO2
B. Ca3(PO4)2 + MgSiO3$\xrightarrow{{{t^ \circ }}}$ Phân lân nung chảy
C. Ag2S + O2 $\xrightarrow{{{t^ \circ }}}$ 2Ag + SO2
D. Ca3(PO4)2 + 3SiO2 + 5C $\xrightarrow{{{t^ \circ }}}$ 3CaSiO3 + 2P + 5CO
Cho sơ đồ phản ứng: Al2(SO4)3 → X → Y→ Al.
Trong sơ đồ trên, mỗi mũi tên là một phản ứng, các chất X, Y lần lượt là những chất nào sau đây?
Al2(SO4)3 + 6NH3 + 6H2O $\xrightarrow{{}}$ 2Al(OH)3↓ + 3(NH4)2SO4
X
2Al(OH)3 $\xrightarrow{{{t^ \circ }}}$ Al2O3 + 3H2O
X Y
Al2O3 $\xrightarrow{{đpnc}}$ 2Al + $\dfrac{3}{2}$ O2 ↑
Cho lá Al vào dung dịch HCl, có khí thoát ra. Thêm vài giọt dung dịch CuSO4 vào thì
Khi thêm vài giọt CuSO4 vào dung dịch sẽ hình thành cặp pin điện hóa Al-Cu làm cho khí thoát ra nhanh hơn
Trường hợp nào sau đây xảy ra ăn mòn điện hoá?
A sai vì là ăn mòn hóa học, không hình thành hai điện cực mới
$3Ag + 4HN{O_3}\xrightarrow{{}}3AgN{O_3} + NO \uparrow + 2{H_2}O$
B sai vì ăn mòn hóa học:
$2Fe + 3C{l_2}\xrightarrow{{{t^o}}}2FeC{l_3}$
C sai vì ăn mòn hóa học, không hình thành hai điện cực mới
$2Al + 3{H_2}S{O_4}\xrightarrow[{}]{}A{l_2}{(S{O_4})_3} + 3{H_2} \uparrow $
D đúng vì hình thành điện cực Zn và Cu. Hai điện cực tiếp xúc với nhau và tiếp xúc với dung dịch điện ly là muối Zn2+ và Cu2+
$Zn\,\,\, + \,\,\,C{u^{2 + }}\xrightarrow{{}}Z{n^{2 + }} + \,\,\,\,Cu \downarrow $
Có 4 dung dịch riêng biệt: CuSO4, ZnCl2, FeCl3, AgNO3. Nhúng vào mỗi dung dịch một thanh Ni. Số trường hợp xuất hiện ăn mòn điện hoá là
CuSO4: Ăn mòn điện hóa vì hình thành hai điện cực Ni và Cu. Hai điện cực tiếp xúc với nhau và tiếp xúc với dung dịch điện ly là muối Ni2+ và Cu2+
$Ni\,\,\, + \,\,C{u^{2 + }}\,\xrightarrow{{}}N{i^{2 + }}\,\, + \,\,\,Cu \downarrow $
-ZnCl2: Không xảy ra ăn mòn do không có phản ứng
-FeCl3: Không xảy ra ăn mòn điện hóa vì không hình thành điện cực mới (không tạo ra Ni)
$Ni\,\,\, + \,\,\,\,2F{e^{3 + }}\xrightarrow{{}}N{i^{2 + }} + \,\,\,2F{e^{2 + }}$
-AgNO3: Ăn mòn điện hóa vì hình thành điện cực Ni và Ag. Hai điện cực tiếp xúc với nhau và tiếp xúc với dung dịch điện ly là muối Ni2+ và
$Ni\,\,\,\, + \,\,\,\,2A{g^ + }\xrightarrow{{}}N{i^{2 + }} + \,\,\,2Ag \downarrow $
Oxi hoá hoàn toàn m gam kim loại X cần vừa đủ 0,25m gam khí O2. X là kim loại nào sau đây?
Gọi hóa trị của X là n
$X = \dfrac{m}{n} = \dfrac{m}{{{n_e}}}$.n = $\dfrac{m}{{\dfrac{{0,25m.4}}{{32}}}}$ . n = 32.n
→ n = 2 và X = 64 → X là Cu
Đốt cháy hoàn toàn 7,2 gam kim loại M (có hoá trị hai không đổi trong hợp chất) trong hỗn hợp khí Cl2 và O2. Sau phản ứng thu được 23,0 gam chất rắn và thể tích hỗn hợp khí đã phản ứng là 5,6 lít (ở đktc). Kim loại M là
Áp dụng định luật bảo toàn khối lượng:
$ \to {m_{{O_2}}} + {m_{C{l_2}}} = 23 - 7,2 = 15,8\,\,gam$
$\left\{ \begin{gathered}{n_{{O_2}}} = x\,\,mol \hfill \\{n_{C{l_2}}} = y\,\,mol \hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered}x + y = \frac{{5,6}}{{22,4}} = 0,25 \hfill \\32{\text{x}} + 71y = 15,8 \hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered}x = 0,05 \hfill \\y = 0,2 \hfill \\ \end{gathered} \right.$
→ne trao đổi = $4{n_{{O_2}}} + 2{n_{C{l_2}}} = 4.0,05 + 2.0,2 = 0,6\,mol$
$M = \dfrac{m}{n} = \dfrac{m}{{{n_e}}}$.hóa trị = 12.hóa trị
→ Hóa trị = 2, M = 24 → M là Mg
Cho 7,84 lít hỗn hợp khí X (đktc) gồm Cl2 và O2 phản ứng vừa đủ với 11,1 gam hỗn hợp Y gồm Mg và Al, thu được 30,1 gam hỗn hợp Z. Phần trăm khối lượng của Al trong Y là
Áp dụng định luật bảo toàn khối lượng:
$ \to {m_X} = {m_{{O_2}}} + {m_{C{l_2}}} = {m_Z} - {m_Y} = 30,1 - 11,1 = 19\,\,gam$
$\left\{ \begin{gathered}{n_{{O_2}}} = x\,\,mol \hfill \\{n_{C{l_2}}} = y\,\,mol \hfill \\ \end{gathered} \right.\,\,\,\, \to \,\,\,\,\left\{ \begin{gathered}x + y = \dfrac{{7,84}}{{22,4}} = 0,35 \hfill \\32{\text{x}} + 71y = 19 \hfill \\ \end{gathered} \right.\,\,\,\,\, \to \,\,\,\,\left\{ \begin{gathered}x = 0,15 \hfill \\y = 0,2 \hfill \\ \end{gathered} \right.$
Gọi số mol của Mg và Al lần lượt là a và b
=> mhh Y = 24a + 27b = 11,1 (1)
Bảo toàn e: 2.nMg + 3.nAl = 2.nCl2 + 4.nO2
=> 2a + 3b = 2.0,2 + 4.0,15 = 1 (2)
Từ (1) và (2) => a = 0,35; b = 0,1
$ \to \% {m_{Al}} = \dfrac{{0,1.27}}{{11,1}}.100\% = 24,32\% $
Hòa tan hỗn hợp X gồm 11,2 gam Fe và 2,4 gam Mg bằng dung dịch H2SO4 loãng (dư), thu được dung dịch Y. Cho dung dịch NaOH dư vào Y thu được kết tủa Z. Nung Z trong không khí đến khối lượng không đổi, thu được m gam chất rắn. Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của m là
${n_{Fe}} = 0,2mol\,;\,{n_{Mg}} = 0,1mol$
$\left\{ \begin{gathered}Fe \hfill \\Mg \hfill \\ \end{gathered} \right.\xrightarrow{{ + {H_2}S{O_{4(l)}}}}\left\{ \begin{gathered}F{e^{2 + }} \hfill \\C{u^{2 + }} \hfill \\ \end{gathered} \right.\xrightarrow{{ + O{H^ - }}}\left\{ \begin{gathered}Fe{(OH)_2} \hfill \\Mg{(OH)_2} \hfill \\ \end{gathered} \right.\xrightarrow[{kk}]{{ + {O_2}}}\left\{ \begin{gathered}F{e_2}{O_3} \hfill \\MgO \hfill \\ \end{gathered} \right.\,\,$
Bảo toàn Fe: ${n_{F{{\text{e}}_2}{O_3}}} = \dfrac{1}{2}.{n_{F{\text{e}}}} = \dfrac{1}{2}.0,2 = 0,1\,mol$
Bảo toàn Mg: nMgO = nMg = 0,1 mol
=> m = 0,1.160 + 0,1.40 = 20 (gam)
Cho 12 gam hợp kim của bạc vào dung dịch HNO3 loãng (dư), đun nóng đến phản ứng hoàn toàn, thu được dung dịch có 8,5 gam AgNO3. Phần trăm khối lượng của bạc trong mẫu hợp kim là
${n_{AgN{O_3}}} = \dfrac{{8,5}}{{170}} = 0,05mol\,\, \to {n_{Ag}} = {n_{AgN{O_3}}} = 0,05mol$
$ \to \% {m_{Ag}} = \dfrac{{0,05.108}}{{12}} \cdot 100 = 45\% $
Cho 2,8 gam hỗn hợp X gồm Cu và Ag phản ứng hoàn toàn với dung dịch HNO3 dư, thu được 0,04 mol NO2 (sản phẩm khử duy nhất của N+5 ) và dung dịch chứa m gam muối. Giá trị của m là
${n_{N{O_2}}} = 0,04mol\,\, \to \,\,{n_{NO_3^ - }}$ (trong muối) = ne nhận = 0,04.1 = 0,04 mol
muối$ = {m_{KL}} + {m_{NO_3^ - }}$(muối) $ = 2,8 + 0,04.62 = 5,28g$
Hoà tan hoàn toàn 12,42 gam Al bằng dung dịch HNO3 loãng (dư), thu được dung dịch X và 1,344 lít (ở đktc) hỗn hợp khí Y gồm 2 khí là N2O và N2. Tỉ khối của hỗn hợp khí Y so với khí H2 là 18. Cô cạn dung dịch X, thu được m gam chất rắn khan. Giá trị của m là
${n_{Al}} = 0,46mol\,;\,{n_Y} = 0,06\,mol$
Đặt ${n_{{N_2}}} = x\,mol\,\,;\,\,{n_{{N_2}O}} = y\,\,mol$
$\left\{ \begin{gathered}x + y = 0,06 \hfill \\28x + 44y = 0,06.18.2 \hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered}x = 0,03 \hfill \\y = 0,03 \hfill \\ \end{gathered} \right.$
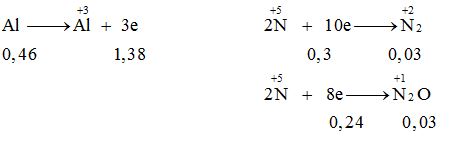
Ta thấy $3{n_{Al}} > (8{n_{{N_2}O}} + 10{n_{{N_2}}})$ → Có muối amoni NH4NO3
Áp dụng định luật bảo toàn e ta có:
$3{n_{Al}} = 8{n_{{N_2}O}} + 10{n_{{N_2}}} + 8{n_{NH_4^ + }} \to {n_{NH_4^ + }} = \dfrac{{0,46.3 - 0,54}}{8} = 0,105mol$
$ \to m = {m_{Al{{(N{O_3})}_3}}} + {m_{N{H_4}N{O_3}}} = 0,46.213 + 0,105.80 = 106,38g$
Cho 2,24 gam bột sắt vào 200 ml dung dịch chứa hỗn hợp gồm AgNO3 0,1M và Cu(NO3)2 0,5M. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X và m gam chất rắn Y. Giá trị của m là
${n_{Fe}} = 0,04mol\,;\,{n_{AgN{O_3}}} = 0,1.0,2 = 0,02mol\,;\,{n_{Cu{{(N{O_3})}_2}}} = 0,5.0,2 = 0,1mol$
$Fe\, + \,2A{g^ + }\xrightarrow{{}}F{e^{2 + }} + 2Ag \downarrow $
0,01 ← 0,02 → 0,02
$Fe\,+ \,C{u^{2 + }}\xrightarrow{{}}F{e^{2 + }} + Cu \downarrow $
0,03 < 0,1 → 0,03
=> mrắn = mAg + mCu = 0,02.108 + 0,03.64 = 4,08 (gam)
Cho một lượng bột Zn vào dung dịch X gồm FeCl2 và CuCl2. Khối lượng chất rắn sau khi các phản ứng xảy ra hoàn toàn nhỏ hơn khối lượng bột Zn ban đầu là 0,5 gam. Cô cạn phần dung dịch sau phản ứng thu được 13,6 gam muối khan. Tổng khối lượng các muối trong X là
mdd tăng = mrắn giảm = 0,5 gam → mdd ban đầu = 13,6 – 0,5 = 13,1 gam
Cho m gam bột Cu vào 400 ml dung dịch AgNO3 0,2M, sau một thời gian phản ứng thu được 7,76 gam hỗn hợp chất rắn X và dung dịch Y. Lọc tách X, rồi thêm 5,85 gam bột Zn vào Y, sau khi phản ứng xảy ra hoàn toàn thu được 10,53 gam chất rắn Z. Giá trị của m là
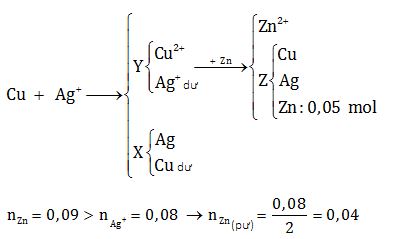
→ nZn dư = 0,05 mol
mX + mZ = mCu + mAg + mZn dư → mCu = 10,53+ 7,76 - 0,08.108 – 0,05.65 = 6,4 gam
Cho V lít hỗn hợp khí (ở đktc) gồm CO và H2 phản ứng với một lượng dư hỗn hợp rắn gồm CuO và Fe3O4 nung nóng. Sau khi các phản ứng xảy ra hoàn toàn, khối lượng hỗn hợp rắn giảm 0,32 gam. Giá trị của V là
Phản ứng tổng quát: Oxit + hỗn hợp H2 và CO
${H_2} + {{\text{[}}O]_{{\text{ox}}it}}\xrightarrow{{{t^ \circ }}}\,\,{H_2}O\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,CO + {{\text{[}}O]_{{\text{ox}}it}}\xrightarrow{{{t^ \circ }}}\,\,C{O_2}$
Nhận xét: Khối lượng chất rắn giảm chính là do ${{\text{[}}O]_{{\text{ox}}it}}$ tham gia phản ứng
$ \to \sum {{n_{{{{\text{[}}O]}_{{\text{ox}}it}}}}} $phản ứng $ = \dfrac{{0,32}}{{16}} = 0,02\,mol\,\,\,\,$
$\xrightarrow{{Theo\,PTHH}}\,\sum {{n_{{{{\text{[}}O]}_{{\text{ox}}it}}}}} = {n_{{H_2}}} + {n_{CO}} = 0,02\,mol \to {V_{hh}} = 0,02.22,4 = 0,448\,\,(l)$
Khử hoàn toàn m gam oxit MxOy cần vừa đủ 17,92 lít khí CO (đktc), thu được a gam kim loại M. Hoà tan hết a gam M bằng dung dịch H2SO4 đặc nóng (dư), thu được 20,16 lít khí SO2 (sản phẩm khử duy nhất, ở đktc). Oxit MxOy là
nO = nCO = 0,8 mol ; ${n_{S{O_2}}} = 0,9\,mol$
Nhìn vào đáp án thấy số oxi hóa cao nhất của Fe, Cr là +3
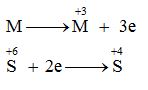
→ ${n_M}\, = \dfrac{{0,9.2}}{3} = 0,6\,mol$
$ \to \dfrac{{{n_M}}}{{{n_O}}} = \dfrac{{0,6}}{{0,8}} = \dfrac{3}{4}$ →MxOy là Fe3O4
Cho hơi nước đi qua than nóng đỏ, thu được 15,68 lít hỗn hợp khí X (đktc) gồm CO, CO2 và H2. Cho toàn bộ X tác dụng hết với CuO (dư) nung nóng, thu được hỗn hợp chất rắn Y. Hoà tan toàn bộ Y bằng dung dịch HNO3 (loãng, dư) được 8,96 lít NO (sản phẩm khử duy nhất, ở đktc). Phần trăm thể tích khí CO trong X là
${n_{NO}} = 0,4\,mol;\,{n_{hh\,X}} = 0,7\,mol$
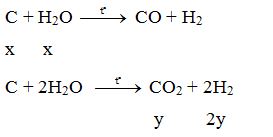
Cách 1: Nhận xét: Số oxi hoá của Cu ban đầu trong oxit và sau trong muối không đổi, ta quy bài toán về dạng:
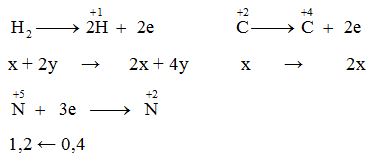
$ \to \left\{ \begin{gathered}{n_{hh\,X}}\, = x + x + y + 2y = 0,7 \hfill \\\xrightarrow{{BT\,\,\,\,electron}}2{\text{x}} + 4y + 2{\text{x}} = 1,2 \hfill \\ \end{gathered} \right.\,\,\, \to \,\,\,\left\{ \begin{gathered}x = 0,2 \hfill \\y = 0,1 \hfill \\ \end{gathered} \right.\,\,\, \to \,\,\,\% {V_{{\text{CO}}}}\,\, = \,\,\,\dfrac{{0,2}}{{0,7}}.100\% \,\, = \,\,28,57\% $
Cách 2:
$C + {H_2}O \to \left\{ \begin{gathered}{n_{CO}} = x\,mol \hfill \\{n_{{H_{_2}}}} = y\,mol \hfill \\{n_{C{O_2}}} = z\,mol \hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered}x + y + z = 0,7 \hfill \\x + y = {n_O} = \dfrac{{{n_e}}}{2} = \dfrac{{0,4.3}}{2} = 0,6 \hfill \\BTNT\,\,O:\,y = x + 2z \hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered}x = 0,2 \hfill \\y = 0,4 \hfill \\z = 0,1 \hfill \\ \end{gathered} \right.$
→ $\,\% {V_{{\text{CO}}}}\,\, = \,\,\,\dfrac{{0,2}}{{0,7}}.100\% \,\, = \,\,28,57\% $
Phát biểu nào sau đây sai?
A đúng, vì Zn bị phá hủy do phản ứng: Zn + 2HCl → ZnCl2 + H2
B đúng, vì thành phần chính của quặng boxit là Al2O3 được dùng để điều chế Al:
2Al2O3 \(\xrightarrow[{criolit}]{{dpnc}}\) 4Al + 3O2
C đúng, PTHH: 2Fe + 3Cl2 \(\xrightarrow{{{t^0}}}\) 2FeCl3
D sai, tính khử của Ag yếu hơn Cu
Cho 6 kim loại sau: Na, Ba, Fe, Ag, Mg, Al lần lượt vào dung dịch CuSO4 dư. Số trường hợp thu được chất sản phẩm là kết tủa sau phản ứng là
- Na + H2O → NaOH + H2; 2NaOH + CuSO4 → Na2SO4 + Cu(OH)2 ↓
⟹ sau phản ứng có kết tủa Cu(OH)2
- Ba + 2H2O → Ba(OH)2 + H2; Ba(OH)2 + CuSO4 → BaSO4 ↓ + Cu(OH)2 ↓
⟹ sau phản ứng có kết tủa Cu(OH)2 và BaSO4
- Fe + CuSO4 → FeSO4 + Cu ↓ ⟹ tạo kết tủa Cu
- Ag không phản ứng
- Mg + CuSO4 → MgSO4 + Cu ⟹ tạo kết tủa Cu
- 2Al + 3CuSO4 → Al2(SO4)3 + 3Cu ⟹ tạo kết tủa Cu
⟹ Các chất phản ứng với CuSO4 tạo sản phẩm kết tủa là Na, Ba, Fe, Mg, Al ⟹ 5 chất

