Hoà tan hoàn toàn 12,42 gam Al bằng dung dịch HNO3 loãng (dư), thu được dung dịch X và 1,344 lít (ở đktc) hỗn hợp khí Y gồm 2 khí là N2O và N2. Tỉ khối của hỗn hợp khí Y so với khí H2 là 18. Cô cạn dung dịch X, thu được m gam chất rắn khan. Giá trị của m là
Trả lời bởi giáo viên
${n_{Al}} = 0,46mol\,;\,{n_Y} = 0,06\,mol$
Đặt ${n_{{N_2}}} = x\,mol\,\,;\,\,{n_{{N_2}O}} = y\,\,mol$
$\left\{ \begin{gathered}x + y = 0,06 \hfill \\28x + 44y = 0,06.18.2 \hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered}x = 0,03 \hfill \\y = 0,03 \hfill \\ \end{gathered} \right.$
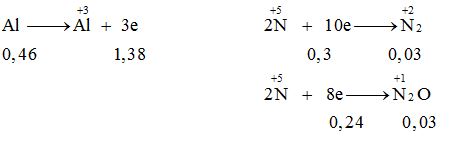
Ta thấy $3{n_{Al}} > (8{n_{{N_2}O}} + 10{n_{{N_2}}})$ → Có muối amoni NH4NO3
Áp dụng định luật bảo toàn e ta có:
$3{n_{Al}} = 8{n_{{N_2}O}} + 10{n_{{N_2}}} + 8{n_{NH_4^ + }} \to {n_{NH_4^ + }} = \dfrac{{0,46.3 - 0,54}}{8} = 0,105mol$
$ \to m = {m_{Al{{(N{O_3})}_3}}} + {m_{N{H_4}N{O_3}}} = 0,46.213 + 0,105.80 = 106,38g$
Hướng dẫn giải:
+) Tính số mol N2O và N2
+) $3{n_{Al}} > (8{n_{{N_2}O}} + 10{n_{{N_2}}})$ → Có muối amoni NH4NO3
+) Bảo toàn e : $3{n_{Al}} = 8{n_{{N_2}O}} + 10{n_{{N_2}}} + 8{n_{NH_4^ + }} \to {n_{NH_4^ + }}$
$ \to m = {m_{Al{{(N{O_3})}_3}}} + {m_{N{H_4}N{O_3}}}$

