Một mẫu nước cứng chứa các ion : Mg2+ , Ca2+ , Cl- , SO42-. Chất được dùng để làm mềm mẫu nước cứng trên là
Chất được dùng để làm mềm mẫu nước cứng trên là Na3PO4 :
Mg2+ + PO43- → Mg3(PO4)2↓
Ca2+ + PO43- → Ca3(PO4)2↓
Phương pháp nào sau đây không sử dụng để làm mềm nước có tính cứng vĩnh cửu?
Nước có tính cứng vĩnh cửu chứa các ion Mg2+, Ca2+, Cl-, SO42-.
Do vậy phương pháp đun sôi nước KHÔNG thể làm mất tính cứng của nước. Phải dùng các phương pháp như: dùng Na3PO4, Na2CO3 để kết tủa hết ion Mg2+, Ca2+ và dùng phương pháp trao đổi ion để làm mêm nước cứng
Nước cứng là nước có chứa nhiều các ion
Nước cứng là nước có chứa nhiều các ion Ca2+, Mg2+.
Chất làm mềm nước có tính cứng toàn phần là
Nước có tính cứng toàn phần là nước có chứa nhiều ion Mg2+, Ca2+, Cl-, SO42- → dùng Na2CO3 để kết tủa hết ion Mg2+, Ca2+ sẽ làm mềm được nước cứng
Mg2+ + CO32- → MgCO3↓
Ca2+ + CO32- → CaCO3↓
Tác hại nào sau đây do nước cứng gây ra?
Tác hại do nước cứng gây ra là làm giảm mùi vị thức ăn khi nấu.
Đáp án: B
Chất nào sau đây được dùng để làm mềm nước cứng vĩnh cửu?
Để làm mềm nước cứng vĩnh cửu ta cần dùng chất có khả năng kết tủa hết Ca2+, Mg2+ ⟹ chọn Na2CO3
Ca2+ + CO32- → CaCO3 ↓
Mg2+ + CO32- → MgCO3 ↓
Để làm sạch lớp cặn trong các dụng cụ đun và chứa nước nóng, người ta thường dùng:
Để làm sạch lớp cặn trong ống đun thường là CaCO3 người ta thường sử dụng giấm ăn
CaCO3 + 2 CH3COOH → (CH3COO)2Ca + H2O
Cho mẫu nước cứng chứa các ion: Ca2+; Mg2+; HCO3-. Hóa chất được dùng để làm mềm mẫu nước cứng trên là
Để làm mềm nước cứng ta cần kết tủa hết ion Ca2+ và Mg2+ ⟹ dùng Na2CO3
Ca2+ + CO32- → CaCO3 ↓
Mg2+ + CO32- → MgCO3 ↓
Nước chứa nhóm ion nào sau đây được gọi là nước cứng toàn phần?
Cốc nước chứa Ca2+ và Mg2+ cùng với thành phần của nước cứng vĩnh cửu (Cl-, SO42-) và thành phần của nước cứng tạm thời (HCO3-) là nước cứng toàn phần.
Nước chứa nhiều ion Ca2+ , Mg2+ thì nước đó thuộc loại
Nước chứa nhiều ion Ca2+ , Mg2+ là nước cứng.
Một dung dịch chứa Ca(HCO3)2. Dung dịch đó thuộc loại?
Dung dịch chứa Ca(HCO3)2 thì dung dịch đó thuộc loại nước cứng tạm thời.
Một dung dịch chứa ion: Ca2+, Mg2+, Cl-, SO42-. Dung dịch đó thuộc loại?
Nước chứa Ca2+, Mg2+, Cl-, SO42- thuộc loại nước vĩnh cửu.
Nước cứng toàn phần là nước chứa?
Nước cứng toàn phần là nước chứa Mg2+, Ca2+, Cl-, SO42-, HCO3- .
Trong các khẳng định sau, khẳng định sai là
Nguyên tắc làm mềm nước cứng: giảm nồng độ ion Ca2+ và ion Mg2+ => C sai
Trong một bể nước gia đình, người ta xử lí nước cứng vĩnh cửu bằng cách cho Ca(OH)2 vào bể nước. Biết rằng khi trích mẫu thử nghiên cứu thì người ta phân tích được trong nước có nồng độ các ion Ca2+ 0,004M; Mg2+ 0,003M và HCO3-. Thể tích dung dịch Ca(OH)2 0,02M vừa đủ để xử lí bể nước có thể tích 1000 lít nước cứng thành nước mềm là V lít. Coi như các phản ứng xảy ra hoàn toàn và kết tủa thu được gồm CaCO3 và Mg(OH)2. Giá trị của V là
- Xét 1 lít nước cứng cần xử lí ta có: nCa2+ = 0,004 mol và nMg2+ = 0,003 mol.
- Giả sử số mol Ca(OH)2 cần dùng vừa đủ để xử lí 1 lít nước cứng là x (mol).
Ta có: \({n_{C{a^{2 + }}}} = x + 0,004;{n_{O{H^ - }}} = 2x;{n_{M{g^{2 + }}}} = 0,003\)
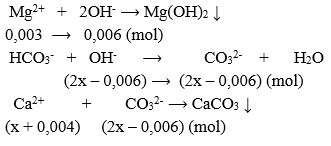
- Lượng Ca(OH)2 cần dùng vừa đủ
⟹ \({n_{C{a^{2 + }}}} = {n_{C{O_3}^{2 - }}} \Rightarrow x + 0,004 = 2x - 0,006 \Rightarrow x = 0,01(mol)\)
- Ta có thể tích dung dịch Ca(OH)2 cần dùng vừa đủ để xử lí 1 lít nước cứng là V(1) = 0,01/0,02 = 0,5 lít.
Vậy thể tích dung dịch Ca(OH)2 cần dùng vừa đủ để xử lí 1000 lít nước cứng là V = 0,5.1000 = 500 lít.
Chất nào sau đây làm mềm nước cứng vĩnh cửu ?
Nước cứng vĩnh cửu là nước chứa ion: Mg2+, Ca2+, Cl-, SO42-.
Làm mềm nước cứng là loại bỏ ion Mg2+, Ca2+.
HCl, CaCl2, Ca(HCO3)2 không làm kết tủa được Mg2+, Ca2+ => loại A, B, C
K2CO3 → 2K+ + CO32-
CO32- + Mg2+ → MgCO3↓
CO32- + Ca2+ → Ca CO3↓
=> Loại bỏ được ion Mg2+, Ca2+
Trong một cốc nước có chứa 0,01 mol K+, 0,02 mol Ca2+; 0,01 mol Mg2+; 0,05 mol HCO3- và anion X-. Đun nóng cốc đến khối lượng không đổi thu được 3,64 gam chất rắn. Nước trong cốc thuộc loại
- Trong một cốc nước có chứa 0,01 mol K+, 0,02 mol Ca2+; 0,01 mol Mg2+; 0,05 mol HCO3- và anion X-.
- Áp dụng định luật bảo toàn điện tích ⟹ nX- = 0,01.1 + 0,02.2 + 0,01.2 – 0,05.1 = 0,02 mol.
- Xét khi đun nóng cốc nước:
Theo PTHH: 2HCO3-\(\xrightarrow{{{t^0}}}\) CO32- + CO2 ↑ + H2O
⟹ \({n_{C{O_3}^{2 - }}} = \dfrac{{{n_{HC{O_3}^ - }}}}{2} = 0,025(mol)\)
- Sau đun nóng đến khối lượng không đổi trong cốc còn lại các ion 0,01 mol K+, 0,02 mol Ca2+; 0,01 mol Mg2+; 0,025 mol CO32- và 0,02 mol X-.
Ta có: mc/rắn = 0,01.39 + 0,02.40 + 0,01.24 + 0,025.60 + 0,02.MX = 3,64 ⟹ MX = 35,5 (anion là Cl-).
Vậy nước trong cốc chứa các ion Ca2+, Mg2+, Cl- thuộc loại nước cứng toàn phần.
Chất nào sau đây không làm mềm được nước cứng tạm thời ?
Nước cứng tạm thời chứa các ion Mg2+, Ca2+, HCO3-
=> Có thể làm mềm bằng NaOH, Ca(OH)2 hoặc Na2CO3
Một loại mẫu nước cứng có chứa các ion Ca2+, Mg2+, HCO3-, Cl-, SO42-. Chất được dùng để làm mềm mẫu nước cứng trên là
Để làm mềm mẫu nước cứng trên ta có thể dùng Na3PO4 vì PO43- kết tủa hết Ca2+ và Mg2+:
3Ca2+ + 2PO43- → Ca3(PO4)2 ↓
3Mg2+ + 2PO43- → Mg3(PO4)2 ↓
Nếu đun sôi nước cứng tạm thời sẽ thấy hiện tượng?
Mg(HCO3)2 \(\buildrel {{t^0}} \over
\longrightarrow \) MgCO3 ↓+ CO2 + H2O
Ca(HCO3)2 \(\buildrel {{t^0}} \over
\longrightarrow \) CaCO3 ↓+ CO2 + H2O
=> Hiện tượng là có khí CO2 bay ra và xuất hiện kết tủa của các ion Ca2+ và Mg2+

