Trong một bể nước gia đình, người ta xử lí nước cứng vĩnh cửu bằng cách cho Ca(OH)2 vào bể nước. Biết rằng khi trích mẫu thử nghiên cứu thì người ta phân tích được trong nước có nồng độ các ion Ca2+ 0,004M; Mg2+ 0,003M và HCO3-. Thể tích dung dịch Ca(OH)2 0,02M vừa đủ để xử lí bể nước có thể tích 1000 lít nước cứng thành nước mềm là V lít. Coi như các phản ứng xảy ra hoàn toàn và kết tủa thu được gồm CaCO3 và Mg(OH)2. Giá trị của V là
Trả lời bởi giáo viên
- Xét 1 lít nước cứng cần xử lí ta có: nCa2+ = 0,004 mol và nMg2+ = 0,003 mol.
- Giả sử số mol Ca(OH)2 cần dùng vừa đủ để xử lí 1 lít nước cứng là x (mol).
Ta có: \({n_{C{a^{2 + }}}} = x + 0,004;{n_{O{H^ - }}} = 2x;{n_{M{g^{2 + }}}} = 0,003\)
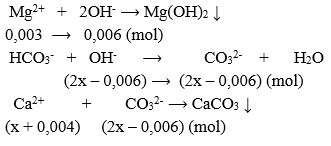
- Lượng Ca(OH)2 cần dùng vừa đủ
⟹ \({n_{C{a^{2 + }}}} = {n_{C{O_3}^{2 - }}} \Rightarrow x + 0,004 = 2x - 0,006 \Rightarrow x = 0,01(mol)\)
- Ta có thể tích dung dịch Ca(OH)2 cần dùng vừa đủ để xử lí 1 lít nước cứng là V(1) = 0,01/0,02 = 0,5 lít.
Vậy thể tích dung dịch Ca(OH)2 cần dùng vừa đủ để xử lí 1000 lít nước cứng là V = 0,5.1000 = 500 lít.
Hướng dẫn giải:
- Xét 1 lít nước cứng cần xử lí ⟹ số mol Ca2+ và Mg2+ trong nước cứng.
- Giả sử số mol Ca(OH)2 cần dùng vừa đủ để xử lí 1 lít nước cứng là x (mol).

