Hấp thụ hết 2,24 mol CO2 vào dung dịch chứa 100ml NaOH 0,5M và 100 ml Ca(OH)2 0,5M, kết thúc các phản ứng thu được m gam kết tủa. Giá trị của m là
nOH- = 0,15 mol ; nCO2 = 0,1 mol => nCO2 < nOH- < 2.nCO2
=> nCO3 = nOH – nCO2 = 0,05 mol
Vì nCO3 < nCa2+ => nCaCO3 = nCO3 = 0,05 mol
=> mkết tủa = 5 gam
Hấp thụ hết 2,24 lít CO2 vào dung dịch chứa 100ml NaOH 0,5M và 100 ml Ca(OH)2 0,5M, kết thúc các phản ứng thu được m gam kết tủa. Giá trị của m là
nOH- = 0,15 mol ; nCO2 = 0,1 mol => nCO2 < nOH- < 2.nCO2
=> nCO3 = nOH – nCO2 = 0,05 mol
Vì nCO3 < nCa2+ => nCaCO3 = nCO3 = 0,05 mol
=> mkết tủa = 5 gam
Hấp thụ hoàn toàn 1,12 lít khí CO2 (đktc) vào 100 ml dung dịch gồm NaOH 0,8M và KOH 0,5M thu được dung dịch X. Cô cạn toàn bộ dung dịch X thu được bao nhiêu gam chất rắn khan ?
nCO2 = 0,05 mol; nOH = nNaOH + nKOH = 0,08+0,05= 0,13 mol > 2nCO2
=> OH- dư
=> nCO3 = nCO2 = 0,05 mol
Và nOH- dư = nOH- ban đầu – nOH- phản ứng = nOH- ban đầu -2nCO2−3 = 0,03 mol
=> mrắn = mNa + mK + mCO3 + mOH dư = 7,3 gam
Sục từ từ V lít khí CO2 (đktc) từ từ vào 100 ml dung dịch hỗn hợp NaOH 2M; KOH 2M và Ba(OH)2 3 M. Kết thúc phản ứng thu được 39,4 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị lớn nhất của V thỏa mãn điều kiện của bài toán là
V lớn nhất khi có hiện tượng hòa tan kết tủa => thuộc trường hợp nCO2 < nOH- < 2.nCO2
nOH = nNaOH + nKOH + 2nBa(OH)2 = 1 mol
nBaCO3 = 0,2 mol < nBa2+ = 0,3 mol => CO32- tạo hết thành kết tủa
=> nCO2 = nOH – nBaCO3 = 1-0,2 = 0,8 mol
=> V = 17,92 lit
Hấp thụ hoàn toàn 4,48 lít khí CO2 (đktc) vào 100 ml dung dịch KOH 5M thu được dung dịch X. Cho từ từ dung dịch HCl 1M vào X đến khi bắt đầu có khí sinh ra thì hết V ml. Giá trị của V là
nCO2 = 0,2 mol; nKOH = 0,5 mol > 2nCO2 => OH- dư
=> dung dịch sau phản ứng gồm K2CO3 0,2 mol và KOH dư = 0,5- 0,2.2 = 0,1 mol
Nhỏ từ từ HCl đến khi có khí thì dừng, có các phản ứng sau :
HCl + KOH → KCl + H2O
K2CO3 + HCl → KHCO3 + KCl
=> nHCl = nKOH + nK2CO3 = 0,1+0,2 = 0,3 mol
=> V = 300 ml
Sục từ từ V lít khí CO2 (đktc) từ từ vào 100 ml dung dịch hỗn hợp NaOH 2M; KOH 2M và Ba(OH)2 3 M. Kết thúc phản ứng thu được dung dịch chứa 62,7 gam muối. Biết các phản ứng xảy ra hoàn toàn. Giá trị lớn nhất của V thỏa mãn điều kiện của bài toán là
Xét dung dịch chứa : x mol Ba2+ ; 0,2 mol K+ ; 0,2 mol Na+ và HCO3-
Bảo toàn điện tích :nHCO−3= 0,4 + 2x mol
=> mmuối = mBa2+ + mK+ + mNa+ +nHCO−3= 62,7 gam => x = 0,1 mol => nBaCO3 = 0,3 – 0,1 = 0,2 mol
+) Bảo toàn C : nCO2 =nCO23− +nHCO−3 = 0,8 mol
=> VCO2 = 17,92 lít
Sục khí CO2 từ từ cho đến dư vào 200 ml dung dịch hỗn hợp NaOH 2M và Ca(OH)2 1M thu được dung dịch A. Cô cạn dung dịch A rồi nhiệt phân đến khối lượng không đổi thu được m gam chất rắn. Các phản ứng xảy ra hoàn toàn. Giá trị của m là
CO2 đến dư thì dung dịch gồm 0,4 mol NaHCO3 và 0,2 mol Ca(HCO3)2
Khi nhiệt phân hoàn toàn thu được : 0,2 mol Na2CO3 và 0,2 mol CaO
=> m = 32,4 gam
Hấp thụ hoàn toàn 3,92 lít CO2 (đktc) vào V ml dung dịch chứa NaOH 2M và K2CO3 1,25 M. Cô cạn cẩn thận 32,5 dung dịch sau phản ứng ở nhiệt độ thường thu được gam chất rắn khan gồm 4 muối. Giá trị của V là
Vì phản ứng tạo 4 muối => có tạo x mol CO32- và y mol HCO3-
=> mrắn = mNa + mK + mCO3 + mHCO3 => 32,5 = 23.2.V+ 1,25.2.39V + 60x + 61y (1)
Bảo toàn điện tích : nNa++nK+=2.nCO2−3+nHCO−3 => 2.V + 2.1,25V = 2x + y (2)
Bảo toàn C : nCO2 + nK2CO3 = x + y = 0,175 + 1,25V (3)
Từ (1), (2) và (3) ta có : V = 0,1 lít = 100 ml
Hấp thụ hoàn toàn V lít CO2 (đktc) vào bình đựng 100 ml dung dịch NaOH 4M và Na2CO3 1M. Cô cạn dung dịch sau phản ứng ở nhiệt độ thường thu được 29,2 gam chất rắn khan. Giá trị của V là :
nNaOH = 0,4 mol ; nNa2CO3 = 0,1 mol
TH1: Giả sử CO2 phản ứng hết , sau phản ứng thu được NaHCO3 và Na2CO3
Đặt nNaHCO3 = a mol
Bảo toàn nguyên tử Na: nNa+ trước phản ứng = nNaHCO3 + 2.nNa2CO3 => nNa2CO3 = 0,3 – 0,5a mol
=> mrắn = 84a + 106.(0,3 – 0,5a) = 29,2 (loại vì a < 0)
TH2: Giả sử CO2 hết, NaOH dư => sau phản ứng thu được Na2CO3 (x mol) và NaOH dư (y mol)
Bảo toàn Na: nNa+ trước phản ứng = 2.nNa2CO3 + nNaOH dư => 2x + y = 0,6 (1)
mrắn khan = mNa2CO3 + mNaOH => 106x + 40y = 29,2 (2)
Từ (1) và (2) => x = 0,2 mol; y = 0,2 mol
Bảo toàn C: nCO2 + nNa2CO3 phản ứng = nNa2CO3 sau phản ứng
=> nCO2 = 0,2 – 0,1 = 0,1 mol => V = 2,24 lít
Dẫn từ từ 10,08 lít CO2 (đktc) vào 100 ml dung dịch chứa đồng thời các chất NaOH 2 M; KOH 1M; Na2CO3 1M; K2CO3 1M thu được dung dịch X. Thêm dung dịch CaCl2 dư vào dung dịch X, số gam kết tủa thu được là:
nCO2 = 0,45 mol; nNaOH = 0,2 mol; nKOH = 0,1 mol; nNa2CO3 = 0,1 mol; nK2CO3 = 0,1 mol
=> nCO3 = 0,2 mol ; nOH = 0,3 mol
Vì nOH- < nCO2 => CO2 phản ứng với OH- tạo HCO3-
CO2 + OH- → HCO3-
0,3 ← 0,3
CO2 + CO32- + H2O → 2HCO3-
0,15 → 0,15
=> nCO3 = 0,2 – 0,15 = 0,05 mol
=> nCaCO3 = nCO3 = 0,05 => mCaCO3 = 5g
Sục 6,72 lít CO2 (đktc) vào 100 ml dung dịch X gồm Ca(OH)2 1M và NaOH 2M. Sau phản ứng thu được m1 gam kết tủa và dung dịch X. Cho dung dịch X tác dụng với 100 ml dung dịch CaCl2 1M; KOH 0,5M thu được m2 gam kết tủa. Giá trị của m2 là:
nOH- = 0,4
có nCO2 = 0,3 < nOH- < 2.nCO2 => tạo 2 muối HCO3- (x mol) và CO32- (y mol)
Bảo toàn C: nCO2 = nHCO3 + nCO3 => x + y = 0,3
Bảo toàn điện tích: nOH- = nHCO3 + 2.nCO3 => x + 2y = 0.4
=> x = 0,2 và y = 0,1
Vì nCO3 = y = 0,1 = nCa2+ = 0,1 => sau phản ứng CO32- hết
=> dung dịch X gồm: 0,2 mol HCO3-; 0,2 mol Na+
nCaCl2 = 0,1 = nCa2+
HCO3- + OH- → CO32- + H2O
0,05 ← 0,05 → 0,05
=> nCO3 = 0,05 < nCa2+ = 0,1 => nCaCO3 = 0,05
=> m2 = 0,05.100 = 5 gam
Hấp thụ hoàn toàn 22,4 lít khí CO2 (đktc) vào dung dịch chứa y mol Ba(OH)2, x mol KOH, x mol NaOH. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch chứa 81,1 gam muối và 39,4 gam kết tủa. Bỏ qua sự thủy phân của các ion. Tỉ lệ x : y có thể là
nCO2 = 1 mol; nBaCO3 = 0,2 mol
Giả sử muối chứa Ba(HCO3)2
=> dung dịch thu được gồm K+ (x mol); Na+ (x mol); Ba2+ và HCO3- (a mol)
Bảo toàn điện tích: nBa2+ = 0,5a – 0,5x – 0,5x= 0,5a -x
Bảo toàn nguyên tố C: nCO2 = nHCO3 + nBaCO3 => 1 = a + 0,2 => a = 0,8 (1)
Bảo toàn nguyên tố Ba: nBa(OH)2 = nBa2+ + nBaCO3 => y = 0,5a – x + 0,2 (2)
mmuối = mK+ + mNa+ + mBa2+ + mHCO3- => 39x + 23x + 137.(0,5a - x) + 61a = 81,1 (3)
Từ (1), (2) và (3) => a = 0,8; x = 0,3; y = 0,3
=> x : y = 1 : 1
Hấp thụ hoàn toàn V lít CO2 vào dung dịch Ca(OH)2 a M thì thu được m1 gam kết tủa. Nếu hấp thụ (V +1,12 ) lít CO2 vào dung dịch Ca(OH)2 trên thì thu được m2 gam kết tủa. Nếu thêm (V + V1) lít CO2 vào dung dịch Ca(OH)2 đã cho thì thu được lượng kết tủa cực đại. Biết m1 : m2 = 2 : 1; m1 bằng 1/2 khối lượng kết tủa cực đại, các khí đều ở đktc. Giá trị của V1 là
Ta thấy lượng 0,05 mol CO2 đưa vào làm 2 nhiệm vụ :
+) Đưa kết tủa từ m1 lên cực đại
+) Đưa kết tủa từ cực đại đến m2
Từ : m1 = 2m2 và m1 = 1/2mmax
=> ta có : n CO2 thêm = mmax
<=> 0,05 = \frac{{{m_{\max }} - {m_1} + {m_{\max }} - {m_2}}}{{100}} = \frac{{2{m_1} - {m_1} + 2{m_1} - 1/2{m_1}}}{{100}}=> \left\{ \begin{array}{l}{m_1} = 2gam\\{m_2} = 1gam\end{array} \right.
=> nCaCO3 max = 0,04 mol
Nếu hấp thụ V lít CO2 thì Ca(OH)2 còn dư => nCO2 = n = nCaCO3 (m1) = 0,02 mol
=> n1 = 0,02 mol => V1 = 0,448 lít
Hấp thụ hết 7,84 lít CO2 (đktc) vào dung dịch chứa x mol KOH và y mol K2CO3 thu được 200 ml dung dịch X. Lấy 100 ml dung dịch X cho từ từ vào 100 ml dung dịch HCl 2M, thu được 3,36 lít khí (đktc). Mặt khác, 100 ml dung dịch X tác dụng với dung dịch Ba(OH)2 dư thu được 39,4 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của x là
nCO2 bđ = 0,35 mol
100 ml X + Ba(OH)2 => nBaCO3 = nC(X) = 0,2 mol
=> Trong 200 ml X có 0,4 mol C => Bảo toàn C : nCO2 bđ + nK2CO3 = nC(X)
=> nK2CO3 = y = 0,05 mol
Giả sử trong 100 ml X có a mol K2CO3 và b mol KHCO3 (a + b = 0,2 mol)
Cho từ từ X vào nHCl = 0,2 mol tạo nCO2 = 0,15 mol
=> K2CO3 và KHCO3 phản ứng đồng thời (vì HCl lúc đầu dư) theo tỉ lệ mol a : b
Gọi nK2CO3 pứ = ax và nKHCO3 pứ = bx
=> 2ax + bx = nHCl = 0,2 mol ; ax + bx = nCO2 = 0,15 mol
=> ax = 0,05 và bx = 0,1 mol
=> a : b = 1 : 2
=> a = 0,05 ; b = 0,15 mol
=> Bảo toàn K : x + 2y = 2.(2a + b)
=> x = 0,4 mol
Sục từ từ khí CO2 đến dư vào dung dịch gồm (a) mol NaOH và (b) mol Ca(OH)2. Sự phụ thuộc của số mol kết tủa CaCO3 vào số mol CO2 được biểu diễn theo đồ thị sau:
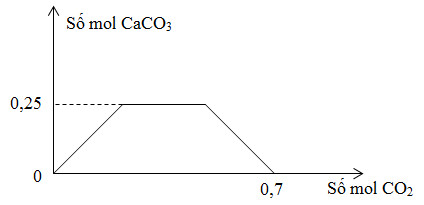
Tỉ lệ (a : b) tương ứng là
+ nCaCO3 max = nCa(OH)2 = b = 0,25 mol
+ Tại nCO2 = 0,7 mol: Phản ứng tạo Ca(HCO3)2 và NaHCO3
BTNT "Ca": nCa(HCO3)2 = nCa(OH)2 = 0,25 mol
BTNT "C": nCO2 = 2nCa(HCO3)2 + nNaHCO3 => 0,7 = 2.0,25 + nNaHCO3 => nNaHCO3 = 0,2 mol
BTNT "Na": nNaOH = nNaHCO3 = a = 0,2 mol
=> a : b = 0,2 : 0,25 = 4 : 5
Sục CO2 vào 200 gam dung dịch Ca(OH)2, kết quả thí nghiệm được biểu diễn bằng đồ thị sau :
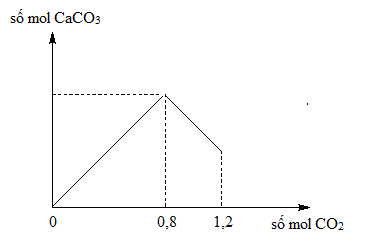
Nồng độ % chất tan trong dung dịch sau phản ứng là
Tại thời điểm kết tủa lớn nhất Ca(OH)2 + CO2 → CaCO3 + H2O
→ nCa(OH)2 = nCO2 = 0,8 mol
Tại thời điểm CO2 : 1,2 mol thì CaCO3 + CO2 + H2O → Ca(HCO3)2
Ban đầu : 0,8 mol 0,4
Sau Pư 0,4 0 0,4
Bảo toàn khối lượng mdd sau pư = 1,2.44 + 200 – 0,4 .100 =212,8 gam
\to \% Ca{(HC{O_3})_2} = \dfrac{{0,4.162}}{{212,8}}.100\% = 30,45\%
Sục từ từ khí CO2 đến dư vào dung dịch gồm a mol NaOH và b mol Ca(OH)2. Sự phụ thuộc của số mol kết tủa CaCO3 vào số mol CO2 được biểu diễn theo đồ thị sau :
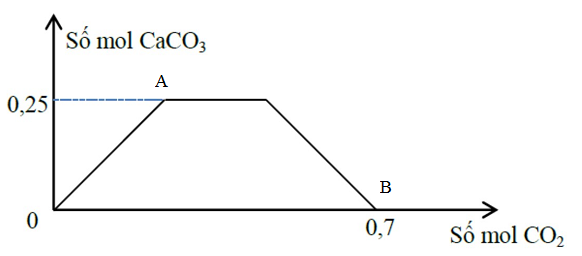
Tỉ lệ a : b tương ứng là :
Tại điểm A: ↓ đạt max: nCO3(2-) = nCO2 = nCa(OH)2 = 0,25 mol → b = 0,25 mol
Tại điểm B: ↓ tan hoàn toàn
Khi số mol kết tủa cực tiểu thì: nOH-/ nCO2 = 1 → nOH- = nCO2 = 0,7 mol
Mặt khác: nOH- = a + 2b = 0,7 mol suy ra a = 0,7-2b = 0,7- 2.0,25 = 0,2 mol
Vậy a : b = 0,2 : 0,25 = 4 : 5
Cho m gam hỗn hợp Na và Ba vào nước dư, thu được dung dịch X và V lít khí H2 đktc. Sục khí CO2 từ từ đến dư vào dung dịch X, lượng kết tủa thể hiện trên đồ thị sau
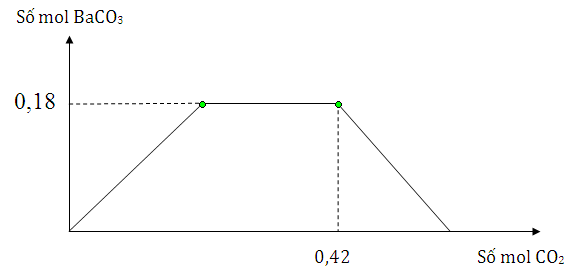
Giá trị của m và V lần lượt là
PTHH: Na + H2O → NaOH + ½ H2
Ba + 2H2O → Ba(OH)2 + H2
Dd X chứa NaOH và Ba(OH)2. Cho CO2 vào dung dịch X xảy ra pư
CO2 + OH- → CO32- + H2O
CO32- + CO2 +H2O → 2HCO3-
Ba2+ + CO32- → BaCO3
Xét đồ thị
nBaCO3 max = 0,18 mol nên nBa = nBaCO3 max = 0,18 mol
Tại thời điểm CO2 là 0,42 mol thì lượng kết tủa bắt đầu giảm dần
→ khi đó sản phẩm chỉ có BaCO3 : 0,18 mol và NaHCO3 : x mol
Bảo toàn C có 0,42 = 0,18 + x nên x = 0,24 mol
Bảo toàn Na có nNa ban đầu = nNaHCO3 = 0,24 mol → m = mBa + mNa = 0,18.137 + 0,24.23 = 30,18 g
Theo PTHH thì nH2 = ½ . nNa + nBa = ½ . 0,24 + 0,18 = 0,3 mol → V =0,3.22,4 =6,72 lít
Dẫn từ từ đến dư khí CO2 vào dung dịch chứa 0,01 mol Ca(OH)2. Sự phụ thuộc của khối lượng kết tủa (y gam) vào thể tích khí CO2 tham gia phản ứng (x lít) được biểu diễn như đồ thị:
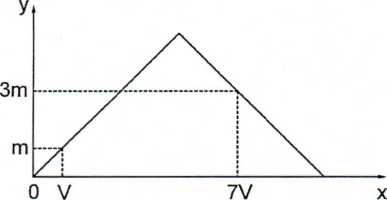
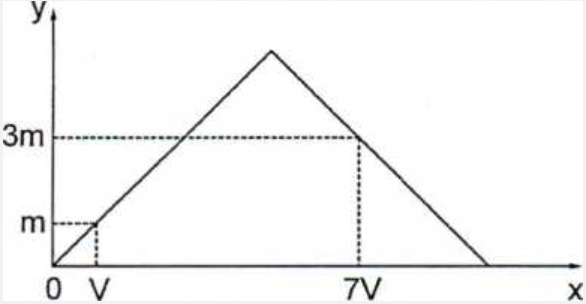
Giá trị của m là
- Khi x = V:
nCO2 = nCaCO3 ⇔ \frac{V}{{22,4}} = \frac{m}{{100}} (1)
- Khi x = 7V:
Ta có: nCaCO3 = \frac{{3m}}{{100}} (mol)
Bảo toàn Ca
→ nCa(HCO3)2 = nCa(OH)2 - nCaCO3 = 0,01 - \frac{{3m}}{{100}} (mol)
Bảo toàn C → nCO2 = nCaCO3 + 2nCa(HCO3)2 ⇔ \frac{{7V}}{{22,4}} = \frac{{3m}}{{100}} + 2.\left( {0,01 - \frac{{3m}}{{100}}} \right)(2)
Giải hệ (1)(2) được:
m = 0,2 và V = 0,0448
Vậy m = 0,2 (g)
Cho từ từ x mol khí CO2 vào 500 gam dung dịch hỗn hợp KOH và Ba(OH)2. Kết quả thí nghiệm được biểu diễn trên đồ thị sau:
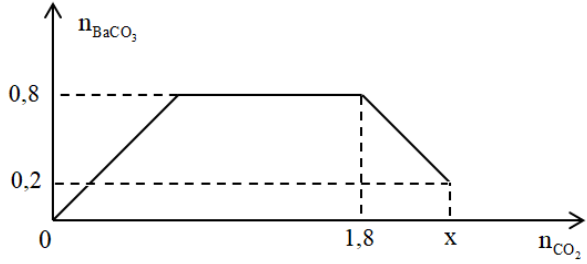
Tổng nồng độ phần trăm khối lượng của các chất tan trong dung dịch sau phản ứng là
Tại điểm A: nkết tủa = nBa2+ = nCO2 = 0,8 mol → nBa(OH)2 = 0,8 mol
Tại điểm B: kết tủa bắt đầu tan:
nCO3(2-) = nOH- - nCO2
⟹ 0,8 = nOH- - 1,8 → nOH- = 2,6 mol → nKOH = 2,6 - 0,8.2 = 1 mol
Tại điểm C: Kết tủa tan 1 phần:
nCO3(2-) = nOH- - nCO2
⟹ 0,2 = 2,6 - nCO2 → nCO2 = 2,4 mol
Dung dịch sau phản ứng có: 0,6 mol Ba2+; 1 mol K+; 2,2 mol HCO3- (áp dụng định luật bảo toàn điện tích)
⟹ mchất tan = 0,6.137 + 1.39 + 2,2.61 = 255,4 gam
Tương tự tìm mdd = mcác chất tham gia pứ - mkết tủa = 2,4.44 + 500 - 0,2.197 = 566,2 (gam)
⟹ C%chất tan = \frac{{255,4}}{{566,2}}.100\% = 45,11%

