Cho các phát biểu sau:
(a) Điện phân dung dịch NaCl với điện cực trơ, thu được khí H2 ở catot
(b) Dùng khí CO dư khử CuO nung nóng, thu được kim loại Cu
(c) Để hợp kim Fe- Ni ngoài không khí ẩm thì kim loại Ni bị ăn mòn điện hóa học
(d) Dùng dung dịch Fe2(SO4)3 dư có thể tách Ag ra khỏi hỗn hợp Ag và Cu
(e) Cho Fe dư vào dung dịch AgNO3 sau phản ứng thu được dung dịch chứa hai muối
Số phát biểu đúng là
(a) Đúng vì tại catot (-) có 2H2O + 2e → 2OH- + H2
(b) Đúng
(c) Sai vì Fe mạnh hơn Ni trong dãy điện hóa nên xảy ra ăn mòn Fe
(d) Đúng vì Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4 → tách Ag ra khỏi hỗn hợp Ag và Cu
(e) Sai vì chỉ tạo muối Fe(NO3)2
Hòa tan hoàn toàn 2 chất rắn X, Y (có số mol bằng nhau) vào nước thu được dung dịch Z. Tiến hành các thí nghiệm sau:
Thí nghiệm 1: Cho dung dịch NH3 dư vào dung dịch Z thu được x1 mol kết tủa
Thí nghiệm 2: Cho dung dịch Na2CO3 dư vào dung dịch Z thu được x2 mol kết tủa
Thí nghiệm 3: Cho dung dịch Ba(OH)2 dư vào dung dịch Z thu được x3 mol kết tủa.
Biết các phản ứng xảy ra hoàn toàn và x1 < x2 < x3. Hai chất X, Y lần lượt là
Giả sử số mol mỗi chất X, Y là 1 mol.
- Phương án A:
TN1: Kết tủa gồm Fe(OH)2 (1 mol) => x1 = 1
TN2: Kết tủa gồm BaCO3 (1 mol) và FeCO3 (1 mol) => x2 = 2
TN3: Kết tủa gồm Fe(OH)2 (1 mol) => x3 = 1
=> Không thỏa mãn x1 < x2 < x3
- Phương án B:
TN1: Kết tủa gồm 1 mol Al(OH)3 và 1 mol Fe(OH)3 => x1 = 2
TN2: Kết tủa gồm 1 mol Al(OH)3 (do Al2(CO3)3 phân hủy thành) và 1 mol Fe(OH)3 (do Fe2(CO3)3 phân hủy thành) => x2 = 2
TN3: Kết tủa gồm 1 mol Fe(OH)3 => x3 = 1
=> Không thỏa mãn x1 < x2 < x3
- Phương án C:
TN1: Kết tủa gồm 2 mol Al(OH)3 (chú ý Zn(OH)2 tạo phức với NH3 nên bị tan) => x1 = 2
TN2: Kết tủa gồm 1 mol ZnCO3 (1 mol) và 2 mol Al(OH)3 (do Al2(CO3)3 phân hủy thành) => x2 = 3
TN3: Kết tủa gồm 4 mol BaSO4 => x3 = 4
=> Thỏa mãn x1 < x2 < x3
- Phương án D:
TN1: Kết tủa gồm 1 mol Fe(OH)2 và 2 mol Fe(OH)3 => x1 = 3
TN2: Kết tủa gồm 1 mol FeCO3 và 2 mol Fe(OH)3 (do Fe2(CO3)3 phân hủy thành) => x2 = 3
TN3: Kết tủa gồm 1 mol Fe(OH)2; 2 mol Fe(OH)3 và 4 mol BaSO4 => x3 = 7 mol
=> Không thỏa mãn x1 < x2 < x3
Cho hỗn hợp gồm Fe và Cu lần lượt tác dụng với các chất lỏng sau:
(1) dung dịch H2SO4 loãng nguội
(2) khí oxi nung nóng
(3) dung dịch NaOH
(4) dung dịch H2SO4 đặc nguội
(5) dung dịch FeCl3
Số chất chỉ tác dụng với một trong hai kim loại là
(1) dung dịch H2SO4 loãng nguội chỉ tác dụng với Fe
(2) khí oxi nung nóng tác dụng với cả hai
(3) dung dịch NaOH không tác dụng với cả hai
(4) dung dịch H2SO4 đặc nguội chỉ tác dụng với Cu
(5) dung dịch FeCl3 tác dụng với cả 2
Số chất chỉ tác dụng với một trong hai kim loại là (1) và (4) => có 2 chất
Phát biểu nào sau đây sai?
A,B,D đúng
C sai vì chất béo (C17H33COO)3C3H5 ở trạng thái lỏng ở điều kiện thường
Cho các phát biểu sau
(1) Thành phần chính của supephotphat kép gồm hai muối Ca(H2PO4)2 và CaSO4
(2) Al là kim loại có tính lưỡng tính
(3) Để xử lý thủy ngân rơi vãi, người ta có thể dùng bột lưu huỳnh
(4) Khí thoát vào khí quyển, Freon phá hủy tầng ozon
(5) Trong khí quyển, nồng độ NO2 và SO2 vượt quá tiêu chuẩn cho phép gây ra hiện tượng mưa axit
(6) Đám cháy Mg có thể dập tắt bằng CO2
(7) Phèn chua được dùng để làm trong nước đục
(8) Trong tự nhiên, các kim loại kiềm chỉ tồn tại dạng đơn chất
Số phát biểu đúng là
(1) sai vì thành phần chính của supephotphat kép là Ca(H2PO4)2
(2) sai vì không có khái niệm kim loại lưỡng tính
(3) đúng vì S phản ứng với Hg ở đk thường tạo thành HgS là chất rắn an toàn
(4) đúng
(5) đúng vì hai chất này là nguyên nhân gây mưa axit
(6) sai vì 2Mg + CO2 \(\xrightarrow{{{t^0}}}\) 2MgO + C làm phản ứng cháy tiếp tục
(7) đúng, phèn chua có công thức là K2SO4.Al2(SO4)3.24H2O có ứng dụng làm trong nước
(8) sai vì trong tự nhiên kim loại kiềm tồn tại dạng hợp chất
=> có 4 phát biểu đúng
Thực hiện các thí nghiệm sau đến phản ứng xảy ra hoàn toàn:
(a) Dẫn a mol khí CO2 vào 0,8a mol Ca(OH)2 trong dung dịch.
(b) Cho a mol Fe vào 3a mol HNO3 trong dung dịch (sản phẩm khử duy nhất tạo ra là NO)
(c) Cho dung dịch NaHCO3 đến dư vào dung dịch Ba(OH)2.
(d) Cho bột Cu vào dung dịch FeCl3 (dư)
Số thí nghiệm thu được dung dịch chứa hai muối là
(a) ta thấy: \(1 < \frac{{{n_{C{O_2}}}}}{{{n_{Ca{{(OH)}_2}}}}} = \frac{a}{{0,8a}} = 1,25 < 2\) => tạo 2 muối CaCO3 và Ca(HCO3)2. Nhưng CaCO3 không tan nên dd chỉ thu được 1 muối Ca(HCO3)2
(b) nHNO3 = 4nNO => nNO = 0,75a (mol) => ne nhận = 3nNO = 2,25a (mol).
Ta thấy: 2nFe < ne nhận = 2,25a < 3nFe => tạo 2 muối Fe(NO3)2 và Fe(NO3)3
(c) 2NaHCO3 dư + Ba(OH)2 → BaCO3↓ + Na2CO3 + 2H2O => dd thu được 2 muối: Na2CO3 và NaHCO3 dư
(d) Cu + 2FeCl3 dư → 2FeCl2 + CuCl2 => thu được 3 muối: CuCl2, FeCl2 và FeCl3 dư
=> có 2 thí nghiệm (b) và (c) thu được 2 muối
Phát biểu nào sau đây đúng?
A. đúng
B. Sai vì Al nhường 3e, còn Cr chỉ nhường 2e do vậy số mol H2 thu được khác nhau
C. Sai BaO + H2O → Ba(OH)2 ; Ba(OH)2 + Na2CO3 → BaCO3↓ + 2NaOH => thu được BaCO3 kết tủa
D.Sai vì nung AgNO3 cho kim loại Ag chứ không phải oxit
Cho hỗn hợp Cu và Fe2O3 vào dung dịch HCl dư. Sau khi phản ứng xảy ra hoàn toàn, thu được dung dịch X và một lượng chất rắn không tan. Muối trong dung dịch X là
Cu và Fe2O3 tác dụng với HCl có phản ứng
Fe2O3 + 6HCl → 2FeCl3 + 3H2O (1)
Cu + 2FeCl3 → CuCl2 + 2FeCl2 (2)
Vì còn một lượng chất rắn không tan là Cu nên phương trình (2) FeCl3 phản ứng hết.
Vậy muối trong dung dịch X gồm CuCl2 và FeCl2
Hòa tan hỗn hợp X gồm FeO, ZnO, PbO, CuO bằng dung dịch HNO3 dư thu được dung dịch Y. Trung hòa Y bằng NaOH thu được dung dịch Z. Nhỏ từ từ dung dịch Na2S cho tới dư vào dung dịch Z được kết tủa T. Số lượng chất có trong T là
\(\eqalign{
& \left\{ \matrix{
FeO \hfill \cr
ZnO \hfill \cr
PbO \hfill \cr
CuO \hfill \cr} \right. + HN{O_{3\,}}dư \to dd\,Y\left\{ \matrix{
F{e^{3 + }},Z{n^{2 + }},P{b^{2 + }},C{u^{2 + }} \hfill \cr
{H^ + } \hfill \cr
N{O_3}^ - \hfill \cr} \right.\buildrel { + trung\,hòa} \over
\longrightarrow dd\,Z \cr
& dd\,Z\left\{ \matrix{
F{e^{3 + }},Z{n^{2 + }},P{b^{2 + }},C{u^{2 + }} \hfill \cr
N{O_3}^ - \hfill \cr} \right.\buildrel { + N{a_2}S} \over
\longrightarrow T\left\{ {Fe{{(OH)}_3},ZnS,CuS,PbS} \right\} \cr} \)
=> các chất có trong T là 4 chất
Cho các phát biểu sau:
(a) Thép là hợp kim của sắt với cacbon và một số nguyên tố khác, trong đó có từ 0,01-2% khối lượng cacbon.
(b) Bột nhôm trộn với bột Fe2O3 dùng để hàn đường ray bằng phản ứng nhiệt nhôm.
(c) Phèn chua và thạch cao sống có công thức hóa học lần lượt là KAl(SO4)2.12H2O và CaSO4.2H2O.
(d) Thạch cao nung dùng để nặn tượng, bó bột khi gãy xương.
(e) Dung dịch Na2CO3, Na3PO4 làm mềm được nước cứng.
(g) Miếng gang để trong không khí ẩm xảy ra ăn mòn điện hóa.
Số phát biểu đúng là
(a) đúng
(b) đúng, hỗn hợp đó được gọi là hỗn hợp tecmit dùng để hàn đường ray
(c) đúng
(d) đúng, thạch cao nung CaSO4.H2O hoặc CaSO4.0,5H2O được dùng để nặn tượng hoặc bó bột khi gãy xương
(e) đúng
(g) đúng, vì khi đó cặp điện cực Fe-C được tiếp xúc với môi trường điện li là không khí ẩm nên xảy ra ăn mòn điện hóa.
Vậy có tất cả 6 phát biểu đúng
Cho các chất: Fe, CrO3, Fe(NO3)2, FeSO4, Cr(OH)3, Na2Cr2O7. Số chất phản ứng được với dung dịch NaOH là
Có 5 chất phản ứng được với NaOH gồm: CrO3, Fe(NO3)2, FeSO4, Fe(OH)3, Na2Cr2O7.
PTHH:
CrO3 + H2O → H2CrO4; H2CrO4 + 2NaOH → Na2CrO4 + 2H2O
Fe(NO3)2 + 2NaOH → Fe(OH)2 + 2NaNO3
FeSO4 + 2NaOH → Fe(OH)2 + Na2SO4
Cr(OH)3 + NaOH → NaCrO2 + 2H2O
Na2Cr2O7 + 2NaOH → 2Na2CrO4 + H2O
Cho các phát biểu sau:
(a) Các kim loại Na, K, Ba đều phản ứng mạnh với nước.
(b) Kim loại Cu tác dụng với dung dịch hỗn hợp NaNO3 và H2SO4 (loãng).
(c) Crom bền trong không khí và nước do có màng oxit bảo vệ.
(d) Cho bột Cu vào lượng dư dung dịch FeCl3, thu được dung dịch chứa 3 muối.
(e) Hỗn hợp Al và BaO (tỉ lệ mol tương ứng là 1 : 1) tan hoàn toàn trong nước dư.
(g) Lưu huỳnh, photpho, ancol etylic đều bốc cháy khi tiếp xúc với CrO3.
Số phát biểu đúng là
(a) đúng
(b) đúng, PTHH: 3Cu + 2NO3- + 8H+ → 3Cu2+ + 2NO + 4H2O
(c) đúng
(d) đúng, PTHH: Cu + 2FeCl3 → CuCl2 + 2FeCl2
(Vậy dung dịch muối thu được gồm 3 muối: CuCl2, FeCl2, FeCl3 dư)
(e) đúng. Giải thích:
BaO + H2O → Ba(OH)2
1 mol → 1 mol
2Al + Ba(OH)2 + 2H2O → Ba(AlO2)2 + 3H2
1 → 0,5dư 0,5 => Al tan hết
(g) đúng vì CrO3 có tính oxi hóa rất mạnh nên lưu huỳnh, photpho, ancol etylic bốc cháy khi gặp CrO3.
Vậy có tất cả 6 phát biểu đúng
Cho hỗn hợp gồm Na2O, CaO, Al2O3 và MgO vào lượng nước dư, thu được dung dịch X và chất rắn Y. Sục khí CO2 đến dư vào X, thu được kết tủa là
Na2O + H2O → 2Na+ + 2OH-
CaO + H2O → Ca2+ + 2OH-
Al2O3 + 2OH- →2AlO2- + H2O
Vậy dung dịch X có chứa Na+, Ca2+, AlO2-, OH- (có thể dư)
Khi sục CO2 dư vào dd X:
CO2 + OH- → HCO3-
CO2 + AlO2- + H2O → Al(OH)3↓ + HCO3-
Vậy kết tủa thu được sau phản ứng là Al(OH)3
Cho các thí nghiệm sau
(a) Cho Ba vào dung dịch chứa phèn chua
(b) Cho FeCl2 vào dung dịch AgNO3
(c) Cho Ca(OH)2 vào Mg(HCO3)2
(d) Sục khí NH3 vào dung dịch hỗn hợp CuCl2 và AlCl3
(e) Cho một miếng nhôm vào dung dịch NaOH dư rồi sục khí CO2 vào
Tổng số thí nghiệm có khả năng tạo kết tủa là :
(a) tạo kết tủa BaSO4 có thể có thêm Al(OH)3
Ba + 2H2O → Ba(OH)2 + H2↑
Ba2+ + SO42- → BaSO4↓ + H2O
Al3+ + 3OH- → Al(OH)3↓
(b) tạo kết tủa AgCl và Ag
FeCl2 + 2AgNO3 → 2AgCl↓ + Fe(NO3)2
Fe(NO3)2 + AgNO3 → Ag↓ + Fe(NO3)3
(c) tạo kết tủa CaCO3 và MgCO3
Ca(OH)2 + Mg(HCO3)2 → CaCO3↓ + MgCO3↓ + 2H2O
(d) tạo Al(OH)3 có thể có Cu(OH)2
NH3 + H2O + AlCl3 → Al(OH)3↓ + NH4Cl
NH3 + H2O + CuCl2 → Cu(OH)2↓ + NH4Cl
4NH3 + Cu(OH)2 → Cu(NH3)4(OH)2 phức tan
(e) tạo kết tủa Al(OH)3 không tan trong CO2
Al + NaOH + H2O → NaAlO2 + 3/2H2↑
Thực hiện các thí nghiệm sau:
(a) Nhiệt phân AgNO3
(b) Nung FeS2 trong không khí
(c) Nhiệt phân KNO3
(d) Nhiệt phân Cu(NO3)2
(e) Cho Fe vào dung dịch CuSO4
(g) Cho Zn vào dung dịch FeCl3 dư
(h) Điện phân dung dịch CuCl2
(i) Cho Ba vào dung dịch CuSO4 (dư)
Số thí nghiệm thu được kim loại sau khi các phản ứng kết thúc là
(a) 2AgNO3 \(\xrightarrow{{{t}^{o}}}\) 2Ag + 2NO2 + O2 => thu được kim loại Ag
(b) 4FeS2 + 11O2 \(\xrightarrow{{{t}^{o}}}\) 2Fe2O3 + 8SO2 => không thu được kim loại
(c) 2KNO3 \(\xrightarrow{{{t}^{o}}}\) 2KNO2 + O2 => không thu được kim loại
(d) 2Cu(NO3)2 \(\xrightarrow{{{t}^{o}}}\) 2CuO + 4NO2 + O2 => không thu được kim loại
(e) Fe + CuSO4 → FeSO4 + Cu => thu được kim loại Cu (có thể thu được Fe dư)
(g) Zn + 2FeCl3 dư → ZnCl2 + 2FeCl2 => không thu được kim loại
(h) CuCl2 \(\xrightarrow{dp\text{dd}}\) Cu + Cl2 => thu được kim loại Cu
(i)
Ba + 2H2O → Ba(OH)2 + H2
CuSO4 + Ba(OH)2 → Cu(OH)2 + BaSO4
=> không thu được kim loại
Vậy có 3 phản ứng thu được kim loại là (a) (e) và (h)
Thực hiện các thí nghiệm sau:
(a) Cho a mol NO2 vào dung dịch chứa a mol NaOH.
(b) Cho a mol HCl vào dung dịch chứa a mol Na3PO4.
(c) Cho Fe3O4 tan vừa hết vào dung dịch chứa H2SO4 loãng.
(d) Cho a mol P2O5 vào dung dịch chứa 3a mol KOH.
(e) Cho Fe(NO3)2 vào dung dịch HCl loãng dư, thu được khí NO (sản phẩm khử duy nhất).
(f) Cho K2Cr2O7 vào dung dịch HCl đặc, đun nóng.
Sau khi các phản ứng kết thúc, số thí nghiệm thu được dung dịch có chứa hai muối mà số mol bằng nhau là
(a) NO2 + 2NaOH → NaNO2 + NaNO3 + H2O=> thu được 2 muối có số mol bằng nhau
(b) HCl + Na3PO4 → NaCl + Na2HPO4 => thu được 2 muối có số mol bằng nhau
(c) Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3 + 4H2O=> thu được 2 muối có số mol bằng nhau
(d) P2O5 + 2H2O → 2H3PO4
a → 2a (mol)
2H3PO4 + 3KOH → K2HPO4 + KH2PO4 + 3H2O => thu được 2 muối có số mol bằng nhau
2a →3a
(e) 9Fe(NO3)2 + 12HCl → 4FeCl3 + 5Fe(NO3)3 + 3NO + 6H2O => Thu được 2 muối có số mol khác nhau
(f) K2Cr2O7 + 14HCl → 2KCl + 2CrCl3 + 3Cl2 + 7H2O=> Thu được 2 muối có số mol khác nhau
=> có 5 thí nghiệm thu được 2 muối có số mol khác nhau
Cho hỗn hợp khí X gồm CO2, CO, N2 và hơi nước lần lượt đi qua các bình mắc nối tiếp chứa lượng dư mỗi chất: CuO đun nóng; dung dịch nước vôi trong; dung dịch H2SO4 đặc.Giả thiết các phản ứng xảy ra hoàn toàn. Khí ra khỏi bình chứa H2SO4 đặc là
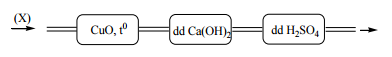
Cho hỗn hợp khí X qua CuO, t0 có CO bị giữ lại
CO + CuO \(\buildrel {{t^0}} \over\longrightarrow \) Cu + CO2↑
Khí đi ra gồm: CO2 và N2. Hỗn hợp khí này cho qua dd Ca(OH)2 thì CO2 sẽ bị giữ lại
CO2 + Ca(OH)2 → CaCO3↓ + H2O
Khí thoát ra là hơi H2O và N2. Cho hỗn hợp khí này qua dd H2SO4 đặc thì H2O bị giữ lại (do H2SO4 đặc có tính háo nước mạnh) => khí thoát ra khỏi bình chứa H2SO4 đặc là N2.
Tiến hành các thí nghiệm sau :
(a) Cho Mg vào dung dịch Fe2(SO4)3 dư
(b) Sục khí H2S vào dung dịch FeCl3
(c) Cho FeS tác dụng với dung dịch HCl
(d) Cho dung dịch AgNO3 vào dung dịch HCl
(e) Cho tinh thể NaNO2 vào dung dịch NH4Cl bão hòa rồi đun nóng
Số thí nghiệm không sinh ra đơn chất là
(a) Mg + Fe2(SO4)3 → MgSO4 + FeSO4
(b) H2S + FeCl3 → FeCl2 +HCl + S↓
(c) FeS + 2HCl → FeCl2 + H2S
(d) AgNO3 + HCl → AgCl↓ + HNO3
(e) NaNO2 + NH4Cl → NaCl + N2↑ + 2H2O
Số thí nghiệm không sinh đơn chất là 2
Cho ba dung dịch, mỗi dung dịch chứa một chất tan tương ứng là X, Y, Z và có cùng nồng độ mol/l. Trộn V lít dung dịch X với Vlít dung dịch Y,thu được dung dịch E chứa một chất tan. Cho dung dịch E tác dụng với 2V lít dung dịch Z, thu được dung dịch F chứa một chất tan. Chất X, Y, Z lần lượt là
A. NaOH + NaHSO4 → Na2SO4 (E)+ H2O
Na2SO4 + NaHCO3 → Không xảy ra pư => loại
B. H3PO4 + Na3PO4 → Na2HPO4 (E)
E không phản ứng với F => loại
C. Loại vì X và Y không phản ứng với nhau
D. H3PO4 + Na2HPO4 → 2NaH2PO4 (E)
V : V → 2V (lít)
NaH2PO4 + Na3PO4 → 2Na2HPO4 (F)
2V : 2V (lít) =>phản ứng vừa đủ hết => thỏa mãn
Có các thí nghiệm:
(1) Nhỏ dung dịch NaOH dư vào dung dịch hỗn hợp KHCO3 và CaCl2.
(2) Đun nóng dung dịch chứa hỗn hợp Ca(HCO3)2 và MgCl2.
(3) Cho "nước đá khô" vào dung dịch axit HCl.
(4) Nhỏ dung dịch HCl vào "thủy tinh lỏng".
(5) Thêm sođa khan vào dung dịch nước vôi trong.
Số thí nghiệm thu được kết tủa là
(1) Thu được kết tủa CaCO3
2NaOH + 2KHCO3 → Na2CO3 + K2CO3 + 2H2O
Na2CO3 + CaCl2 → CaCO3↓ + 2NaCl
(2) Thu được kết tủa MgCO3
Ca(HCO3)2 + MgCl2 \(\buildrel {{t^0}} \over\longrightarrow \) CaCl2 + MgCO3↓ + CO2↑ + H2O
(3) Không thu được kết tủa
(4) Thu được kết tủa H2SiO3
HCl + Na2SiO3 → NaCl + H2SiO3↓
(5) Thu được kết tủa CaCO3
Na2CO3 + Ca(OH)2 → CaCO3↓ + 2NaOH
=> có 4 thí nghiệm thu được kết tủa.

