Cho biết năng lượng ở trạng thái dừng thứ n của nguyên tử hiđrô có biểu thức En=−13,6n2eV(n=1,2,3...). Một nguyên tử hiđrô đang ở mức năng lượng C thì nhận một photon có năng lượng ε=1715eV chuyển lên mức năng lượng D. Cho r0 là bán kính Bo. Trong quá trình đó, bán kính quỹ đạo nguyên tử hiđrô đã tăng thêm
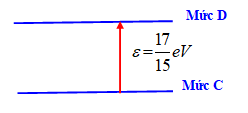
Để electron chuyển từ trạng thái có mức năng lượng C lên trạng thái có mức năng lượng D thì cần nhận photon có năng lượng:
ε=ED−EC→1715=(−13,6n2D+13,6n2C)→1n2C−1n2D=113→1n2C>112→nC<3,5
+ nC=1→1n2C=1(loại)
+ nC=2→1n2C=14(loại)
+ nC=3→1n2C=19→nD=6
Bán kính quỹ đạo nguyên tử hiđrô đã tăng thêm: Δr=62ro−32ro=27ro
Xét nguyên tử hiđrô theo mẫu nguyên tử Bo, mức năng lượng của nó ở các trạng thái dừng theo thứ tự tăng dần từ giá trị nhỏ nhất là E1,E2,E3… Nguyên tử hiđrô hấp thụ một phôtôn có năng lượng ε=E3−E1 thì êlectron chuyển từ quỹ đạo
Các mức năng lượng E1,E2,E3 tương ứng với các trạng thái dừng trên các quỹ đạo K,L,M.
Vậy khi nguyên tử hiđrô hấp thụ một phôtôn có năng lượng ε=E3−E1 thì êlectron chuyển từ quỹ đạo K lên quỹ đạo M.
Xét nguyên tử hiđrô theo mẫu nguyên tử Bo, khi nguyên tử chuyển từ trạng thái dừng có năng lượng −3,4eV sang trạng thái dừng có năng lượng −13,6eV thì nó phát ra một phôtôn có năng lượng là
Khi nguyên tử chuyển từ trạng thái dừng có năng lượng −3,4 eV sang trạng thái dừng có năng lượng −13,6 eV thì nó phát ra một phôtôn có năng lượng là ε=−3,4−(−13,6)=10,2eV
Đề thi thử THPT chuyên Lam Sơn - 2021
Đối với nguyên tử Hiđrô, khi electron chuyển từ quỹ đạo L về quỹ đạo K thì nguyên tử phát ra photon ứng với bước sóng 121,8nm. Khi electron chuyển từ quỹ đạo M về quỹ đạo L, nguyên tử phát ra photon ứng với bước sóng 656,3nm. Khi electron chuyển từ quỹ đạo M về quỹ đạo K, nguyên tử phát ra photon ứng với bước sóng là bao nhiêu?
Ta có: {ε1=hcλ1=EL−EKε2=hcλ2=EM−EL
Khi electron chuyển từ quỹ đạo M về quỹ đạo K:
ε3=hcλ3=EM−EK=EM−EL+EL−EK=ε2+ε1
⇔hcλ3=hcλ1+hcλ2⇒λ3=λ1.λ2λ1+λ2=102,734nm
Mẫu nguyên tử Bohr khác mẫu nguyên tử Rutherford ở điểm nào dưới đây?
Mẫu Bohr đưa ra khái niệm trạng thái dừng là trạng thái có năng lượng xác định, còn mẫu Rutherford thì không có khái niệm trạng thái dừng.
Xét mẫu nguyên tử Hidro của Bo, coi chuyển động của electron trên quỹ đạo dừng là chuyển động tròn đều. Tỉ số giữa tốc độ của electron trên quỹ đạo K và trên quỹ đạo M là
Công thức tính lực hướng tâm: Fht=mv2r
Biểu thức của định luật Culong: F=k.|q1q2|r2
Khi electron chuyển động trên quỹ đạo dừng thì lực hút tĩnh điện đóng vai trò lực hướng tâm.
Ta có: k|q1q2|r2n=mv2rn⇒vn=√k.|q1q2|m.rn
⇒vKvM=√k.|q1q2|m.rKk.|q1q2|m.rM=√rMrK
Mặt khác bán kính quỹ đạo dừng được xác định là rn=n2.r0
Quỹ đạo K ứng với n=1; quỹ đạo M ứng với n=3
Nên tỉ số vLvN=√32.r0√12.r0=3
Biết năng lượng ứng với các trạng thái dừng của nguyên tử Hiđrô được tính theo biểu thức En=−E0n2 (E0 là hằng số dương và n = 1, 2, 3,…). Một đám nguyên tử hiđrô đang ở trạng thái cơ bản. Khi chiếu bức xạ có tần số f1 vào đám nguyên tử này thì chúng phát ra tối đa 3 bức xạ. Khi chiếu bức xạ có tần số f2 = 1,08f1 vào đám nguyên tử này thì chúng phát ra tối đa là
+ Khi chiếu bức xạ có tần số f1 vào đám nguyên tử này thì chúng phát ra tối đa 3 bức xạ:
N1=n1(n1−1)2=3⇒n1=3
⇒hf1=−E032−(−E012)=89E0
+ Lại có:
hf2=1,08.hf1=−E0n22−(−E012)⇔1.08.89E0=−E0n22+E0⇒n2=5
Số bức xạ phát ra tối đa:
N2=n2(n2−1)2=5.(5−1)2=10
Cho bán kính Bo là r0 = 5,3.10-11m, hằng số k = 9.109N.m2/C2, điện tích nguyên tố e = 1,6.10-19C, khối lượng êlectron me = 9,1.10-31 kg. Trong nguyên tử hiđrô, nếu êlectron chuyển động tròn đều quanh hạt nhân thì ở quỹ đạo L, tốc độ góc của êlectron là
Khi electron chuyển động tròn đều quanh hạt nhân, lực Cu – lông đóng vai trò là lực hướng tâm
Ta có: FC=Fht⇒k|q1q2|r2=mv2r⇒ke2r2=mω2r
⇒ω=√ke2mr3=√ke2m(n2r0)3=√ke2m(22r0)3⇒ω=√9.109.(1,6.10−19)29,1.10−31.(22.5,3.10−11)3=5,15.1015=0,5.1016(rad/s)
Nguyên tử hiđrô chuyển từ trạng thái dừng có năng lượng En = - 0,85 eV sang trạng thái dừng có năng lượng Em = - 3,40 eV. Bước sóng của bức xạ mà nguyên tử hiđrô phát ra xấp xỉ bằng
Khi hạt nhân Hidro chuyển từ mức năng lượng Em sang mức năng lượng En thì nó phát ra (hoặc hấp thụ) một photon có năng lượng :
ε=hcλ=En−Em=(−0,85)−(−3,40)=2,55eV=4,08.10−19J⇒λ=hcε=6,625.10−34.3.1084,08.10−19=0,48.10−6m=0,48μm
Xét nguyên tử hiđrô theo mẫu nguyên tử Bo. Khi nguyên tử hiđrô chuyển từ trạng thái dừng có năng lượng En về trạng thái cơ bản có năng lượng −13,6eV thì nó phát ra một phôtôn ứng với bức xạ có bước sóng 0,1218μm. Lấy h=6,625.10−34J.s ; c=3.108m/s ; 1eV=1,6.10−19J . Giá trị của En là
Ta có: En−Em=hf=hcλ
⇒En=hcλ.1,6.10−19−13,6(eV)=6,625.10−34.3.1080,1218.10−6.1,6.10−19−13,6=−3,4eV
Theo tiên đề Bo, bán kính Bo là ro=5,3.10-11m. Khi electron của nguyên tử chuyển động trên quỹ đạo có bán kính 132,5.10-11m đi được quãng đường 3S, thì cũng trong khoảng thời gian đó electron chuyển động trên quỹ đạo M sẽ đi được quãng đường là
Khi bán kính quỹ đạo là, 132,5.10-11m, n1=√rnrO=5
Lực Culong giữa electron và hạt nhân có vai trò là lực hướng tâm: Fht=ke2rn=mev2r→v=e.√kme.rn=2,2.106n=> v tỉ lệ nghịch với n
Quãng đường electron đi được trong một khoảng thời gian tỉ lệ thuận với vận tốc chuyển động của electron, nên tỉ lệ nghịch với n.
→S1S2=n2n1→S2=S1n1n2=3S.53=5S
Chọn C
Xét nguyên tử hiđrô theo mẫu nguyên tử Bo. Cho biết bán kính Bo r0 = 5,3.10-11 m. Quỹ đạo dừng M của êlectron trong nguyên tử có bán kính
Áp dụng tiên đề về trạng thái dừng của nguyên tử trong mẫu nguyên tử Bo
Quỹ đạo dừng M có n=3
→r=n2r0=32.5,3.10−11=4,77.10−10m
Xét nguyên tử hidro theo mẫu nguyên tử Bo, bán kính các quỹ đạo dừng: K; L; M; N; O;... của electron tăng tỉ lệ với bình phương của các số nguyên liên tiếp. Quỹ đạo dừng K có bán kính ro (bán kính Bo). Quỹ đạo dừng N có bán kính
Bán kính quỹ đạo Bo: rn=n2r0
Quỹ đạo dừng N ứng với n=4
⇒rN=42r0=16r0
Một electron hấp thụ năng lượng chuyển từ quỹ đạo L lên quỹ đạo N thì bán kính quỹ đạo
Quỹ đạo L ứng với n=2; quỹ đạo N ứng với n=4.
Ta có: rNrL=42r022r0=4⇒rN=4rL
Xét nguyên tử hidro theo mẫu nguyên tử Bo. Khi nguyên tử hiđrô chuyển từ trạng thái dùng có năng lượng –0,544 eV về trạng thái dừng có năng lượng ‒3,4 eV thì nó phát ra một phôtôn ứng với bức xạ có bước sóng . Lấy h=6,{625.10^{ - 34}}J.s; c = {3.10^8}m/s; 1eV = 1,{6.10^{ - 19}}J. Giá trị của \lambda là
Ta có:
\dfrac{{hc}}{\lambda } = {E_1} - {E_2} \\\to \lambda = \dfrac{{hc}}{{{E_1} - {E_2}}} = \dfrac{{6,{{625.10}^{ - 34}}{{.3.10}^8}}}{{( - 0,544 + 3,4).1,{{6.10}^{ - 19}}}} \approx 0,{4349396.10^{ - 6}}(m)
Theo mẫu nguyên tử Bo, trong nguyên tử hidro, bán kính quỹ đạo dừng K là r0. Khi electron chuyển từ quỹ đạo dừng O về quỹ đạo dừng M thì bán kính quỹ đạo giảm
Quỹ đạo O có n = 5; quỹ đạo M có n = 3
Bán kính quỹ đạo dừng M và O là:{r_M} = {{{r_0}}}{{{3^2}}} = {{{r_0}}}{9};{r_O} = {{{r_0}}}{{{5^2}}} = {{{r_0}}}{{25}}
Vậy khi chuyển từ quỹ đạo O về M thì bán kính quỹ đạo giảm: 25r0 - 9r0 = 16r0
Theo mẫu Bo về nguyên tử hidro, tốc độ của electron trên quỹ đạo K là v. Để tốc độ của electron là v/3 thì nó chuyển động trên quỹ đạo nào sau đây?
Electron chuyển động tròn trong nguyên tử hidro nên lực điện đóng vai trò lực hướng tâm
k\dfrac{{{e^2}}}{{{r^2}}} = m\dfrac{{{v^2}}}{r} \\\Rightarrow {v^2} = \dfrac{{k{e^2}}}{{mr}} = \dfrac{{k{e^2}.{n^2}}}{{m{r_0}}}
Để tốc độ giảm 3 lần thì n tăng lên 3 lần vậy electron chuyển động trên quỹ đạo M có n = 3
Theo mẫu nguyên tử Bo, trạng thái dừng của nguyên tử:
Theo mẫu nguyên tử Bo, trạng thái dừng của nguyên tử có thể là trạng thái cơ bản hoặc trạng thái kích thích.
Theo mẫu nguyên tử Bo, bán kính quỹ đạo dừng được xác định bởi:
Theo mẫu nguyên tử Bo, bán kính quỹ đạo dừng được xác định bởi:
{r_n} = {n^2}{r_0}
Cho bán kính quỹ đạo Bo thứ nhất của nguyên tử H là 0,53.10-10m. Bán kính quỹ đạo Bo thứ 5 của nguyên tử H bằng:
Bán kính của quỹ đạo Bo thứ 5 là :
{r_5} = {5^2}.{r_0} = 25.0,{53.10^{ - 10}} = 13,{25.10^{ - 10}}m

