Các hạt cấu tạo nên nguyên tử là:
Hầu hết nguyên tử đều bao gồm các hạt p, n, e
Hợp chất A có công thức hóa học là MX3, M là kim loại, X là phi kim, biết:
Trong A, tổng số hạt p,n, e là 196, số hạt mang điện nhiều hơn số hạt không mang điện là 60. Số khối của X lớn hơn M là 8. Tổng số hạt trong X nhiều hơn trong M là 12. Công thức hóa học của A là:
Ta có hệ : ![]() => P + E = 128 : N = 68
=> P + E = 128 : N = 68
Vì P = E => P = E = 128 : 2 = 64
AX = AM + 8 => P x + N x = P M + N M + 8
Tổng số hạt trong X nhiều hơn trong M là 12 vì số P = E nên
2 P x + N x = 2 P M + N M + 12
Ta có hệ : ![]() =>P x = P M + 4
=>P x = P M + 4
Mà tổng P = 64
Ta có hệ : ![]() => Px = 17 , PM = 13
=> Px = 17 , PM = 13
=>X là Cl
=>M là Al
Phát biểu nào dưới đây không đúng?
Ta có: đường kính của hạt nhân nguyên tử vào khoảng 10-5 nm= 10-14m,
đường kính nguyên tử vào khoảng 10-10m
Suy ra đường kính của hạt nhân nhỏ hơn đường kính nguyên tử khoảng 10 000 lần. Vậy phát biểu A đúng.
Ta có: mp= 1,6726.10-27kg và mn= 1,6748.10-27 kg. Suy ra phát biểu B đúng.
Ta có: me= 9,1094.10-31 kg nên khối lượng nguyên tử tập trung chủ yếu ở hạt nhân nguyên tử. Suy ra phát biểu C đúng.
Ta có me <<mP nên khối lượng electron nhỏ hơn khối lượng của proton khoảng 1840 lần.
Vậy phát biểu D không đúng.
Đồng vị nào sau đây mà hạt nhân không có notron?
Đồng vị \({}_1^1H\) có số n= 1-1= 0
Đồng vị \({}_1^2H\) có số n= 2-1 = 1
Đồng vị \({}_1^3H\) có số n= 3- 1= 2
Vậy đồng vị \({}_1^1H\) thì hạt nhân không có notron.
Nguyên tử có tổng số hạt là 34, trong đó tổng số hạt mang điện gấp 1,8333 lần số hạt không mang điện. Số hạt không mang điện của nguyên tử đó là:
Gọi số hạt p (bằng số hạt e) trong nguyên tử nguyên tố X bằng Z.
Gọi số hạt n trong nguyên tử nguyên tố X bằng N.
Vì nguyên tử có tổng số hạt là 34, trong đó tổng số hạt mang điện gấp 1,8333 lần số hạt không mang điện nên ta có: 2Z + N= 34 và 2Z= 1,8333N
Giải hệ trên ta có: Z= 11 và N= 12
Vậy số hạt không mang điện bằng 12
Ở điều kiện thường crom có cấu trúc mạng lập phương tâm khối trong đó thể tích các nguyên tử chiếm 68% thể tích tinh thể. Khối lượng riêng của Cr là 7,2 g/cm3. Tính bán kính nguyên tử của crom (cho Cr = 52; coi nguyên tử Cr có dạng hình cầu).
Xét 1 mol nguyên tử crom có số nguyên tử crom bằng 6,022.1023 nguyên tử và khối lượng là 52 gam.
Thể tích của 1 mol nguyên tử crom là: \(V = \dfrac{{52}}{{7,2}} = 7,22(c{m^3}) = 7,{22.10^{ - 6}}({m^3})\)
Thể tích thực của 1 nguyên tử crom là: \(V = \dfrac{{7,{{22.10}^{ - 6}}.0,68}}{{6,{{022.10}^{23}}}} = 8,{16.10^{30}}({m^3})\)
Do coi nguyên tử Cr có dạng hình cầu nên thể tích nguyên tử được tính theo công thức:
\(V = \dfrac{{4\pi {R^3}}}{3}\) suy ra R = 0,125.10-9 m= 0,125 nm
Hạt mang điện tích dương là
Hạt mang điện tích dương là hạt proton
Hợp chất Y có công thức phân tử MX2, trong đó M chiếm 46,67% về khối lượng. Trong hạt nhân M có số notron nhiều hơn số proton là 4 hạt. Trong hạt nhân X số notron bằng số proton. Tổng số proton trong MX2 là 58. Phân tử khối của Y là (chấp nhận nguyên tử khối có trị số bằng số khối)?
Tổng số proton trong MX2 là 58 hạt nên ZM + 2.ZX= 58 (1)
Trong hạt nhân M có số notron nhiều hơn số proton là 4 hạt nên –ZM + NM= 4 (2)
Trong hạt nhân X số notron bằng số proton nên ZX= NX (3)
Phân tử khối của hợp chất Y bằng MY= ZM + NM + 2.(ZX + NX)= (ZM+ 2.ZX) + (NM+ 2.NX)= 58 + NM + 2.NX
Trong hợp chất MX2, nguyên tố M chiếm 46,67% về khối lượng nên ta có:
\(\dfrac{{{N_M} + {Z_M}}}{{58 + {N_M} + 2{N_X}}}.100\% = 46,67\% \) (4)
Từ 4 phương trình (1), (2), (3), (4) ta có ZM= 26, NM=30.
Suy ra AM= ZM + NM= 26 + 30= 56 suy ra M là nguyên tố Fe
Thay vào (4) ta có NX= 16, ZX= 16 suy ra AX= NX + ZX= 32 suy ra X là nguyên tố S.
Hợp chất Y là FeS2, hợp chất Y có phân tử khối bằng 56 + 2.32= 120
Cho các nhận định sau:
(1) Số protron trong hạt nhân nguyên tử bằng số electron trong nguyên tử.
(2) Trong hạt nhân nguyên tử, số proton luôn bằng số nơtron.
(3) Số hiệu nguyên tử bằng số đơn vị điện tích hạt nhân nguyên tử.
(4) Chỉ có hạt nhân nguyên tử lưu huỳnh mới có 16 nơtron.
Những nhận định đúng là
(1) đúng, số protron trong hạt nhân nguyên tử bằng số electron trong nguyên tử (do nguyên tử trung hòa về điện).
(2) sai, chỉ có biểu thức liên hệ giữa số p và số n: 1 ≤ n / p ≤ 1,52 (áp dụng với 82 nguyên tố đầu tiên).
(3) đúng.
(4) sai, hạt nhân \({}_{15}^{31}P\)cũng có 31 - 15 = 16 nơtron.
Vậy các nhận định (1), (3) đúng.
asdga
sdgasdg
Nguyên tử của nguyên tố X có tổng số hạt là 40. Tổng số hạt mang điện nhiều hơn tổng số hạt không mang điện là 12 hạt. Nguyên tố X có số khối là :
Gọi số p = số e = Z; số n = N
- Tổng số hạt = số p + số e + số n = 2Z + N = 40 (1)
- Số hạt mang điện (p, e) nhiều hơn số hạt không mang điện (n): 2Z – N = 12 (2)
Giải (1) và (2) thu được Z = 13 và N = 14
Số khối A = Z + N = 13 + 14 = 27
Các hạt cấu tạo nên hầu hết các hạt nhân nguyên tử là
????
Chromium có cấu trúc mạng lập phương tâm khối có bán kính nguyên tử là 1,25\(\mathop A\limits^o \). Khối lượng riêng của Cr là 7,2 g/cm3 và khối lượng nguyên tử của Cr là 51,99. Nếu xem nguyên tử Cr có dạng hình cầu thì các nguyên tử Cr chiếm bao nhiêu phần trăm trong tinh thể?
Thể tích của 1 mol nguyên tử Cr là \(V = \dfrac{{51,99}}{{7,2}} = 7,22\,\,\,c{m^3} = 7,{22.10^{ - 6}}\,\,\,{m^3}\)
Gọi phần trăm các nguyên tử Cr chiếm chỗ trong tinh thể là a
=> Thể tích thực của 1 nguyên tử Cr là \(V = \dfrac{{7,{{22.10}^{ - 6}}.a}}{{6,{{022.10}^{23}}}}\,\,\)
Có \(V = \dfrac{4}{3}\Pi {r^3} \Leftrightarrow \frac{{7,{{22.10}^{ - 6}}.a}}{{6,{{022.10}^{23}}}} = \dfrac{4}{3}.\Pi .{(1,{25.10^{ - 10}})^3} \Leftrightarrow a = 68\% \)
Giả thiết nguyên tử aluminium có bán kính 1,43 \(\mathop A\limits^o \) và có nguyên tử khối là 27. Trong tinh thể các nguyên tử chỉ chiếm 74% thể tích, còn lại là các khe trống. Khối lượng riêng của aluminium có giá trị là
Thể tích 1 mol nguyên tử Al là \(V = \dfrac{M}{d}.74\% = \dfrac{{27}}{d}.74\% \)
Thể tích 1 nguyên tử Al là \(V = \dfrac{{27}}{d}.74\% .\dfrac{1}{{6,{{022.10}^{23}}}}\)
Có \(V = \dfrac{4}{3}\Pi {r^3} \Rightarrow d = 2,7\,\,\,g/c{m^3}\)
sdgas
sgs
sdgas
sdgsd
Cho mô hình nguyên tử được cấu tạo bởi ba loại hạt cơ bản X, Y, Z như hình vẽ sau đây:
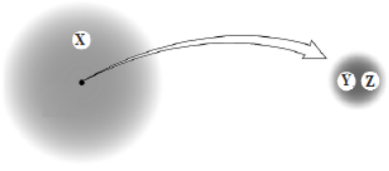
Cho các phát biểu sau:
(a) Trong mọi nguyên tử, khối lượng của Y lớn hơn khối lượng của X.
(b) Số hạt Y và số hạt Z bằng nhau trong mọi nguyên tử.
(c) Tổng số hạt Y và Z trong tất cả các nguyên tử được gọi là số khối của nguyên tử.
(d) Tổng số điện tích của Y và Z trong tất cả các nguyên tử là dương.
Số phát biểu đúng là
Từ hình vẽ => X là hạt electron; Y và Z là hạt proton, neutron trong hạt nhân nguyên tử
(a) đúng vì khối lượng nguyên tử xấp xỉ bằng khối lượng hạt nhân nguyên tử
(b) sai vì trong nguyên tử không có quy ước số hạt proton bằng số hạt neutron
(c) đúng
(d) đúng
Hạt nhân của hầu hết các nguyên tử được cấu tạo từ các loại hạt sau:
Hạt nhân của hầu hết các nguyên tử cấu tạo từ các loại hạt proton và notron (trừ nguyên tử H không có notron).
AAAAA
SFSDG
Trong các câu sau đây, câu nào sai ?
Câu sai là: Electron có khối lượng đáng kể so với khối lượng nguyên tử.
Vì electron có khối lượng rất nhỏ bé so với proton và nơtron

