Cho mô hình cấu tạo nguyên tử của 4 nguyên tố X, Y, Z, T như hình sau:

Những nguyên tố nào có khả năng tham gia hình thành liên kết cộng hoá trị?
Liên kết cộng hoá trị thường hình thành giữa các phi kim với nhau
Nguyên tố là phi kim khi có 5, 6, 7e lớp ngoài cùng
=> Nguyên tố có khả năng hình thành liên kết cộng hoá trị là Y, Z, T
Bảng dưới đây cho biết sự phân bố electron trên các lớp vỏ của bốn nguyên tử X, Y, Z, W

Hai nguyên tử nguyên tố nào có thể kết hợp với nhau tạo thành hợp chất chứa liên kết cộng hoá trị?
Liên kết cộng hoá trị thường hình thành giữa các phi kim với nhau
Nguyên tố là phi kim khi có 5, 6, 7e lớp ngoài cùng
=> Hai nguyên tử nguyên tố có thể kết hợp với nhau tạo thành hợp chất chứa liên kết cộng hoá trị là Y và Z
Để tuân theo quy tắc octet, các nguyên tử trong chất có liên kết cộng hóa trị liên kết với nhau bằng
Để tuân theo quy tắc octet, các nguyên tử trong chất có liên kết cộng hóa trị liên kết với nhau bằng việc sử dụng các cặp electron dùng chung.
Phân tử HCl (hydrogen chloride) được tạo thành bởi liên kết cộng hóa trị. Mô tả nào sau đây đúng khi nói về sự tạo thành phân tử HCl?
Nguyên tử H có 1 electron ở lớp ngoài cùng, nguyên tử Cl có 1 electron ở lớp ngoài cùng. Để đạt đến cấu hình của khí hiếm gần nhất, hai nguyên tử H và Cl đã liên kết với nhau bằng cách mỗi nguyên tử góp 1 electron tạo thành 1 cặp electron dùng chung trong phân tử HCl.

Cho phản ứng giữa hai hợp chất AB và CD cùng mô hình liên kết như sau:
\(2AB + CD \to (E) + {A_2}D\)

Phát biểu nào sau đây không đúng?
Sau phản ứng tạo thành hợp chất A2D => Gía trị của m là 2
Từ mô hình của D2- => Mô hình của D gồm có 3 lớp electron
Nhận thấy mô hình của B và D đều có 3 lớp electron. Sự khác nhau là ở số electron lớp ngoài cùng.
- Với B có 3 cặp electron chưa tham gia liên kết ở lớp ngoài cùng
- Với D không có cặp electron nào chưa tham gia liên kết ở lớp ngoài cùng
=> B đúng
Từ mô hình thấy có ion C2+, B nhận thêm 1 electron tạo thành B- => Hợp chất E là CB2 => C đúng
D sai vì A với D tạo thành liên kết ion => B với C tạo thành liên kết ion
Cho hình sau đây mô tả cặp electron dùng chung giữa các nguyên tử trong các hợp chất WX và WYZ
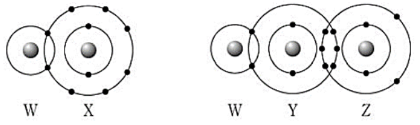
Phát biểu nào sau đây không đúng?
Y có 4 electron lớp ngoài cùng => Y thuộc nhóm IVA
W có 1 electron lớp ngoài cùng => W thuộc nhóm IA
=> Hợp chất giữa Y và W là YW4 => B đúng
X có 7 electron lớp ngoài cùng => X thuộc nhóm VIIA
Z có 5 electron lớp ngoài cùng => Z thuộc nhóm VA
=> Độ âm điện của các nguyên tố nhóm IVA < VA < VIIA => C đúng
W có giá trị độ âm điện nhỏ hơn X => Trong WX, W mang một phần điện tích dương => D đúng
Cho mô hình liên kết trong các hợp chất WX và YXZ sau:

Phát biểu nào sau đây đúng?
Từ mô hình thấy
- Y có 6 electron lớp ngoài cùng và có 2 lớp electron => Y thuộc nhóm VIA và chu kì 2
- X có 4 electron lớp ngoài cùng và có 2 lớp electron => X thuộc nhóm IVA và chu kì 2
- Z có 7 electron lớp ngoài cùng và có 2 lớp electron => Z thuộc nhóm VIIA và chu kì 2
- W2+ có 2 lớp electron. W2+ thêm 2 electron thì tạo cấu hình của W => W có 3 lớp electron và có 2 electron ở lớp ngoài cùng => W thuộc nhóm IIA
=> B đúng, D đúng
Các nguyên tố X, Y, Z thuộc cùng một chu kì. Trong một chu kì theo chiều tăng dần điện tích hạt nhân, độ âm điện tăng dần
=> Chiều sắp xếp tăng dần điện tích hạt nhân là X, Y, Z
=> Chiều sắp xếp tăng dần độ âm điện là X, Y, Z => C đúng
A sai vì Y thuộc nhóm VIA, Z thuộc nhóm VIIA đều là các phi kim điển hình => Hợp chất giữa Y và Z là hợp chất cộng hoá trị
Chọn câu đúng nhất về liên kết cộng hoá trị. Liên kết cộng hoá trị là liên kết:
Liên kết cộng hóa trị là liên kết được tạo thành từ hai nguyên tử bằng 1 hay nhiều cặp e chung.
Liên kết hóa học giữa các nguyên tử trong phân tử HCl thuộc loại liên kết
Liên kết trong HCl là liên kết cộng hóa trị phân cực
Trong các nhóm chất sau đây, nhóm nào chỉ gồm những hợp chất cộng hóa trị:
A. Loại vì MgCl2 chứa liên kết ion
B. Loại vì K2O, NaOH chứa liên kết ion
C. Đúng
D. Loại vì MgCl2 chứa liên kết ion
Kiểu liên kết tạo nên giữa hai nguyên tử bằng một hay nhiều cặp electron chung được gọi là
Liên kết cộng hóa trị được hình thành giữa hai nguyên tử bằng một hay nhiều cặp electron dùng chung.
Trong phân tử N2, số cặp electron dùng chung là (cho 7N)
Cấu hình e của 7N là 1s22s22p3
=> N thiếu 3 e để đạt được cấu hình bền của khí hiếm Ne 1s22s22p6
=> Trong phân tử N2, mỗi nguyên tử N góp chung 3e để mỗi nguyên tử đạt cấu hình bền
=> Số cặp e dùng chung là 3
Liên kết cộng hóa trị là liên kết được hình thành giữa 2 nguyên tử bằng
Liên kết cộng hóa trị là liên kết được hình thành giữa 2 nguyên tử bằng 1 hay nhiều cặp electron chung.
Liên kết cộng hóa trị phân cực là liên kết có thể tạo bởi
Liên kết cộng hóa trị phân cực là liên kết có thể tạo bởi hai nguyên tử của hai nguyên tố phi kim khác nhau
Dãy phân tử nào cho dưới đây đều có liên kết cộng hóa trị không phân cực ?
Liên kết cộng hóa trị không phân cực là liên kết mà trong đó đôi electron dùng chung không bị lệch về phía nguyên tử nào cả. => Liên kết cộng hóa trị không cực thường được hình hình thành giữa các nguyê tử của cùng một nguyên tố.
=>Dãy phân tử đều có liên kết cộng hóa trị không phân cực là: Cl2, O2, N2, F2.
Liên kết hoá học trong phân tử HCl là :
- Cấu hình e của H: 1s1 => thiếu 1e để tạo cấu hình bền => góp chung 1e
Cấu hình e của Cl: 1s22s22p63s23p5 => thiếu 1e để tạo thành cấu hình bền => góp chung 1e

- Cặp e liên kết bị lệch về phía clo (clo có độ âm điện lớn hơn) => liên kết cộng hóa trị bị phân cực.
Vậy liên kết hoá học trong phân tử HCl là liên kết cộng hoá trị phân cực.
Công thức electron của Cl2 là :
Clo có cấu hình e: 1s22s22p63s23p5 => mỗi nguyên tử góp chung 1e tạo cấu hình bền
=> Công thức electron của Cl2 là : $:\underset{.\,\,.}{\overset{.\,\,.}{\mathop{Cl}}}\,:\underset{.\,\,.}{\overset{.\,\,.}{\mathop{Cl}}}\,:$
Công thức cấu tạo phân tử O2 là
Oxi có cấu hình e: 1s22s22p4 => mỗi nguyên tử góp chung 2e tạo cấu hình bền
$:\overset{.\,\,.}{\mathop{O}}\,:\,\,+\,\,:\overset{.\,\,.}{\mathop{O}}\,:\,\,\,\to \,\,\,:\overset{.\,\,.}{\mathop{O}}\,::\overset{.\,\,.}{\mathop{O}}\,:$
=> Công thức cấu tạo phân tử O2 là O = O
Cho nguyên tố H (Z = 1) và nguyên tố S (Z = 16). Hợp chất tạo thành từ 2 nguyên tố là
H: 1s1 => góp chung 1e
S: 1s22s22p63s23p4 => góp chung 2e
=> 1 nguyên tử S liên kết với 2 nguyên tử H tạo thành hợp chất H2S
Các liên kết trong phân tử nitơ gồm
N: 1s22s22p3
- Mỗi nguyên tử nitơ có 5e lớp ngoài cùng => còn thiếu 3e để đạt cấu hình bền theo quy tắc bát tử
=> mỗi nguyên tử N góp chung 3e
=> Hai nguyên tử N liên kết với nhau bằng 3 cặp electron liên kết biểu thị bằng 3 gạch (≡)
=> hình thành liên kết 3
Liên kết ba bao gồm: 1 liên kết δ, 2 liên kết π.

