Bài 22: Hydrogen halide - Muối halide
Sách kết nối tri thức với cuộc sống
Mệnh đề không chính xác là
Mệnh đề không chính xác là: tất cả các muối AgX (X là halogen) đều không tan.
Vì AgF là muối tan
Cho dãy axit HF, HCl, HBr, HI. Theo chiều từ trái sang phải, tính chất axit biến đổi như sau:
$\xrightarrow{{HF\,\,\,\,\,\,\,\,\,\,\,HCl\,\,\,\,\,\,\,\,\,\,\,\,HB{\text{r}}\,\,\,\,\,\,\,\,\,\,\,\,HI}}$
Tính axit tăng dần, tính khử tăng dần
Trong muối NaCl có lẫn NaBr và NaI. Để loại 2 muối này ra khỏi NaCl, người ta có thể
Để loại 2 muối này ra khỏi NaCl, người ta cho dung dịch hỗn hợp tác dụng với khí Cl2 dư, sau đó cô cạn dung dịch.
2NaBr + Cl2 → 2NaCl + Br2
2NaI + Cl2 → 2NaCl + I2
Cho các phát biểu sau:
(a) Trong các phản ứng hóa học, flo chỉ thể hiện tính oxi hóa;
(b) Axit flohiđric là axit yếu;
(c) Dung dịch NaF loãng được dùng làm thuốc chống sâu răng;
(d) Trong hợp chất, các halogen (F, Cl, Br, I) đều có số oxi hóa -1, +1, +3, +5, +7;
(e) Tính khử của các ion halogenua tăng dần theo thứ tự: F-, Cl-, Br-, I-.
Trong các phát biểu trên, số phát biểu đúng là
Các phát biểu đúng là
(a) Trong các phản ứng hóa học, flo chỉ thể hiện tính oxi hóa;
(b) Axit flohiđric là axit yếu
(c) Dung dịch NaF loãng được dùng làm thuốc chống sâu răng;
(e) Tính khử của các ion halogenua tăng dần theo thứ tự: F-, Cl-, Br-, I-.
Điều nào sau đây đúng khi nói về cấu tạo của phân tử hydrogen halide HX với X là các halogen?
A sai vì liên kết H với X là liên kết cộng hoá trị
C sai. Để đạt được trạng thái bền của khí hiếm gần nhất, các nguyên tố halogen nhận thêm 1 electron
D sai. Liên kết HX thuộc loại liên kết cộng hóa trị phân cực
Cho các tính chất vật lí sau:
(1) Ở điều kiện thường tồn tại dạng thể khí.
(2) Không tan trong nước lạnh, tan tốt trong nước nóng.
(3) Nhiệt độ sôi tăng dần.
(4) Độ dài liên kết tăng dần.
(5) Năng lượng liên kết tăng dần.
Số phát biều đúng khi nói về tính chất vật lí của các hydrogen halide từ HF đến HI là
Đáp án A
Tại sao HF lỏng có nhiệt độ sôi cao bất thường?
HF lỏng có nhiệt độ sôi cao bất thường vì HF phân cực mạnh, có khả năng tạo liên kết hydrogen
Cho bảng thông tin về các hydrogen halide như sau:
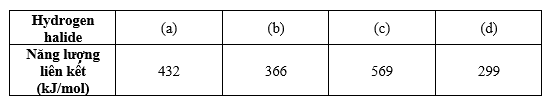
Chất (b) và (d) lần lượt là
Năng lượng liên kết của Hydrogen halide giảm dần từ HF đến HI
=> (c) là HF, (a) là HCl, (b) là HBr và (d) là HI
Cho các phát biểu sau:
(1) Từ HF đến HI, tính acid tăng dần.
(2) Acid HCl thường được dùng để đánh sạch lớp oxide, hydroxide, muối carbonate bám trên bề mặt kim loại trước khi sơn, hàn, mạ điện dựa trên tính acid của HCl.
(3) Trong công nghiệp, hỗn hợp gồm KF và HF (có tỉ lệ mol tương ứng 3:1) được dùng để điện phân nóng chảy sản xuất fluorine.
(4) Acid HF phân li hoàn toàn trong nước, còn các acid HCl, HBr, HI phân li một phần trong nước.
Số phát biểu sai là
(3) sai. Trong công nghiệp, hỗn hợp gồm KF và HF (có tỉ lệ mol tương ứng 1:3) được dùng để điện phân nóng chảy sản xuất fluorine.
(4) sai. Từ HF đến HI, tính acid tăng dần nên HF phân li một phần, còn HCl, HBr, HI phân li hoàn toàn trong nước
Thứ tự sắp xếp tính khử theo chiều tăng dần là
Thứ tự sắp xếp tính khử theo chiều tăng dần là Cl-, Br-, I-
Cho các dung dịch sau: NaCl, KI, Mg(NO3)2, AgNO3. Chỉ dùng thuốc thử duy nhất là dung dịch HCl thì nhận biết được bao nhiêu dung dịch trên?

\(AgN{O_3} + NaCl \to AgCl \downarrow + NaN{O_3}\)
\(AgN{O_3} + KI \to AgI \downarrow + KN{O_3}\)
Cho 14,25 gam hỗn hợp NaX, NaY (X, Y là hai halogen ở hai chu kì liên tiếp) vào dung dịch AgNO3 có dư thu được 14,35 gam kết tủa. X và Y là
TH1: Gỉa sử X là F, Y là Cl
\( \Rightarrow {n_ \downarrow } = {n_{AgCl}} = \dfrac{{14,35}}{{143,5}} = 0,1mol\)
\(\begin{array}{*{20}{c}}{NaCl}\\{0,1}\end{array}\begin{array}{*{20}{c}} + \\{}\end{array}\begin{array}{*{20}{c}}{AgN{O_3}}\\{}\end{array}\begin{array}{*{20}{c}} \to \\{}\end{array}\begin{array}{*{20}{c}}{NaN{O_3}}\\{}\end{array}\begin{array}{*{20}{c}} + \\{}\end{array}\begin{array}{*{20}{c}}{AgCl}\\{0,1}\end{array}\)
\( \Rightarrow {n_{NaCl}} = 0,1.58,5 = 5,85g\)
TH2: Gọi hai nguyên tố X, Y là \(\mathop R\limits^ - \)
\(\begin{array}{*{20}{c}}{Na\mathop R\limits^\_ }\\{\dfrac{{14,25}}{{23 + \mathop R\limits^\_ }}}\end{array}\begin{array}{*{20}{c}} + \\{}\end{array}\begin{array}{*{20}{c}}{AgN{O_3}}\\{}\end{array}\begin{array}{*{20}{c}} \to \\{}\end{array}\begin{array}{*{20}{c}}{NaN{O_3}}\\{}\end{array}\begin{array}{*{20}{c}} + \\{}\end{array}\begin{array}{*{20}{c}}{Ag\mathop R\limits^\_ \downarrow }\\{\frac{{14,35}}{{108 + \mathop R\limits^\_ }}}\end{array}\)
\( \Rightarrow \dfrac{{14,25}}{{23 + \mathop R\limits^\_ }} = \dfrac{{14,35}}{{108 + \mathop R\limits^\_ }} \Rightarrow \mathop R\limits^\_ = 12089,5\) (Không có giá trị PTK của halogen nào thỏa mãn) (Loại)
X là F, Y là Cl

