Các liên kết biểu diễn bằng các đường nét đứt (liên kết X) như hình dưới đây có vai trò quan trọng trong việc làm bền chuỗi xoắn đôi DNA
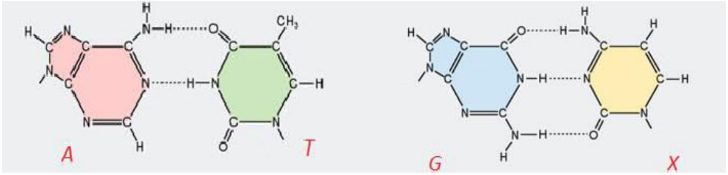
Liên kết X là loại liên kết gì?
Liên kết X là liên kết hydrogen
Mức độ liên kết hydrogen của hợp chất phụ thuộc vào
Mức độ liên kết hydrogen của hợp chất phụ thuộc vào trạng thái vật chất của hợp chất
Thứ tự nào sau đây thể hiện độ mạnh giảm dần của các liên kết?
Độ mạnh giảm dần của các liên kết là liên kết ion, liên kết cộng hoá trị, liên kết hydrogen, tương tác van der Waals.
Quy tắc octet không được sử dụng khi xem xét sự hình thành của loại liên kết nào sau đây?
Quy tác octet không được sử dụng khi xem xét sự hình thành của liên kết hydrogen và tương tác van der Waals.
Giữa các nguyên tử He có thể có loại liên kết nào?
Giữa các nguyên tử He có thể có tương tác van der Waals
Nguyên tố nào sau đây ít có khả năng tham gia liên kết hydrogen nhất?
Độ âm điện càng lớn thì mức độ phân cực của liên kết H-X càng lớn và khả năng tạo liên kết hydrogen giữa H của nguyên tử này với Y của nguyên tử khác dễ dàng hơn
Trong 3 nguyên tố trên S có độ âm điện nhỏ nhất
Giữa ancol ethanol, phenol, nước có 9 loại liên kết hydrogen. Loại liên kết nào sau đây bền nhất?
Liên kết hydrogen càng bền khi thành phần hydro mang điện tích dương nhất và Y mang điện tích âm nhất
=> Liên kết hydrogen giữa phenol và alcohol là bền nhất
Nguyên tử của nguyên tố X có cấu hình electron 1s22s22p63s1, nguyên tử của nguyên tố Y có cấu hình electron 1s22s22p63s23p5. Liên kết hóa học được hình thành giữa nguyên tử X và nguyên tử Y thuộc loại liên kết
Bước 1: Xác định X, Y
Cấu hình của X: 1s22s22p63s1 → X có số p = số e = 11 (hạt) → X là nguyên tố natri (Na).
Cấu hình của Y: 1s22s22p63s23p5 → Y có số p = số e = 17 (hạt) → Y là nguyên tố clo (Cl).
Bước 2: Xác định liên kết hình thành giữa X và Y
Vậy liên kết giữa kim loại điển hình Na và phi kim điển hình Cl là liên kết ion.
Nguyên tử của nguyên tố X có cấu hình electron 1s22s22p63s2, nguyên tử của nguyên tố Y có cấu hình electron 1s22s22p5. Liên kết hoá học giữa nguyên tử X và nguyên tử Y thuộc loại liên kết:
Bước 1: Xác định X, Y
X có cấu hình electron 1s22s22p63s2 => X thuộc nhóm IIA => KL điển hình
Y có cấu hình electron 1s22s22p5 => Y thuộc nhóm VIIA => PK điển hình
Bước 2: Xác định liên kết hình thành giữa X và Y
Liên kết hóa học giữa kim loại điển hình và phi kim điển hình là liên kết ion
Hoàn thành nội dung sau : “Số oxi hoá của một nguyên tố trong phân tử là ...(1)… của nguyên tử nguyên tố đó trong phân tử, nếu giả định rằng liên kết giữa các nguyên tử trong phân tử là ...(2)….”.
Số oxi hoá của một nguyên tố trong phân tử là điện tích của nguyên tử nguyên tố đó trong phân tử, nếu giả định rằng liên kết giữa các nguyên tử trong phân tử là liên kết ion
Chỉ ra nội dung sai khi nói về ion :
Ion âm là anion, ion dương là cation
=> Câu B sai
Liên kết ion là liên kết được hình thành bởi:
Liên kết ion là liên kết được hình thành bởi lực hút tĩnh điện giữa các ion mang điện trái dấu.
Hoàn thành nội dung sau : “Các ……….... thường tan nhiều trong nước. Khi nóng chảy và khi hoà tan trong nước, chúng dẫn điện, còn ở trạng thái rắn thì không dẫn điện”.
Các hợp chất ion thường tan nhiều trong nước. Khi nóng chảy và khi hoà tan trong nước, chúng dẫn điện, còn ở trạng thái rắn thì không dẫn điện”.
Vì hợp chất ion phân cực nên dễ tan trong nước (dung môi phân cực)
Cho dãy các chất: N2, H2, NH3, NaCl, HCl, H2O. Số chất trong dãy mà phân tử chỉ chứa liên kết cộng hóa trị không cực là
Liên kết cộng hóa trị không cực thông thường là liên kết giữa các nguyên tử của cùng một nguyên tố.
=> Các chất mà phân tử chỉ chứa liên kết cộng hóa trị không cực là N2, H2
Chất nào sau đây là hợp chất ion?
Hợp chất ion là hợp chất có chứa liên kết ion. Liên kết ion là liên kết được tạo thành do lực hút tĩnh điện giữa các ion mang điện tích trái dấu (thường là kim loại điển hình và phi kim điển hình)
B đúng vì K2O là hợp chất ion vì liên kết giữa K và O là liên kết ion.
A, C, D sai vì SO2, CO2, HCl là hợp chất cộng hóa trị vì liên kết trong hợp chất là liên kết cộng hóa trị giữa các phi kim S, O, C, H, Cl.
Hợp chất trong phân tử có liên kết ion là:
Liên kết ion là liên kết được tạo thành do lực hút tĩnh điện giữa các ion mang điện tích trái dấu.
A đúng vì:
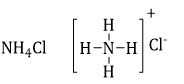
Phân tử NH4Cl chứa liên kết ion tạo thành do lực hút tĩnh điện giữa $NH_4^ + $ và $C{l^ - }$.
B, C, D sai vì liên kết trong phân tử NH3, HCl, H2O là liên kết cộng hóa trị.
Các chất mà phân tử không phân cực là:
A sai vì HBr là phân tử có cực.
C sai vì NH3 là phân tử có cực.
D sai vì HCl là phân tử có cực.
B đúng vì $Cl - Cl\,\,\,;\,\,\,O = C = O\,\,\,;\,\,\,CH \equiv CH$ là phân tử không phân cực.
Chú ý: liên kết C = O, C – H là liên kết cộng hóa trị phân cực.
Liên kết hóa học giữa các nguyên tử trong phân tử HCl thuộc loại liên kết
Liên kết trong phân tử HCl thuộc loại liên kết cộng hóa trị có cực do độ âm điện của H và Cl chênh lệch lớn, cặp electron dùng chung lệch về phía nguyên tử Cl.
Dãy gồm các chất trong phân tử chỉ có liên kết cộng hoá trị phân cực là:
A sai vì liên kết O=O trong O2 là liên kết cộng hóa trị không phân cực
B đúng vì liên kết H với O, H với F, H với S là liên kết cộng hóa trị phân cực
C sai vì liên kết O-O trong O3 là liên kết cộng hóa trị không phân cực
D sai vì liên kết Cl-Cl trong Cl2 là liên kết cộng hóa trị không phân cực
Liên kết hóa học giữa các nguyên tử trong phân tử NH3 là liên kết
- Liên kết của NH3 tạo bởi 2 phi kim khác nhau là N và H => Liên kết cộng hóa trị.
- Xác định hiệu độ âm điện:
${\Delta _{\chi {\kern 1pt} (N - H)}} = \left| {3,04 - 2,2} \right| = 0,84$
Ta có 0,4< 0,84< 1,7
=> liên kết cộng hóa trị phân cực

