Đốt cháy hoàn toàn m gam một chất béo X cần vừa đủ a mol O2, sau phản ứng thu được CO2 và b mol H2O. Biết m = 78a - 103b. Nếu cho c mol X tác dụng với dung dịch Br2 dư thì lượng Br2 phản ứng tối đa là 0,15 mol. Giá trị của c là
BTKL → mCO2 = mX + mO2 - mH2O = 11a - 121b
→ nCO2 = 2,5x - 2,75y (mol)
Bảo toàn O → nO(trong X) = 2nCO2 + nH2O - 2nO2 = 3x - 4,5y (mol)
X có 6O → nX = 1/6.nO(trong X) = 0,5x - 0,75y (mol)
Khi đốt hợp chất hữu cơ chứa C, H, O thì: \({n_{hchc}} = \frac{{{n_{C{O_2}}} - {n_{{H_2}O}}}}{{k - 1}}\) (với k là độ bất bão hòa của toàn phân tử)
\(\begin{array}{l} \to 0,5{\rm{x}} - 0,75y = \frac{{\left( {2,5{\rm{x}} - 2,75y} \right) - y}}{{k - 1}}\\ \to \left( {0,5{\rm{x}} - 0,75y} \right) = \frac{{5\left( {0,5{\rm{x}} - 0,75y} \right)}}{{k - 1}}\\ \to 1 = \frac{5}{{k - 1}}\\ \to k = 6\end{array}\)
=> X có chứa 6 liên kết π, mà có 3 π trong 3 nhóm COO
→ còn lại 3 π ngoài gốc hiđrocacbon
- Khi X phản ứng với Br2 thì X + 3Br2 → Sản phẩm cộng
→ nX = 1/3.nBr2 = 1/3.0,15 = 0,05 mol = a
Thủy phân hoàn toàn m gam chất béo bằng dung dịch NaOH đun nóng, thu được 9,20 gam glixerol và 91,80 gam muối. Giá trị của m là:
Phản ứng tổng quát: (RCOO)3C3H5 + 3NaOH → 3RCOONa + C3H5(OH)3
nGlixerol = 9,2 : 92 = 0,1 mol → nNaOH = 3nGlixerol = 0,3 mol
Bảo toàn khối lượng: m + mNaOH = mmuối + mglixerol
→ m = 91,8 + 9,2 - 0,3.40 = 89 gam
Xà phòng hoá hoàn toàn 35,6 gam chất béo X cần vừa đủ dung dịch chứa 0,12 mol NaOH. Cô cạn dung dịch sau phản ứng, thu được m gam muối. Giá trị của m là
Phản ứng thủy phân chất béo: (RCOO)3C3H5 + 3NaOH → 3RCOONa + C3H5(OH)3
Ta luôn có: n Glixerol = 1/3.nNaOH = 0,04 mol
BTKL: m muối = m chất béo + mNaOH - m glixerol
= 35,6 + 0,12.40 - 0,04.92 = 36,72 (g)
Số đồng phân este ứng với công thức phân tử C3H6O2 là
\(k = \pi + v = {{3.2 + 2 - 6} \over 2} = 1\)→ Este no, đơn chức, mạch hở
(1) HCOOCH2CH3
(2) CH3COOCH3
Este nào sau đây khi thủy phân với dung dịch NaOH tạo ra hai muối?
CH3COO(CH2)2OOCCH3+ 2NaOH → 2CH3COONa + CH2OH-CH2OH
CH3OOC-COOCH3 + 2NaOH → (COONa)2 + 2CH3OH
C6H5COOCH3 + NaOH → C6H5COONa + CH3OH
CH3COOC6H5 + 2NaOH → CH3COONa + C6H5ONa + H2O
Khi cho 0,03 mol este đơn chức X tác dụng với dung dịch NaOH (dư), sau khi phản ứng kết thúc thì lượng NaOH phản ứng là 2,4 gam và 5,94 gam tổng sản phẩm các chất hữu cơ. Số đồng phân cấu tạo của X thoả mãn các tính chất trên là
\({n_{NaOH}} = {{2,4} \over {40}} = 0,06\,\,mol\) => nNaOH = 2. neste
→ este của phenol RCOOC6H4R’
RCOOC6H4R’ +2NaOH → RCOONa + R’C6H4ONa + H2O
meste = msản phẩm hữu cơ + mH2O - mNaOH = 5,94+ 0,03.18 – 2,4 = 4,08 g
${M_{Este}} = {{4,08} \over {0,03}}$= 136→ C8H8O2
=> CTCT của X:
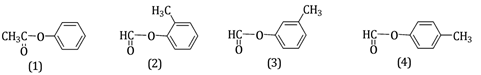
Thủy phân chất X bằng dung dịch NaOH, thu được hai chất Y và Z (trong đó Z tráng bạc Y không tráng bạc). Z tác dụng được với Na sinh ra khí H2. Chất X là
Z vừa có phản ứng tráng bạc, vừa tác dụng được với Na => Z chứa gốc –CHO và –OH
Y không tráng bạc => X có dạng R’COOCH=CH-R-OH hoặc R’COO-CH2-RCHO
Từ 4 đáp án => X là CH3COO-CH2CHO
PTHH: CH3COO-CH2CHO + NaOH → CH3COONa + HO-CH2CHO
Số đồng phân este ứng với công thức phân tử C4H8O2 là
$k = \pi + v = \dfrac{{2.4 + 2 - 8}}{2} = 1$ → Este no, đơn chức, mạch hở
(1) HCOOCH2CH2CH3
(2) HCOOCH(CH3)2
(3) CH3COOCH2CH3
(4) CH3CH2COOCH3
Vai trò của quá trình thoát hơi nước ở thực vật là
Thoát hơi nước là động lực đầu trên của sự vận chuyển nước, ion khoáng từ rễ lên thân và lá.
Có mấy tác nhân ngoại cảnh sau đây ảnh hưởng đến quá trình thoát hơi nước ở cây?
I.Các ion khoáng II. Ánh sáng
III. Nhiệt độ IV. Gió V. Nước
Tất cả các nhân tố trên đều ảnh hưởng tới quá trình thoát hơi nước ở cây.
Khi cho 0,15 mol este đơn chức X tác dụng với dung dịch NaOH (dư), sau khi phản ứng kết thúc thì lượng NaOH phản ứng là 12 gam và tổng khối lượng sản phẩm hữu cơ thu được là 29,7 gam. Số đồng phân cấu tạo của X thoả mãn các tính chất trên là
${n_{NaOH}} = \dfrac{{12}}{{40}} = 0,3\,\,mol = 2{n_{{\text{es}}te}}$ → este của phenol RCOOC6H4R’
RCOOC6H4R’ +2NaOH $\xrightarrow{{}}$ RCOONa + R’C6H4ONa + H2O
meste = msản phẩm hữu cơ + mH2O - mNaOH
= 29,7 + 0,15.18 – 12 = 20,4 g
${{\text{M}}_{{\text{es}}te}} = \dfrac{{20,4}}{{0,15}} = 136$→ C8H8O2
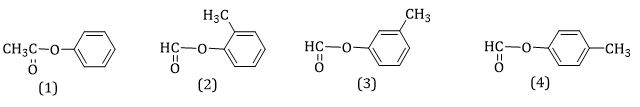
Trong mô thực vật có bao nhiêu con đường liên kết NH3 với các hợp chất hữu cơ?
Trong mô thực vật có 3 con đường liên kết NH3 với các hợp chất hữu cơ: amin hóa, chuyển vị amin và hình thành amit
Este nào sau đây khi phản ứng với dung dịch NaOH dư, đun nóng không tạo ra hai muối?
C6H5COOC6H5 + 2NaOH → C6H5COONa + C6H5ONa + H2O
CH3COO-[CH2]2-OOCCH2CH3 + 2NaOH → CH3COONa + CH3CH2COONa + CH2OH-CH2OH
CH3OOC-COOCH3 + 2NaOH → (COONa)2 + 2CH3OH
CH3COOC6H5 + 2NaOH → CH3COONa + C6H5ONa + H2O
Xét các trường hợp sau
(1) những cơn giông: N2 + O2 → NO2 (tia lửa điện)
(2) xác của động vật, thực vật: RNH2→ NH3 → NO3-
(3) sự cố định của vi sinh vật: N2 + NH3 → 2 NH3
(4) sự cung cấp của con người: muối NO3-, NH4+
(5) quang hợp của cây xanh
Những trường hợp nào trên đây là nguồn cung cấp nitơ cho cây?
(1), (2), (3) và (4) là các con đường tạo ra nitơ dưới dạng mà cây hấp thụ được hoặc các chất có thể tạo ra dạng nitơ đó.
Thủy phân chất X bằng dung dịch NaOH, thu được hai chất Y và Z đều có phản ứng tráng bạc, Z tác dụng được với Na sinh ra khí H2. Chất X là
Z vừa có phản ứng tráng bạc, vừa tác dụng được với Na => Z chứa gốc –CHO và –OH
=> X có dạng HCOOCH=CH-R-OH hoặc HCOO-CH2-RCHO
Từ 4 đáp án => X là HCOO-CH2CHO
PTHH: HCOO-CH2CHO + NaOH → HCOONa + HO-CH2CHO
Khi nói về quá trình quang hợp ở thực vật, phát biểu nào sau đây đúng?
Phát biểu đúng là B
Ý D sai vì O2 được tạo từ H2O
Thực hiện phản ứng xà phòng hoá chất hữu cơ X đơn chức với dung dịch NaOH thu được một muối Y và ancol Z. Đốt cháy hoàn toàn 2,07 gam Z cần 3,024 lít O2 (đktc) thu được lượng CO2 nhiều hơn khối lượng nước là 1,53 gam. Nung Y với vôi tôi xút thu được khí T có tỉ khối so với không khí bằng 1,03. CTCT của X là:
- Theo đề bài: X đơn chức, tác dụng với NaOH sinh ra muối và ancol
=> X là este đơn chức: RCOOR’.
- Mặt khác: \({m_X} + {m_{{O_2}}} = {m_{C{O_2}}} + {m_H}_{_2O} \Rightarrow 44.{\text{ }}{n_{C{O_2}}} + 18.{n_{{H_2}O}} = 2,07 + 0,135.32 = 6,39\) gam
Và \(44.{n_{C{O_2}}} - 18.{n_H}_{_2O} = 1,53{\text{ }}gam \Rightarrow {n_{C{O_2}}} = 0,09{\text{ }}mol;{\text{ }}{n_H}_{_2O} = 0,135{\text{ }}mol\)
\({n_H}_{_2O} > {n_{C{O_2}}}\) => Z là ancol no, đơn chức, mạch hở có công thức: CnH2n+1OH (n ≥ 1)
Từ phản ứng đốt cháy Z => \(\dfrac{{{n_{{H_2}O}}}}{{{n_{C{O_2}}}}} = \dfrac{{n + 1}}{n} = \dfrac{{0,135}}{{0,09}} \Rightarrow n = 2\)
Y có dạng CxHyCOONa => T: CxHy+1 => MT = 12x + y + 1 = 1,03.29
=> x = 2 và y = 6 => CTPT este: C2H5COOC2H5
Có bao nhiêu phát biểu sau đây đúng, khi nói về quá trình quang hợp ở thực vật?:
I. Ở thực vật C3 sản phẩm đầu tiên của giai đoạn cố định CO2 là hợp chất AlPG.
II. Thực vật C4 và thực vật CAM có 2 loại lục lạp ở tế bào mô giậu và tế bào bao bó mạch
III. Sản phẩm đầu tiên trong giai đoạn cố định CO2 ở thực vật CAM là một hợp chất 4C.
IV. Sản phẩm trong pha sáng của quá trình quang hợp gồm có ATP, NADPH, O2
Các phát biểu đúng là: III, IV
I sai vì sản phẩm đầu của quá trình cố định CO2 ở thực vật C3 là hợp chất APG
II sai vì chỉ có thực vật C4 có 2 loại lục lạp ở tế bào mô giậu và tế bào bao bó mạch
Đun 20,4 gam một chất hữu cơ A đơn chức với 300 ml dung dịch NaOH 1M thu được muối B và hợp chất hữu cơ C. Cho C phản ứng với Na dư thu được 2,24 lít H2 (đktc). Nung B với NaOH rắn thu được khí D có tỉ khối đối với O2 bằng 0,5. Khi oxi hóa C bằng CuO được chất hữu cơ E không phản ứng với AgNO3/NH3. Xác định CTCT của A?
Chất C tác dụng với Na sinh ra khí H2 => C là ancol
Oxi hóa C ra E không phản ứng với AgNO3 => C không là ancol bậc 1
Dựa vào các đáp án cho A là este đơn chức => B là muối của Na
Nung B với NaOH rắn tạo ra D có MD = 32.0,5 = 16 => D là CH4 => Gốc R trong D là CH3-
Đặt công thức của A là RCOOR’
CH3COOR’ + NaOH → CH3COONa + R’OH
R’OH + Na → R’ONa + H2
Ta có: nH2 = 0,1 mol => nancol = 2.0,1 = 0,2 mol
nNaOH = 0,3 mol > nancol => NaOH dư, este phản ứng hết
=> neste = nancol = 0,2 mol => ${M_{este}} = \dfrac{{20,4}}{{0,2}} = 102$
=> R’ = 102 – 59 = 43 => gốc R’ là C3H7- và ancol bậc 2
Một cây C3 và một cây C4 được đặt trong cùng một chuông thủy tinh kín được chiếu sáng. Nồng độ CO2 sẽ
Vì cây C4 có điểm bù CO2 thấp hơn cây C3 nên cây C4 có thể quang hợp ở nồng độ CO2 thấp hơn so với cây C3 →nồng độ CO2 sẽ giảm đến điểm bù của cây C4.

