Hai este X, Y có cùng công thức phân tử C8H8O2 và chứa vòng benzen. Cho 0,25 mol hỗn hợp gồm X và Y tác dụng tối đa với 0,3 mol NaOH trong dung dịch, thu được dung dịch Z chứa 23,5 gam ba muối.
Khối lượng muối của phenol có trong Z là:
Khối lượng muối của phenol có trong Z là:
Bước 1: Tính số mol X, Y trong hỗn hợp
- Ta thấy 1 < nNaOH : nhh = 0,3 : 0,25 = 1,2 < 2
⟹ Trong hỗn hợp có 1 este của phenol (giả sử là X) và 1 este thường (giả sử là Y).
- Gọi neste của phenol = a mol, neste thường = b mol.
Ta có hệ phương trình \(\left\{ \begin{array}{l}X:{a^{mol}}\\Y:{b^{mol}}\end{array} \right. \to \left\{ \begin{array}{l}{n_{hh}} = a + b = 0,25\\{n_{NaOH}} = 2{\rm{a}} + b = 0,3\end{array} \right. \to \left\{ \begin{array}{l}a = 0,05\\b = 0,2\end{array} \right.\)
Bước 2: Tính khối lượng muối do X sinh ra
- PTHH: X + 2NaOH → Muối 1 + Muối 2 + H2O
0,05 → 0,05 → 0,05 → 0,05 (mol)
- Tổng khối lượng muối 1 và muối 2 = 0,05.136 + 0,1.40 - 0,05.18 = 9,9 gam.
Bước 3: Tìm CTCT muối Y, biện luận tìm X
- Khối lượng muối do Y tác dụng với NaOH tạo ra là 23,5 - 9,9 = 13,6 gam.
⟹ Mmuối do Y = 13,6 : 0,2 = 68 (HCOONa).
- Do sau phản ứng thu được 3 muối nên X phải sinh ra 2 muối khác HCOONa
⟹ X là CH3COOC6H5.
Bước 4: Tính khối lượng muối của phenol
Muối của phenol trong Z là C6H5ONa (0,05 mol)
⟹ mmuối của phenol = 0,05.116 = 5,8 gam.
Cho 5,94 gam hỗn hợp E gồm hai este mạch hở X và Y (đều tạo bởi axit cacboxylic và ancol, MX < MY < 150) tác dụng vừa đủ với dung dịch NaOH, thu được ancol Z và 6,74 gam hỗn hợp muối T. Cho toàn bộ Z tác dụng với một lượng dư Na thu được 1,12 lít khí H2 (đktc). Đốt cháy toàn bộ T thu được H2O, Na2CO3 và 0,05 mol CO2.
Phần trăm khối lượng của X trong E là:
Phần trăm khối lượng của X trong E là:
- Sơ đồ bài toán:
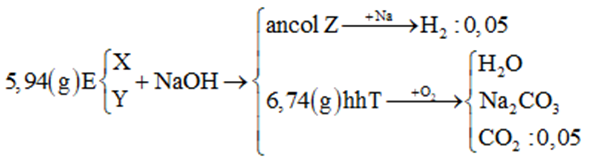
Bước 1: Tìm CTPT của Z
- nH2 = 0,05 mol ⟹ nOH(ancol) = 2nH2 = 0,1 mol = nNaOH(pư).
BTKL: mZ = 5,94 + 0,1.40 - 6,74 = 3,2 gam.
Đặt ancol Z: R(OH)x (\(\dfrac{{0,1}}{x}\)mol) ⟹ \(\dfrac{{0,1}}{x}\).(R + 17x) = 3,2 ⟹ R = 15x ⟹ x = 1; R = 15 (CH3-) thỏa mãn.
Vậy Z là CH3OH.
Bước 2: Tìm CTPT của hh muối T
- BTNT "Na" ⟹ nNa2CO3 = ½nNaOH = 0,05 mol
⟹ nC(muối) = nNa2CO3 + nCO2 = 0,05 + 0,05 = 0,1 mol
- Nhận thấy nC = nNa ⟹ Muối gồm HCOONa (a mol) và (COONa)2 (b mol) (vì MX,Y < 150).
Bước 3: Tính %mX
- Ta có hệ phương trình: \(\left\{ \begin{array}{l}a + 2b = 0,1\left( {BT:Na} \right)\\68{\rm{a}} + 134b = {m_{muoi}} = 6,74\end{array} \right. \to \left\{ \begin{array}{l}a = 0,04\\b = 0,03\end{array} \right.\)
⟹ \(E\left\{ {\begin{array}{*{20}{l}}{X:HCOOC{H_3}\left( {0,04} \right)}\\{Y:{{\left( {COOC{H_3}} \right)}_2}\left( {0,03} \right)}\end{array}} \right.\)
⟹ %mX = 40,40%.
Hỗn hợp X gồm 2 este đơn chức (không chứa nhóm chức nào khác). Cho 0,08 mol X tác dụng hết với dung dịch AgNO3/NH3 thu được 0,16 mol Ag. Mặt khác thủy phân hoàn toàn 0,08 mol X bằng dung dịch NaOH dư thu được dung dịch chứa 9,34 gam hỗn hợp 2 muối và 1,6 gam CH3OH.
Phần trăm khối lượng este có phân tử khối lớn hơn trong X là:
Phần trăm khối lượng este có phân tử khối lớn hơn trong X là:
Bước 1: Đặt X là RCOOR’, xác định R.
- X + AgNO3:
Ta thấy nAg : nX = 2 : 1 ⟹ Cả 2 este đều có đầu HCOO-.
Bước 2: Xác định CTCT của 2 este
- X + NaOH:
+ Do thu được CH3OH ⟹ 1 este là HCOOCH3 ⟹ nHCOOCH3 = nCH3OH = 1,6/32 = 0,05 mol.
+ Sau phản ứng thu được 2 muối ⟹ este còn lại là este của phenol có dạng HCOOC6H4Y
\(\begin{array}{l}X\left\{ {\begin{array}{*{20}{l}}{HCOOC{H_3}:0,05}\\{HCOO{C_6}{H_4}Y:0,03}\end{array}} \right.\\ \to Muối{\mkern 1mu} {\mkern 1mu} \,gồm:\begin{array}{*{20}{l}}{HCOON{\rm{a}}:0,08{\mkern 1mu} mol}\\{Y{C_6}{H_4}ON{\rm{a}}:0,03{\mkern 1mu} mol}\end{array}\end{array}\)
⟹ mmuối = 0,08.68 + 0,03.(Y + 115) = 9,34 ⟹ Y = 15 (CH3-)
Bước 3: Tính %m este có PTK lớn hơn trong X
- \(X\left\{ \begin{array}{l}HCOOC{H_3}:0,05\\HCOO{C_6}{H_4}C{H_3}:0,03\end{array} \right.\)
⟹ %mHCOOC6H4CH3 = \(\dfrac{{0,03.136}}{{0,05.60 + 0,03.136}}.100\% \) = 57,63%.
Đốt cháy hoàn toàn 6,46 gam hỗn hợp E gồm ba este no, mạch hở X, Y, Z (đều tạo bởi axit cacboxylic và ancol, MX < MY < MZ < 248) cần vừa đủ 0,235 mol O2, thu được 5,376 lít khí CO2. Cho 6,46 gam E tác dụng hết với dung dịch NaOH (lấy dư 20% so với lượng phản ứng) rồi chưng cất dung dịch, thu được hỗn hợp hai ancol đồng đẳng kế tiếp và hỗn hợp chất rắn khan T. Đốt cháy hoàn toàn T, thu được Na2CO3, CO2 và 0,18 gam H2O.
Phân tử khối của Y là:
Phân tử khối của Y là:
Bước 1: Xác định CTCT của 2 muối trong T
- Xét E + O2 ⟶ CO2 + H2O
BTKL ⟹ mH2O = 3,42 gam ⟹ nH2O = 0,19 mol.
BTNT O ⟹ nO(E) = 2nCO2 + nH2O - 2nO2 = 0,2 mol ⟹ n-COO-(E) = 0,1 mol.
- Xét E + NaOH
⟹ nNaOH(pứ) = n-COO-(E) = 0,1 mol.
⟹ nNaOH(dư trong T) = 0,1.20%/100% = 0,02 mol.
* Xét đốt cháy T gồm 0,02 mol NaOH ⟶ 0,01 mol H2O
BTNT H ⟹ nNaOH = 2nH2O ⟹ muối trong T không chứa H mà 3 este trong E no, mạch hở
⟹ Axit tạo nên este trong E là (COOH)2 và 2 ancol tạo E đồng đẳng no, đơn chức, mạch hở.
Ta có muối trong T là (COONa)2 có n(COONa)2 = nNaOH(pứ)/2 = 0,05 mol.
⟹ mT = m(COONa)2 + nNaOH(dư) = 7,5 gam.
Bước 2: Xác định CTCT của 2 ancol trong T
- Xét E + NaOH ⟶ T + ancol
BTKL ⟹ mancol = mE + mNaOH - mT = 6,46 + 0,12.40 - 7,5 = 3,76 gam.
Lại có nancol = nNaOH(pứ) = 0,1 mol.
⟹ MTB(ancol) = 37,6/0,1 = 37,6 ⟹ Hỗn hợp hai ancol là CH3OH và C2H5OH.
Bước 3: Xác định CTCT của Y, tính MY.
- Hỗn hợp E gồm ba este no, mạch hở X, Y, Z (MX < MY < MZ < 248)
⟹ X là (COOCH3)2 ; Y là CH3OOC-COOC2H5 và Z là (COOC2H5)2.
⟹ MY = 132.
Hỗn hợp E gồm ba este no, mạch hở X, Y, Z (MX < MY < MZ) trong đó có hai este đơn chức và một este hai chức). Đốt cháy hoàn toàn 10,86 gam E trong O2 thu được H2O và 0,44 mol CO2. Mặt khác, cho 10,86 gam E phản ứng vừa đủ với dung dịch NaOH, thu được hỗn hợp T gồm ba ancol và dung dịch chứa 11,88 gam hỗn hợp hai muối của 2 axit đồng đẳng kế tiếp. Toàn bộ T cho vào bình đựng Na dư, sau phản ứng thấy khối lượng bình tăng 4,83 gam.
Phần trăm khối lượng của Y trong E là:
Phần trăm khối lượng của Y trong E là:
Bước 1: Xác định CTCT của 2 muối của 2 axit đồng đẳng kế tiếp
- Đặt nNaOH = e ⟹ nOH(ancol) = e ⟹ nH2 = 0,5e.
mtăng = mancol - mH2 ⟹ mancol = e + 4,83.
- Bảo toàn khối lượng phản ứng:
mE + mNaOH = mmuối + mancol ⟹ 10,86 + 40e = 11,88 + e + 4,83 ⟹ e = 0,15 mol
- Mmuối = 11,88/0,15 = 79,2 ⟹ 2 muối là HCOONa; CH3COONa.
Bước 2: Tính số mol 2 muối của 2 axit đồng đẳng kế tiếp
- Ta có: nHCOONa + nCH3COONa = nNaOH (1)
68.nHCOONa + 82.nCH3COONa = 11,88 (2)
Từ (1) (2) nHCOONa = 0,03 mol; mCH3COONa = 0,12 mol
Bước 3: Quy đổi hỗn hợp ancol, tính số mol các chất
- Quy đổi ancol thành CH3OH (a); C2H4(OH)2 (b) và CH2 (c).
+) nNaOH = a + 2b = 0,15
+) mancol = 32a + 62b + 14c = 4,83 + 0,15 = 4,98
+) nC (ancol) = a + 2b + c = 0,44 - nC (muối) = 0,44 - 0,03 - 0,12.2 = 0,17
⟹ nCH3OH = a = 0,05 mol; nC2H4(OH)2 = b = 0,05 mol và nCH2 = c = 0,02 mol
Bước 4: Xác định CTCT X, Y, Z. Tính %mY
- Hỗn hợp ancol chứa 0,05 mol C2H4(OH)2
Mà nHCOONa = 0,03 mol < nC2H4(OH)2 = 0,05 mol
⟹ Este đa chức là (CH3COO)2C2H4 (0,05).
- Còn lại HCOONa (0,03); CH3COONa (0,02); CH3OH (0,05) và CH2 (0,02) của các este đơn chức tạo ra.
Do c < 0,03 và c = 0,02 nên các este đơn chức là:
X là HCOOCH3 (0,03); Y là CH3COOC2H5 (0,02).
⟹ %mY = 16,20%.
Hỗn hợp E gồm ba este đều đơn chức X, Y, Z (MX < MY < MZ). Cho 0,09 mol hỗn hợp E tác dụng với một lượng vừa đủ tối đa 0,11 lít dung dịch NaOH 1M, cô cạn hỗn hợp sau phản ứng thu được hỗn hợp hơi G gồm một anđehit, một ancol và phần rắn chứa 9,7 gam 2 muối. Chia G thành 2 phần bằng nhau: Phần một cho vào dung dịch AgNO3 dư/NH3 thu được 4,32 gam Ag. Đốt cháy hoàn toàn phần 2, thu được 0,07 mol CO2.
Phần trăm khối lượng của este Y trong E là:
Phần trăm khối lượng của este Y trong E là:
Bước 1: Biện luận xác định thành phần và tính số mol các chất trong hh của este
- Ta thấy 1 < nNaOH/nE = 1,22 < 2 ⟹ hỗn hợp có este thường và este của phenol.
- Gọi neste thường = a; neste phenol = b
⟹ a + b = 0,09 mol và nNaOH = a + 2b = 0,11
⟹ neste thường ancol = 0,07 mol; neste phenol = 0,02 mol
Bước 2: Xác định CTCT chung của 2 muối
- Phần 1: nAg = 0,04 mol ⟹ nanđehit = 0,02 mol
⟹ nancol = 0,035 - 0,02 = 0,015 mol.
- Phần 2: Gọi số C trong anđehit và ancol lần lượt là x và y
⟹ nCO2 = 0,02x + 0,015y = 0,07 ⟹ x = y = 2
⟹ CH3CHO và C2H5OH.
- Hỗn hợp chỉ gồm có 2 muối ⟹ 3 este cùng chung 1 gốc axit ACOONa (0,09 mol) và muối phenol: BONa (0,02 mol)
mmuối = mACOONa + mBONa = 9,7 ⟹ 9A + 2B = 289
⟹ A = 15 (CH3-) và B = 77 (C6H5-)
Bước 3: Tính %mY trong E.
- Vậy hỗn hợp E gồm:
X: CH3COOC2H5 (0,03 mol)
Y: CH3COOCH=CH2 (0,04 mol)
Z: CH3COOC6H5 (0,02 mol)
⟹ %mY = 30%.
Hỗn hợp E gồm 2 este: X đơn chức và Y hai chức (X, Y chỉ chứa nhóm chức este, mạch hở). Đốt cháy hoàn toàn m gam E trong oxi dư thu được 1,85 mol CO2. Mặt khác, m gam E tác dụng vừa đủ với dung dịch NaOH thu được 37 gam hỗn hợp Z gồm 2 muối và hỗn hợp T gồm 2 ancol (2 ancol đều có khả năng tách nước tạo anken). Đốt cháy hoàn toàn 37 gam hỗn hợp Z thu được H2O, 0,275 mol CO2 và 0,275 mol Na2CO3. Phần trăm khối lượng của Y trong E gần nhất với giá trị nào sau đây?
Bước 1: Xác định CTCT 2 muối Z
- Đốt hỗn hợp muối Z:
+ Bảo toàn C: nC (muối) = nCO2 + nNa2CO3 = 0,55 mol
+ Bảo toàn Na: nNa = 2.nNa2CO3 = 0,55 mol
Ta thấy số C = số Na ⟹ hai muối là HCOONa và (COONa)2.
- Đặt nHCOONa = a; n(COONa)2 = b
+ Bảo toàn Na: a + 2b = 0,55 (1)
+ mmuối = 68a + 134b = 37 (2)
Từ (1), (2) ⟹ nHCOONa = a = 0,15 mol; n(COONa)2 = b = 0,2 mol.
Bước 2: Biện luận, dự đoán CTCT 2 ancol T
- Các ancol tách nước tạo anken ⟹ Hai ancol no, đơn chức, mạch hở (từ C2H5OH trở lên).
Bước 3: Xác định CTCT 2 este X, Y
- Gọi công thức 2 este là HCOOC2H5.xCH2 (0,15 mol) và (COOC2H5)2.yCH2 (0,2 mol)
Bước 4: Tính %mY trong E.
- Bảo toàn C: nCO2 = 0,15.(x + 3) + 0,2.(y + 6) = 1,85
⟹ 3x + 4y = 4 ⟹ x = 0; y = 1 thỏa mãn
⟹ 2 este là HCOOC2H5 và C2H5OOC-COOC3H7.
⟹ %mY = 74,246%.
Cho 9,38 gam hỗn hợp X1 gồm: đimetyl ađipat; anlyl axetat; glixerol triaxetat và phenyl benzoat thủy phân hoàn toàn trong dung dịch KOH dư, đun nóng, thu được a gam hỗn hợp muối và 2,43 gam hỗn hợp X2 gồm các ancol. Cho toàn bộ hỗn hợp X2, thu được ở trên tác dụng với K dư, thu được 0,728 lít H2 (ở đktc). Mặt khác, đốt cháy hoàn toàn 9,38 gam hỗn hợp X1 bằng O2 dư, thu được 11,312 lít CO2 (ở đktc) và 5,4 gam H2O. Giá trị a gần nhất với giá trị nào sau đây?
Bước 1: Tính số mol của COO trong hỗn hợp X1
- Đốt X1: nCO2 = 0,505 mol; nH2O = 0,3 mol
⟹ nO(X1) = (mX - mC - mH)/16 = 0,17 mol
⟹ nCOO = 0,085 mol (do nhóm COO có 2 nguyên tử O)
Bước 2: Tính nKOH phản ứng
- Khi ancol tác dụng với K:
nOH(ancol) = 2nH2 = 0,065 mol
⟹ nCOO(phenol) = 0,085 - 0,065 = 0,02 mol
⟹ nH2O = 0,02 mol ⟹ nKOH pư = 0,065 + 0,02.2 = 0,105 mol
Bước 3: Tính a
Bảo toàn khối lượng: mX1 + mKOH pư = mmuối + mX2 + mH2O
⟹ 9,38 + 0,105.56 = a + 2,43 + 0,02.18
⟹ a = 12,47 gam.
X, Y là hai este đều đơn chức, mạch hở, trong phân tử có 2 liên kết π, (MX < MY); Z là este no, hai chức, mạch hở. Đun nóng hỗn hợp E chứa X, Y, Z với dung dịch NaOH vừa đủ, thu được hỗn hợp M chứa 2 muối và hỗn hợp G chứa 2 ancol đồng đẳng kế tiếp. Đun nóng toàn bộ G với H2SO4 đặc ở 140oC (giả sử hiệu suất đạt 100%) thu được 19,35 gam hỗn hợp 3 ete. Đốt cháy toàn bộ M cần dùng 1,675 mol O2, thu được CO2, 0,875 mol H2O và 0,375 mol Na2CO3.
Phần trăm khối lượng của Y có trong hỗn hợp E là:
Phần trăm khối lượng của Y có trong hỗn hợp E là:
Bước 1: Xác định CTCT các hợp chất của G
- Do sau phản ứng thu được 2 ancol đồng đẳng kế tiếp nên các ancol phải là đơn chức.
Mà thu được 2 muối (trong đó có 1 muối 2 chức) nên 2 este đơn chức phải có chung gốc axit.
- Bảo toàn Na: nNaOH = 2nNa2CO3 = 0,75 mol
⟹ nancol G = nNaOH = 0,75 mol
⟹ nH2O (pư ete hóa) = ½.nancol G = 0,375 mol
- BTKL cho pư ete hóa: mancol G = mete + mH2O = 19,35 + 0,375.18 = 26,1 gam
⟹ \({\bar M_G} = \dfrac{{26,1}}{{0,75}} = 34,8\)
⟹ CH3OH (0,6 mol) và C2H5OH (0,15 mol) (giải hệ số mol và khối lượng hỗn hợp G để tìm mol mỗi ancol)
Bước 2: Tính số mol các muối M
- Quy đổi hỗn hợp muối thành:
\(\left\{ \begin{array}{l}C{H_2} = CHCOON{\rm{a}}:a\\{(COON{\rm{a}})_2}:b\\C{H_2}:c\end{array} \right. + {O_2}:1,675 \to \left\{ \begin{array}{l}N{a_2}C{O_3}:0,375\\C{O_2}:3{\rm{a}} + 2b + c - 0,375(BT.C)\\{H_2}O:0,875\end{array} \right.\)
+) Bảo toàn Na: a + 2b = 0,75
+) Bảo toàn H: 3a + 2c = 2.0,875
+) Bảo toàn O: 2a + 4b + 2.1,675 = 3.0,375 + 2.(3a + 2b + c - 0,375) + 0,875
Giải hệ trên được a = 0,35; b = 0,2; c = 0,35.
Bước 3: Tính %mY
Từ \(\left\{ \begin{array}{l}C{H_2} = CHCOON{\rm{a}}:0,35\\{(COON{\rm{a}})_2}:0,2\\C{H_2}:0,35\end{array} \right. \Rightarrow M\left\{ \begin{array}{l}{C_3}{H_5}COON{\rm{a}}:0,35\\{(COON{\rm{a}})_2}:0,2\end{array} \right.\)
Kết hợp thành phần muối và thành phần ancol ta suy ra:
\(E\left\{ \begin{array}{l}X:{C_3}{H_5}COOC{H_3}\left( {0,6 - 0,2.2 = 0,2} \right)\\Y:{C_3}{H_5}COO{C_2}{H_5}\left( {0,15} \right)\\Z:{\left( {COOC{H_3}} \right)_2}\left( {0,2} \right)\end{array} \right.\)
⟹ %mY(E) = 28,17%.
Cho 35,04 gam hỗn hợp X gồm ba este đều đơn chức tác dụng tối đa với 560 ml dung dịch NaOH 1,0M thu được a gam hỗn hợp Y gồm hai ancol no, mạch hở và b gam hỗn hợp muối Z (phân tử các muối chỉ chứa một nhóm chức). Đun nóng a gam Y với H2SO4 đặc ở 140oC thu được 6,64 gam hỗn hợp T gồm ba ete. Hóa hơi hoàn toàn lượng T nói trên thu được thể tích hơi bằng thể tích của 3,36 gam N2 (ở cùng điều kiện nhiệt độ, áp suất). Biết các phản ứng đều xảy ra hoàn toàn.
Cho biết nguyên tử khối của các nguyên tố: H = 1; C = 12; N= 14; O = 16; Na = 23; S = 32.)
Giá trị của b bằng:
Cho biết nguyên tử khối của các nguyên tố: H = 1; C = 12; N= 14; O = 16; Na = 23; S = 32.)
Giá trị của b bằng:
Bước 1: Xác định CT chung của este X
- Xét Y ⟶ T (ete) + H2O
Ta có: VT = V(3,36 gam N2) ⟹ nT = nN2 = 3,36/28 = 0,12 mol.
Luôn có: nH2O = nT = 0,12 mol và nY = 2nT = 0,24 mol.
Bảo toàn khối lượng ⟹ mY = mT + mH2O = 8,8 gam.
- Nhận thấy nY = 0,24 mol < nNaOH = 0,56 mol
Mà Y gồm 2 ancol no, đơn chức, mạch hở ⟹ X chứa este có dạng RCOOC6H4R' và R1COOR1'
Bước 2: Tính số mol các chất trong hỗn hợp muối Z
- Xét X + NaOH

Bảo toàn khối lượng ⟹ mX + mNaOH = mY + mZ + mH2O
Bước 3: Tính giá trị của b
Vậy b = mZ = 35,04 + 0,56.40 - 8,8 - 0,16.18 = 45,76 gam.
Hỗn hợp E gồm ba este mạch hở, đều có bốn liên kết pi (π) trong phân tử, trong đó có một este đơn chức là este của axit metacrylic và hai este hai chức là đồng phân của nhau. Đốt cháy hoàn toàn 12,22 gam E bằng O2, thu được 0,37 mol H2O. Mặt khác, cho 0,36 mol E phản ứng vừa đủ với 234 ml dung dịch NaOH 2,5M, thu được hỗn hợp X gồm các muối của các axit cacboxylic không no, có cùng số nguyên tử cacbon trong phân tử; hai ancol không no, đơn chức có khối lượng m1 gam và một ancol no, đơn chức có khối lượng m2 gam. Tỉ lệ m1 : m2 có giá trị gần nhất với giá trị nào sau đây?
Bước 1: Tính n este đơn chức và n este hai chức trong phản ứng thủy phân hh E
- nNaOH = 0,234.2,5 = 0,585 mol
- Xét phản ứng thủy phân hỗn hợp E trong NaOH:
- Đặt n este đơn chức = x và n este hai chức = y (mol)
⟹ nE = x + y = 0,36 mol và nNaOH = x + 2y = 0,585
Giải hệ thu được x = 0,135 và y = 0,225
⟹ x : y = 3 : 5
Bước 2: Tính n este đơn chức và n este hai chức trong phản ứng đốt cháy E
- Xét phản ứng đốt cháy E:
Do X, Y đều chứa 4 liên kết π nên ta giả sử E gồm:
CnH2n-6O2 (3a mol) và CmH2m-6O4 (5a mol)
- nCO2 - nH2O = 3nE ⟹ nCO2 - 0,37 = 3.8a
⟹ nCO2 = 24a + 0,37 (mol)
- Mặt khác: mE = mC + mH + mO
⟹ 12(24a + 0,37) + 0,37.2 + 3a.32 + 5a.64 = 12,22 ⟹ a = 0,01 mol
⟹ nCO2 = 24.0,01 + 0,37 = 0,61 mol; n este đơn chức = 0,03 và n este hai chức = 0,05 (mol)
Bước 3: Xác định CTCT các chất trong E
- BTNT "C": nCO2 = 0,03n + 0,05m = 0,61 chỉ có nghiệm n = 7 và m = 8 thỏa mãn
(Do các axit đều 4C và ancol không no tối thiểu 3C nên n ≥ 7 và m ≥ 8)
- Do thủy phân E trong NaOH thu được hỗn hợp X gồm các muối của các axit cacboxylic không no, có cùng số nguyên tử cacbon trong phân tử; hai ancol không no, đơn chức và một ancol no, đơn chức nên ta suy ra cấu tạo của các chất trong E là:
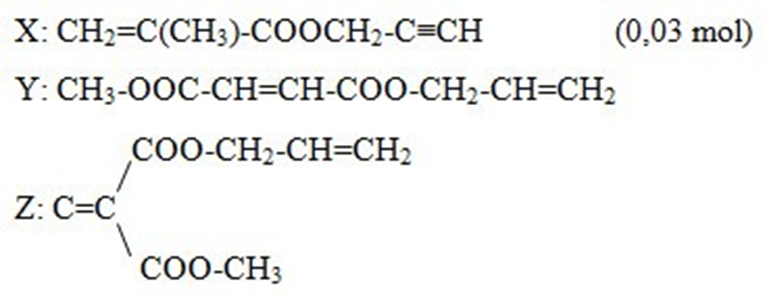
Bước 4: Xác định CTCT của ancol đơn chức và đa chức. Tính m1:m2
Ancol đa chức gồm: CH≡C-CH2-OH (0,03 mol) và CH2=CH-CH2-OH (0,05 mol)
⟹ m1 = 0,03.56 + 0,05.58 = 4,58 gam
Ancol đơn chức gồm: CH3OH (0,05 mol)
⟹ m2 = 0,05.32 = 1,6 gam
⟹ m1 : m2 = 4,58 : 1,6 = 2,8625 gần nhất với 2,9.

