Lượng HCl và K2Cr2O7 tương ứng cần sử dụng đề điều chế 672 ml khí Cl2 (đktc) là:
K2Cr2O7 + 14HCl → 2CrCl3 + 3Cl2 + 2KCl + 7H2O
0,01 ← 0,14 ← 0,03
Thực hiện phản ứng nhiệt nhôm giữa Al và Cr2O3 trong điều kiện không có không khí, sau phản ứng hoàn toàn thu được hỗn hợp X có khối lượng 43,9 gam. Chia X làm 2 phần bằng nhau. Cho phần 1 tác dụng với dung dịch NaOH (dư) thu được 1,68 lít khí (đktc). Phần 2 cho tác dụng vừa đủ với V lít dung dịch HCl 1M (loãng nóng). Giá trị của V là
2Al + Cr2O3 → Al2O3 + 2Cr
2x x x 2x
½ X + NaOH : Do có khí thoát ra nên Al còn, Cr2O3 hết, hỗn hợp X gồm Al2O3, Cr và Al dư
nAl dư 1 phần = 2/3.nH2 = 0,05 mol
=> mX = 27.0,05.2 + 102x + 52.2x = 43,9 => x = 0,2 mol
½ X + HCl :
Al2O3 + 6HCl → 2AlCl3 + 3H2O
0,1 → 0,6
Cr + 2HCl → CrCl2 + H2
0,2 → 0,4
2Al + 6HCl → 2AlCl3 + 3H2
0,05→ 0,15
=> nHCl = 1,15 mol
=> V ddHCl = 1,15 lít
Chia 31,2 gam hỗm hợp X gồm Cr và Zn, Ni và Al thành hai phần bằng nhau. Hòa tan hết phần 1 trong lượng dư dung dịch HCl loãng nóng thu được 7,28lít H2(đktc). Cho phần 2 tác dụng với khí Cl2 (dư ) đốt nóng , thu được 42,225 gam muối clorua . Phần tram khối lượng của crom trong hỗn hợp X là
½ X + HCl → muối Z (CrCl2 , ZnCl2 , NiCl2 , AlCl3) + H2
=> mZ = 15,6 + 71.7,28 / 22,4 = 38,675 gam
½ X + Cl2 → muối Y (CrCl3 , ZnCl2 , NiCl2 , AlCl3)
Gọi 2a là số mol Cr chứa trong hỗn hợp X
=> a = (mY - mX ) / 35,5 = (42,225 – 38,675 ) / 35,5 = 0,1 mol
=> %Cr = 52.0,1.100% / 15,6 = 33,33%
Nung nóng 46,6 gam hỗn hợp gồm Al và Cr2O3 (trong điều kiện không có không khí) đến khi phản ứng xảy ra hoàn toàn. Chia hỗn hợp thu được sau phản ứng thành hai phần bằng nhau. Phần một phản ứng vừa đủ với 300 ml dung dịch NaOH 1M (loãng). Để hòa tan hết phần hai cần vừa đủ dung dịch chứa a mol HCl. Giá trị của a là
TH1: Al dư, Cr2O3 hết. Chỉ có Al dư và Al2O3 tan trong NaOH => nAl ban đầu = nNaOH = 0,3 mol
=> nCr2O3 = 0,1
Với HCl, sản phẩm chứa Al3+ (0,3 mol), Cr2+ (0,2 mol) => nCl- = 1,3 mol
Vậy nHCl = 1,3 mol
TH2: Al hết (x mol), Cr2O3 còn dư (y mol)
=> nNaOH = x + 2y = 0,3
mhh = 27x + 152.(0,5x + y) = 23,3
=> x = 1/54 và y = 19/135
Với HCl, sản phẩm chứa Al3+ (1/54 mol), Cr3+ (2y = 38/135) và Cr2+ (1/54 mol)
=> nCl- = 0,937 mol
Cho 0,6 mol KI tác dụng hết với dung dịch K2Cr2O7 trong axit sunfuric thì thu được một đơn chất. Tính số mol của đơn chất này.
6KI + K2Cr2O7 + 7H2SO4 → Cr2(SO4)3 + 4K2SO4 + 3I2 + 7H2O
=> nI2=nKI2=0,3(mol)
Nung hỗn hợp bột gồm 15,2 gam Cr2O3 và m gam Al ở nhiệt độ cao. Sau khi phản ứng hoàn toàn, thu được 23,3 gam hỗn hợp rắn X. Cho toàn bộ hỗn hợp X phản ứng với axit HCl (dư) thoát ra V lít khí H2 (ở đktc). Giá trị của V là
Trong phản ứng nhiệt nhôm, không có chất nào tách ra khỏi hỗn hợp rắn, nên khối lượng hỗn hợp chất rắn trước và sau phản ứng bằng nhau.
=>nAl=23,3−15,227=0,3(mol)
Như vậy, sau phản ứng Al dư:
2Al + Cr2O3 → Al2O3 + 2Cr
Hỗn hợp X gồm 0,1 mol Al; 0,1 mol Al2O3; 0,2 mol Cr
Khi phản ứng với HCl :
Al → Al3+ + 3e 2H+ + 2e → H2
0,1 0,3 0,7 0,35
Cr → Cr2+ +2e
0,2 0,2
=> V = 0,35.22,4 = 7,84 (lít)
Khi cho 41,4 gam hỗn hợp X gồm Fe2O3, Cr2O3 và Al2O3 tác dụng với dung dịch NaOH đặc (dư), sau phản ứng thu được chất rắn có khối lượng 16 gam. Để khử hoàn toàn 41,4 gam X bằng phản ứng nhiệt nhôm, phải dùng 10,8 gam Al. Thành phần phần trăm theo khối lượng của Cr2O3 trong hỗn hợp X là (Hiệu suất của các phản ứng là 100%)
{Fe2O3Cr2O3Al2O3 +NaOH(dac,du)→{Fe2O3↓Cr2O3,Al2O3:tan
=> nFe2O3 = 0,1(mol)
{Fe2O3Cr2O3Al2O3Al(to)→{Cr,FeAl2O3
Cr2O3 + 2Al to→ 2Cr + Al2O3
Fe2O3 + 2Al to→ 2Fe + Al2O3
=>12nAlpu=nCr2O3+nFe2O3=12.10,827=0,2(mol)
=>nCr2O3=0,2−nFe2O3=0,2−0,1=0,1(mol)
=>%mCr2O3(X)=152.0,141,4.100%=36,71%.
Từ 1 tấn quặng sắt cromit (có thể viết tắt Fe(CrO2)2 người ta điều chế được 216 kg hợp kim ferocrom (hợp kim Fe-Cr) có chứa 65% Cr. Giả sử hiệu suất của quá trình là 90%. Phần trăm khối lượng của của tạp chất trong quặng là
mCr =216.65100=140,4(kg)
=>nCr = 2,7(kmol)
Bảo toàn nguyên tố Cr;
2nCr = ncromit = 2,7 (kmol)
=> ncromit (LT) = 1,35 (kmol)
=> ncromit (TT) = 1,35.10090=1,5(kmol)
=> %quặng = 1,5.2241000.100
=> %tạp chất = 66,4%
Hòa tan 58,4 gam hỗn hợp muối khan AlCl3 và CrCl3 vào nước, thêm dư dung dịch NaOH vào sau đó tiếp tục thêm nước clo rồi lại thêm dư dung dịch BaCl2 thì thu được 50,6 gam kết tủa. Thành phần % khối lượng của các muối trong hỗn hợp đầu là
Gọi a, b lần lượt là số mol của AlCl3 và CrCl3
=> 133,5a + 158,5b = 58,4 (1)
Bảo toàn Al và Cr: nAlCl3 = nNaAlO2 = a mol; nCrCl3 = nNaCrO2 = nBaCrO4 kết tủa = b mol
nkết tủa = 50,6/253 = 0,2 (mol)
=> mCrCl3 = 158,5.0,2 = 31,7 (g)
=>
%mCrCl3=31,758,4.100=54,3
=> %mAlCl3 =45,7%
Cho dung dịch NaOH vào lượng dư dung dịch chất X, thu được kết tủa màu lục xám. Chất X là:
Cho dung dịch NaOH vào lượng dư dung dịch chất X, thu được kết tủa màu lục xám. Chất X là vì CrCl3
FeCl3 + 3NaOH → 3NaCl + Fe(OH)3 (màu nâu đỏ)
CrCl3 + 3NaOH → 3NaCl + Cr(OH)3 (màu lục xám)
MgCl2 + 2NaOH → 2NaCl + Mg(OH)2 (màu trắng)
FeCl2 + 2NaOH → 2NaCl + Fe(OH)2 (trắng xanh)
Tính thể tích của dung dịch K2Cr2O7 0,05M vừa đủ phản ứng với dung dịch chứa 0,06 mol FeSO4 trong môi trường H2SO4 dư.
Phương trình hóa học:
K2Cr2O7 + 6FeSO4 + 7H2SO4 → Cr2(SO4)3 + K2SO4 + 3Fe2(SO4)3 + 7H2O
0,01 ← 0,06 (mol)
⟹ VK2Cr2O7 = 0,2 lít = 200 (ml)
Tính thể tích khí oxi (đktc) cần dùng để đốt cháy hoàn toàn 5,2 gam Cr để tạo ra sản phẩm Cr2O3?
PTHH: 4Cr + 3O2 t0→ 2Cr2O3
Ta có: nCr = 5,2 : 52 = 0,1 (mol)
Theo PTHH ta có: nO2 = ¾ . nCr = 0,075 mol → VO2 = 0,075 . 22,4 = 1,68 (lít)
Để điều chế Cr từ Cr2O3 (tách được từ quặng cromit) người ta dùng phương pháp nhiệt nhôm với hiệu suất 80%. Khối lượng nhôm cần dùng để điều chế 104 gam crom là
Ta có: nCr = 2 mol
PTHH: Cr2O3 + 2Al → Al2O3 + 2Cr
2 mol ← 2 mol
→ Thực tế nAl = 2.(100/80) = 2,5 mol → mAl = 67,5 gam
Thực hiện phản ứng nhiệt nhôm hỗn hợp Al, Fe2O3, Cr2O3 sau một thời gian thu được hỗn hợp chất rắn X. Chia X thành 2 phần bằng nhau. Hòa tan hoàn toàn phần 1 trong dung dịch H2SO4 đặc, nóng dư sau khi các phản ứng xảy ra hoàn toàn, thu được 2,016 lít khí SO2 (sản phẩm khử duy nhất, đktc). Hòa tan hết phần 2 trong 400 ml dung dịch HNO3 2M, thu được dung dịch Y và khí NO (sản phẩm khử duy nhất của N+5). Cho từ từ dung dịch NaOH 1M đến dư vào dung dịch Y thu được kết quả như hình vẽ sau:
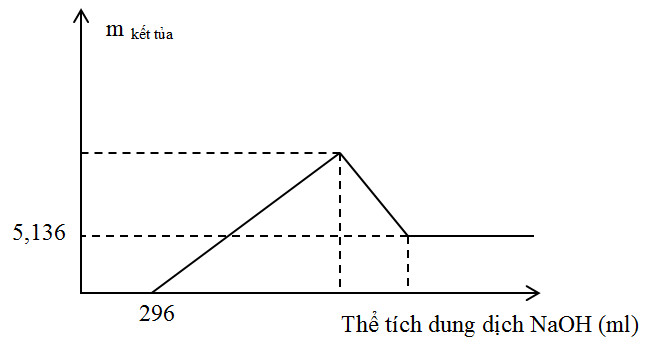
Khối lượng Cr2O3 trong hỗn hợp ban đầu là
Nhìn vào đồ thị ta thấy sau một thời gian kết tủa xuất hiện nên suy ra trong dung dịch Y có chứa H+ dư
=> nH+ dư = 0,296 mol
Khi thêm NaOH khối lượng kết tủa không đổi và bằng 5,136 gam => mFe(OH)3 = 5,136 gam
=> nFe(OH)3 = 0,048 mol
Quy đổi mỗi phần thành: Al (x mol); Fe (0,048 mol); Cr (y mol); O (x mol)
=> nFe2O3 = 0,5.0,048 = 0,024 (mol); nCr2O3 = 0,5y (mol)
+ Ta có: nO = 3nFe2O3 + 3nCr2O3 => z = 3.0,024 + 3.0,5y (1)
+ BTe quá trình phần 1 tác dụng với H2SO4 đặc nóng dư:
3nAl + 3nFe + 3nCr = 2nO + 2nSO2 => 3x + 3.0,048 + 3y = 2z + 0,09.2 (2)
+ Phần 2 tác dụng với HNO3:
Thành phần dung dịch Y {Al3+:xFe3+:0,048Cr3+:yH+du:0,296BTDT⟶NO3−:3x+3y+0,44
Do 2 phần có khối lượng bằng nhau nên ta suy ra lượng e trao đổi của SO2 bằng lượng e trao đổi của NO
=> 2nSO2 = 3nNO => nNO = 2/3.nSO2 = 2/3.0,09 = 0,06 mol
BTNT "N": nHNO3 pư = nNO3- + nNO => 0,8 = 3x + 3y + 0,44 + 0,06 (3)
Giải hệ (1) (2) (3) được x = 0,06; y = 0,04; z = 0,132
Trong mỗi phần ta có: nCr = y = 0,04 => nCr2O3 = 0,02 mol => mCr2O3 = 3,04 gam
=> mCr2O3 (hh đầu) = 6,08 gam
Tiến hành phản ứng nhiệt nhôm hỗn hợp X gồm 0,03 mol Cr2O3; 0,04 mol FeO và a mol Al. Sau một thời gian phản ứng, trộn đều, thu được hỗn hợp chất rắn Y. Chia Y thành hai phần bằng nhau. Phần 1 phản ứng vừa đủ với 400 ml dung dịch NaOH 0,1M (loãng). Phần 2 phản ứng với dung dịch HCl loãng, nóng, dư thu được 1,12 lít khí H2 (đktc). Giả sử trong phản ứng nhiệt nhôm, Cr2O3 chỉ bị khử thành Cr. Phần trăm khối lượng Cr2O3 đã phản ứng là:
- Sau phản ứng chia làm hai phần bằng nhau, vậy mỗi phần tương đương với lượng phản ứng ban đầu là 0,015 mol Cr2O3, 0,02 mol FeO và b mol Al (với b = a/2). Số mol các chất trong mỗi phần của hỗn hợp Y là như nhau. (Al, Al2O3, Cr, Cr2O3, Fe, FeO).
Chú ý: Nhiều HS giải cho rằng FeO phản ứng hết. Điều này có thể không chính xác và không khẳng định được.
- Các chất phản ứng với dd NaOH loãng là Al, Al2O3. Riêng Cr2O3 chỉ phản ứng với dd NaOH đặc
- Các chất phản ứng với dd HCl loãng nóng, tạo H2 là Al, Cr, Fe.
- Vậy xét P1: Al + NaOH và Al2O3 + 2NaOH
x x y 2y
=> Số mol Al ban đầu = x + 2y = nNaOH = 0,04 mol
- Xét các phản ứng nhiệt nhôm
2Al + Cr2O3 → Al2O3 + 2Cr
m m/2 m
2Al + 3FeO → Al2O3 + 3Fe
n 1,5n
- Xét phản ứng với dd HCl, ta có tỉ lệ
Al → 1,5H2 ; Cr → H2; Fe → H2
=> nH2 = 1,5x + m + 1,5n và x = 0,04 – m – n
=> 1,5 (0,04 – m – n) + m + 1,5n = 0,05 => 0,06 - 1,5m - 1,5n + m + 1,5n = 0,05
=> 0,06 – 0,5m = 0,05 => m = 0,02
=> Số mol Cr2O3 phản ứng = m/2 = 0,01 mol
=> h = 0,01/0,015*100% = 66,67%.
- Đến đây ta thấy rằng lượng FeO phản ứng không ảnh hưởng tới kết quả phản ứng của Cr2O3.
Gọi x là % Cr2O3 đã phản ứng
0,5a = 0,04
0,5a*3 - 0,015x*2 = 0,05*2
=> a = 0,08 và x = 0,6667
Hoặc: (0,04*3-0,05*2):2*100:0,015 = 66,667%

