Trường hợp nào sau đây xảy ra ăn mòn điện hoá ?
Khi cho CuSO4 vào thì xảy ra phản ứng: Zn + CuSO4 → ZnSO4 + Cu
Cu tạo ra bám trên Zn→ tạo ra 1 pin điện hóa làm thanh kẽm ăn mòn nhanh
Có 6 dung dịch riêng biệt: Fe(NO3)3, AgNO3, CuSO4, ZnCl2, Na2SO4, MgSO4. Nhúng vào mỗi dung dịch một thanh Cu kim loại, số trường hợp xảy ra ăn mòn điện hóa là
+) Cu + 2Fe(NO3)3 → Cu(NO3)2 + 2Fe(NO3)2
→ không tạo thành 2 điện cực mới → không xảy ra ăn mòn điện hóa
+) Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
→ Ag sinh ra bám vào thanh Cu, hình thành 2 điện cực cùng tiếp xúc với dung dịch chất điện li
→ xảy ra quá trình ăn mòn điện hóa
Tiến hành 6 thí nghiệm sau đây
TN1: Nhúng thanh sắt vào dung dịch FeCl3.
TN2: Nhúng thanh sắt vào dung dịch CuSO4.
TN3: Để chiếc đinh làm bằng thép ngoài không khí ẩm.
TN4: Cho chiếc đinh làm bằng sắt vào dung dịch H2SO4.
TN5: Nhúng thanh đồng vào dung dịch Fe2(SO4)3.
TN6: Nhúng thanh nhôm vào dung dịch H2SO4 loãng có hòa tan vài giọt CuSO4.
Số trường hợp xảy ra ăn mòn điện hóa là
(1) Fe + 2FeCl3 → 3FeCl2 không tạo ra 2 điện cực mới → ăn mòn hóa học
(2) Fe + CuSO4 → FeSO4 + Cu
→ Cu sinh ra bám vào thanh sắt và hình thành 2 điện cực cùng tiếp xúc với dung dịch chất điện li
→ xảy ra ăn mòn điện hóa
(3) Đinh thép là hợp kim Fe-C, để ngoài không khí ẩm xảy ra sự ăn mòn điện hóa
(4) Fe + H2SO4 → FeSO4 + H2
không tạo ra 2 điện cực mới → ăn mòn hóa học
(5) Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4
không tạo ra 2 điện cực mới → ăn mòn hóa học
(6) 2Al + 3CuSO4 → Al2(SO4)3 + 3Cu
→ Cu sinh ra bám vào thanh nhôm và hình thành 2 điện cực cùng tiếp xúc với dung dịch chất điện li
→ xảy ra ăn mòn điện hóa
Vậy có 3 trường hợp xảy ra ăn mòn điện hóa
Tiến hành các thí nghiệm sau :
(1) Nhúng thanh Zn vào dung dịch AgNO3.
(2) Cho vật bằng gang vào dung dịch HCl.
(3) Cho Na vào dung dịch CuSO4.
(4) Để miếng tôn (Fe tráng Zn) có vết xước sâu ngoài không khí ẩm.
(5) Cho đinh sắt vào dung dịch H2SO4 2M.
(6) Cho Mg vào dung dịch FeCl3 dư.
Số thí nghiệm xảy ra ăn mòn hóa học là
(1) Zn + AgNO3 → Zn(NO3)2 + Ag
=> ăn mòn điện hóa
(2) Gang có thành phần chính là Fe và C
Fe + 2HCl → FeCl2 + H2
Tạo ra 2 điện cực mới (Fe là cực (-), C là cực (+) → ăn mòn điện hóa
(3) Cho Na vào dung dich CuSO4 có phản ứng
2Na + 2H2O → 2NaOH + H2
2NaOH + CuSO4 → Cu(OH)2 + Na2SO4
Phản ứng không tạo ra 2 điện cực mới → ăn mòn hóa học
(4) Tôn là Fe gắn với Zn. Vết xước sâu để cả Fe và Zn đều tiếp xúc với môi trường không khí ẩm
→ xảy ra ăn mòn điện hóa
(5) Fe + H2SO4 → FeSO4 + H2 không tạo ra 2 điện cực mới → ăn mòn hóa học
(6) Mg + FeCl3 dư → MgCl2 + FeCl2 không tạo ra 2 điện cực mới → ăn mòn hóa học
Thực hiện các thí nghiệm sau :
(1) Thả một viên Fe vào dung dịch HCl.
(2) Thả một viên Fe vào dung dịch Cu(NO3)2.
(3) Thả một viên Fe vào dung dịch FeCl3.
(4) Nối một dây Ni với một dây Fe rồi để trong không khí ẩm.
(5) Đốt một dây Fe trong bình kín chứa đầy khí O2.
(6) Thả một viên Fe vào dung dịch chứa đồng thời CuSO4 và H2SO4 loãng.
Trong các thí nghiệm trên thì thí nghiệm mà Fe không bị ăn mòn điện hóa là
(1) Fe + 2HCl → FeCl2 + H2 không tạo ra 2 điện cực mới → ăn mòn hóa học
(2) Fe + Cu(NO3)2 → Fe(NO3)2 + Cu
→ Cu sinh ra bám vào viên Fe và hình thành 2 điện cực cùng tiếp xúc với dung dịch chất điện li
→ xảy ra ăn mòn điện hóa
(3) Fe + 2FeCl3 → 3FeCl2 không tạo thành 2 điện cực mới → ăn mòn hóa học
(4) Ni và Fe được nối với nhau và đặt trong không khí ẩm → ăn mòn điện hóa
(5) 3Fe + 4O2 Fe3O4 (ăn mòn hóa học)
(6) Fe + CuSO4 + H2SO4 : cả ăn mòn điện hóa và ăn mòn hóa học vì xảy ra các phản ứng sau
Fe + H2SO4 → FeSO4 + H2 (ăn mòn hóa học vì không hình thành 2 điện cực mới)
Fe + CuSO4 → FeSO4 + Cu
→ Cu sinh ra bám vào thanh sắt và hình thành 2 điện cực cùng tiếp xúc với dung dịch chất điện li
→ xảy ra ăn mòn điện hóa
Cho các thí nghiệm sau :
- TN1: Nhúng thanh Zn vào dung dịch chứa lượng nhỏ FeCl3.
- TN2: Nhúng thanh Fe vào dung dịch chứa lượng nhỏ CuSO4.
- TN3: Nhúng thanh Cu vào dung dịch chứa lượng nhỏ FeCl3.
- TN4: Nhúng thanh hợp kim Zn-Fe vào dung dịch chứa lượng nhỏ HCl loãng.
- TN5: Nhúng thanh Cu dung dịch chứa lượng nhỏ HCl loãng/ bão hòa oxi.
- TN6: Đốt thanh sắt trong oxi ở nhiệt độ cao.
- TN7: Vật bằng gang để trong môi trường không khí ẩm.
Số trường hợp có hiện tượng ăn mòn hóa học là
- TN1: Zn + FeCl3 → ZnCl2 + FeCl2 (ăn mòn hóa học vì không hình thành 2 điện cực mới)
Zn + FeCl2 → ZnCl2 + Fe
→ Fe sinh ra bám vào thanh kẽm và hình thành 2 điện cực cùng tiếp xúc với dung dịch chất điện li
→ xảy ra ăn mòn điện hóa đồng thời với ăn mòn hóa học
- TN2: Fe + CuSO4 → FeSO4 + Cu
→ Cu sinh ra bám vào thanh sắt và hình thành 2 điện cực cùng tiếp xúc với dung dịch chất điện li
→ xảy ra ăn mòn điện hóa đồng thời với ăn mòn hóa học
- TN3: Cu + 2FeCl3 → CuCl2 + 2FeCl2 không tạo thành 2 điện cực mới → ăn mòn hóa học
- TN4: Zn + 2HCl → ZnCl2 + H2 (ăn mòn hóa học)
Fe + 2HCl → FeCl2 + H2 (ăn mòn hóa học)
Hai thanh kim loại được nối với nhau và được nhúng trong dung dịch chất điện li → xảy ra cả ăn mòn điện hóa đồng thời với ăn mòn hóa học
- TN5: Cu+2HCl+12O2→CuCl2+H2O không có kim loại mới → ăn mòn hóa học
- TN6: 3Fe + 2O2 → Fe3O4 (ăn mòn hóa học)
- TN7: Ăn mòn điện hóa
=> Các TN1, TN2, TN3, TN4, TN5, TN6 có xảy ra ăn mòn hóa học
Các vật dụng bằng sắt trong đời sống đều không phải là sắt nguyên chất. Đó là nguyên nhân dẫn đến
Các vật dụng bằng sắt trong đời sống đều không phải là sắt nguyên chất là nguyên nhân dẫn tới ăn mòn điện hóa
→ dễ bị gỉ sét khi tiếp xúc với dung dịch điện li
Cơ sở hóa học của các phương pháp chống ăn mòn kim loại là
Cơ sở hóa học của các phương pháp chống ăn mòn kim loại :
- Phương pháp bảo vệ bề mặt là phủ lên bề mặt kim loại một lớp sơn, dầu mỡ, chất dẻo hoặc tráng, mạ bằng một kim loại khác. Nếu lớp bảo vệ bị hư, kim loại sẽ bị ăn mòn.
- Phương pháp bảo vệ điện hóa là dùng một kim loại có tính khử mạnh hơn làm vật hi sinh để bảo vệ vật liệu kim loại. Vật hi sinh và kim loại cần bảo vệ hình thành một pin điện, trong đó vật hi sinh đóng vai trò cực âm và bị ăn mòn.
→ Ngăn cản hạn chế quá trình oxi hóa kim loại.
Người ta gắn tấm Zn vào vỏ ngoài của tàu thuỷ ở phần chìm trong nước biển để
Người ta gắn tấm Zn vào vỏ ngoài của tàu thuỷ ở phần chìm trong nước biển để chống ăn mòn kim loại bằng phương pháp điện hoá (SGK lớp 12 nâng cao – trang 135)
Để bảo vệ những vật bằng Fe khỏi bị ăn mòn, người ta phủ một lớp sơn lên vật liệu. Làm như vậy là để chống ăn mòn theo phương pháp nào sau đây?
Phương pháp chống ăn mòn ở đây là bảo vệ bề mặt (SGK lớp 12 nâng cao – trang 135).
Để chống ăn mòn cho đường ống dẫn dầu bằng thép chôn dưới đất, người ta dùng phương pháp điện hoá. Trong thực tế, người ta dùng kim loại nào sau đây làm điện cực hi sinh ?
Thực tế người ta dùng Zn phải dùng kim loại hoạt động mạnh hơn để hi sinh bên ngoài, bảo vệ kim loại Fe bên trong
Hỗn hợp tecmit dùng để hàn những chỗ vỡ, mẻ của đường tàu hỏa là
Hỗn hợp tecmit gồm Al và Fe2O3.
Tôn là sắt được tráng
Tôn là sắt được tráng kẽm
Vật làm bằng hợp kim Zn-Cu trong môi trường không khí ẩm (hơi nước có hòa tan O2) đã xảy ra quá trình ăn mòn điện hóa. Tại anot xảy ra quá trình
Pin điện Zn-Cu đặt trong không khí ẩm:
Anot (-): Zn → Zn2+ + 2e => xảy ra quá trình oxi hóa Zn
Catot (+): O2 + H2O + 4e → 4OH- => xảy ra quá trình khử O2
Nối một sợi dây nhôm với một sợi dây đồng rồi để lâu trong không khí ẩm. Tại chỗ nối sẽ xảy ra chủ yếu là quá trình
Nối một sợi dây nhôm với một sợi dây đồng rồi để lâu trong không khí ẩm sẽ xảy ra hiện tượng ăn mòn điện hóa. Tính khử Al > Cu nên Al sẽ bị ăn mòn ⟹ chủ yếu xảy ra quá trình oxi hóa nhôm.
Tiến hành 3 thí nghiệm như hình vẽ sau:
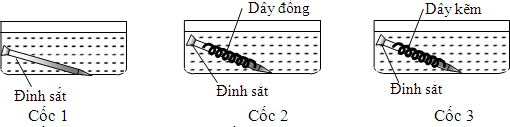
Đinh sắt trong cốc nào sau đây bị ăn mòn nhanh nhất?
Cốc 1: Đinh sắt bị ăn mòn hóa học. Khí H2 sinh ra bám vào bề mặt của đinh sắt, ngăn cản sự tiếp xúc của đinh sắt với dung dịch HCl nên khí thoát ra chậm.
⟹ Đinh sắt bị ăn mòn chậm.
Cốc 2: Đinh sắt và dây đồng tiếp xúc trực tiếp với nhau, cùng được nhúng trong dung dịch chất điện li HCl nên có xảy ra hiện tượng ăn mòn điện hóa. Đinh sắt đóng vai trò anot (do Fe có tính khử mạnh hơn Cu) nên bị ăn mòn. Khí sinh ra trên bề mặt thanh Fe giảm nên sự tiếp xúc giữa Fe và dung dịch HCl tăng lên.
⟹ Đinh sắt bị ăn mòn nhanh.
Cốc 3: Đinh sắt và dây kẽm tiếp xúc trực tiếp với nhau, cùng được nhúng trong dung dịch chất điện li HCl nên có xảy ra hiện tượng ăn mòn điện hóa. Dây kẽm đóng vai trò anot (do Zn có tính khử mạnh hơn Fe) nên bị ăn mòn. ⟹ Đinh sắt được bảo vệ.
Vậy đinh sắt trong cốc 2 bị ăn mòn nhanh nhất.
Thí nghiệm nào sau đây chỉ xảy ra ăn mòn hóa học?
- A sai vì có phản ứng: Zn + CuSO4 → ZnSO4 + Cu
Cu sinh ra bám vào Zn và cùng tiếp xúc với dung dịch điện li nên xảy ra ăn mòn điện hóa.
- B đúng vì Fe và C tiếp xúc với nhau nhưng môi trường khí O2 không phải là môi trường chất điện li nên chỉ xảy ra ăn mòn hóa học.
- C sai vì có phản ứng: Fe + CuSO4 → FeSO4 + Cu
Cu sinh ra bám vào Fe và cùng tiếp xúc với dung dịch điện li nên xảy ra ăn mòn điện hóa.
- D sai vì Fe và C tiếp xúc trực tiếp và cùng được đặt trong môi trường chất điện li (không khí ẩm) nên xảy ra ăn mòn điện hóa.
Phương pháp thường được áp dụng để chống ăn mòn kim loại là
Các phương pháp bảo vệ kim loại không bị ăn mòn là:
+ Phương pháp bảo vệ bề mặt.
+ Phương pháp điện hóa.

Phát biểu nào sau đây không đúng khi so sánh ăn mòn điện hóa và ăn mòn hóa học?
C sai vì ăn mòn điện hóa có phát sinh dòng điện, ăn mòn hóa học không phát sinh dòng điện.

