Số oxi hoá của S trong các hợp chất sau: Cu2S, FeS, NaHSO4, (NH4)2S2O8, Na2SO3 lần lượt là:
+1Cu2−2S, +2Fe−2S, +1Na+1H+6S−2O4, (−3N+1H4)2+7S2−2O8, Na2+4SO3
Ở trạng thái kích thích cao nhất, nguyên tử lưu huỳnh có thể có tối đa bao nhiêu electron độc thân?
Ở trạng thái kích thích cao nhất, nguyên tử lưu huỳnh có thể có tối đa 6 electron độc thân
Hạt vi mô nào sau đây có cấu hình electron giống Ar (Z = 18)?
Ar (Z = 18): 1s22s22p63s23p6
=> hạt có cấu hình e giống Ar là S2-
X2 là chất khí, không màu, không mùi, nặng hơn không khí. X là chất nào?
X2 là chất khí nặng hơn không khí => loại A
X2 là chất khí không màu không mùi => loại C
Loại D vì Argon không tồn tại dạng X2
Trong không khí, oxi chiếm:
Trong không khí, oxi chiếm 20% về thể tích.
Với các nguyên tố nhóm VIA, nhận xét nào sau đây sai ?
Nhận xét sai là: Tính axit tăng dần: H2SO4 < H2SeO4 <H2TeO4. Vì tính axit giảm dần: H2SO4 > H2SeO4 > H2TeO4.
Cho hình vẽ mô tả thí nghiệm điều chế khí Y từ chất rắn X như sau
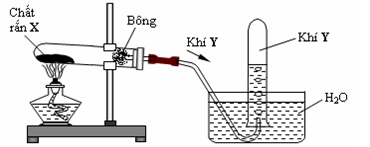
Hình vẽ trên minh họa cho phản ứng nào sau đây ?
Đun nóng rắn X thu được khí Y không bị hòa tan trong nước nên đáp án B vì khí tạo ra là O2 vì O2 không bị hòa tan trong nước còn NH3 và SO2 tan nhiều trong nước

