Khi điện phân có màng ngăn dung dịch muối ăn bão hòa trong nước thì ở catot xảy ra quá trình
PTHH: 2NaCl + 2H2O \(\buildrel {dpmn} \over
\longrightarrow \) 2NaOH + H2 + Cl2
=> hiện tượng ở catot xảy ra quá trình khử nước xuất hiện khí hiđro
Cho các kim loại: Na, Ca, Al, Fe, Cu, Ag. Bằng phương pháp điện phân dung dịch có thể điều chế được bao nhiêu kim loại trong số các kim loại ở trên ?
Bằng phương pháp điện phân có thể điều chế được tất cả các kim loại trên.
- phương pháp điện phân dung dịch: Fe, Cu, Ag
Khi điện phân một dung dịch muối giá trị pH ở gần một điện cực giảm đi. Dung dịch muối đó là
Khi điện phân một dung dịch muối giá trị pH ở gần một điện cực tăng lên. Dung dịch muối đó là KCl vì
PTĐP:
2CuSO4 + 2H2O → 2Cu + O2 + 2H2SO4
FeCl2 → Fe + Cl2
KCl + H2O → KOH + H2 + Cl2
Điện phân dung dịch K2SO4 chính là điện phân H2O ở 2 điện cực
Điện phân CuSO4 sinh ra axit nên làm pH ở 1 điện cực giảm đi
Dung dịch Cu(NO3)2 có lẫn tạp chất AgNO3 .Phương pháp hoá học đơn giản để loại được tạp chất là
Phương pháp hoá học đơn giản để loại được tạp chất là cho Cu dư vào dung dịch, sau khi phản ứng xong lọc bỏ chất rắn. Vì Cu loại bỏ được muối AgNO3 theo PTHH:
Cu + AgNO3→ Cu(NO3)2 +Ag
Để điều chế K người ta có thể dùng phương pháp nào
Để điều chế K người ta dùng phương pháp điện phân nóng chảy muối và bazơ của Na
=>điện phân nóng chảy KOH
Từ các nguyên liệu KCl, Na2CO3, BaCO3 và các điều kiện cần thiết có đủ, có thể điều chế được các đơn chất nào ?
KCl → K + Cl2
Na2CO3 + 2HCl → 2KCl + CO2 + H2O
KCl →K + Cl2
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
CaCl2→ Ca + Cl2
Hỗn hợp X gồm A12O3, MgO, Fe2O3, CuO. Cho khí H2 dư qua X nung nóng được chất rắn Y. Cho Y vào dung dịch Cu(NO3)2 dư được dung dịch E và chất rắn G. Cho chất rắn G vào dung dịch NaOH dư thu được chất rắn F. Chất rắn F gồm
\(\left\{ \matrix{
A{l_2}{O_3} \hfill \cr
MgO \hfill \cr
F{e_2}{O_3} \hfill \cr
CuO \hfill \cr} \right.\buildrel {CO} \over
\longrightarrow \left\{ \matrix{
A{l_2}{O_3} \hfill \cr
MgO \hfill \cr
Fe \hfill \cr
Cu \hfill \cr} \right.\buildrel { + Cu{{(N{O_3})}_2}} \over
\longrightarrow ddE(Fe{(N{O_3})_2}) + {\rm{G}}\left\{ \matrix{
MgO \hfill \cr
A{l_2}{O_3} \hfill \cr
Cu \hfill \cr} \right.\buildrel {NaOH} \over
\longrightarrow F\left\{ \matrix{
MgO \hfill \cr
Cu \hfill \cr} \right.\)
Tiến hành các thí nghiệm sau:
(1) Cho Mg vào dung dịch Fe2(SO4)3 dư;
(2) Dẫn khí H2 (dư) qua bột MgO nung nóng;
(3) Cho dung dịch AgNO3 tác dụng với dung dịch Fe(NO3)2 dư;
(4) Cho Na vào dung dịch MgSO4;
(5) Nhiệt phân Hg(NO3)2;
(6) Đốt Ag2S trong không khí;
(7) Điện phân dung dịch Cu(NO3)2 với các điện cực trơ.
Số thí nghiệm tạo thành kim loại là
(1) Mg + Fe2(SO4)3 dư → MgSO4 + 2FeSO4 => không tạo thành kim loại
(2) H2 không phản ứng với MgO =>không tạo thành kim loại
(3) AgNO3 + Fe(NO3)2 → Ag↓ + Fe(NO3)3
(4) 2Na + 2H2O → 2NaOH + H2
2NaOH + MgSO4 → Mg(OH)2 + Na2SO4 =>không tạo thành kim loại
(5) Hg(NO3)2 → Hg↓ + 2NO2 + O2
(6) Ag2S+ O2 → 2Ag + SO2
(7) 2Cu(NO3)2 + 2H2O → 2Cu + O2 + 4HNO3
Vậy thí nghiệm thu được kim loại là (3); (5); (6); (7).
Dãy kim loại nào dưới đây điều chế được bẳng cách điện phân nóng chảy muối clorua?
Dãy kim loại nào dưới đây điều chế được bẳng cách điện phân nóng chảy muối clorua : Na, Ba, Mg
Để tinh chế Ag từ hỗn hợp (Fe,Cu,Ag) sao cho khối lượng Ag không đổi ta dùng:
A. dùng dd AgNO3 thì sẽ làm lượng Ag trong hỗn hợp tăng lên
B. dùng dd HCl thì sẽ không tinh chế được Ag vì cả Ag và Cu cùng không phản ứng với dd HCl
C. Không dùng được
D. Dùng dd Fe(NO3)3 sẽ tinh chế được Ag mà không làm thay đổi khối lượng của chúng
2Fe(NO3)3 + Fe → 3Fe(NO3)2
2Fe(NO3)3 + Cu → 2Fe(NO3)2 + Cu(NO3)2
Để điều chế Ag từ dung dịch AgNO3 ta không thể dùng:
\(\eqalign{
& A.\,4AgN{O_3} + 2{H_2}O\buildrel {DPDD} \over
\longrightarrow 4Ag + {O_2} + 4HN{O_3} \cr
& B.\,AgN{O_3}\buildrel {{t^0}} \over
\longrightarrow Ag + N{O_2} + {1 \over 2}{O_2} \uparrow \cr} \)
C. Ba + 2H2O → Ba(OH)2 + H2↑
Ba(OH)2 + 2AgNO3 → Ag2O↓ + Ba(NO3)2 + H2O
=> không thu được Ag
D. Cu + 2AgNO3 → Cu(NO3)2 + Ag↓
Cho sơ đồ sau: \(X\xrightarrow{dpnc}Na+...\) Hãy cho biết X có thể là chất nào sau đây?
+ A loại vì NaNO3 bị nhiệt phân tạo NaNO2
+ B loại vì Na2SO4 không bị nhiệt phân
+ C đúng
2NaCl \(\xrightarrow{dpnc}\) 2Na + Cl2
2NaOH \(\xrightarrow{dpnc}\) 2Na + O2 + H2
+ D loại vì NaHCO3 bị nhiệt phân thành Na2CO3
Kim loại nào chỉ được điều chế từ phương pháp điện phân nóng chảy
Kim loại chỉ điều chế được bằng phương pháp điện phân nóng chảy là K
Cách nào sau đây không điều chế được NaOH?
KOH không có phản ứng với Na2CO3 nên không điều chế được NaOH
Hóa chất nào sau đây dùng để tách Ag ra khỏi hỗn hợp Ag, Fe, Cu mà vẫn giữ nguyên khối lượng Ag ban đầu :
A sai vì Fe và Cu sau tác dụng tạo ra Ag làm tăng khối lượng Ag thu được
B sai không tác dụng với cả 3 chất
C đúng vì Fe + 2Fe(NO3)3 → 3Fe(NO3)2 ; Cu + 2Fe(NO3)3 → Cu(NO3)2 + 2Fe(NO3)2 nên rắn còn lại chỉ là Ag
D sai vì rắn thu được có cả Cu và Ag
Cho luồng khí H2 (dư) qua hỗn hợp các oxit CuO, Fe2O3, MgO nung nóng ở niệt độ cao. Sau khi phản ứng xảy ra hoàn tàn, hỗn hợp rắn còn lại là
PTHH: H2 + CuO \(\xrightarrow{{{t^0}}}\) Cu + H2O
H2 + Fe2O3 \(\xrightarrow{{{t^0}}}\)Fe + 3H2O
MgO không có pư với H2
Sau khi phản ứng xảy ra hoàn toàn hỗn hợp rắn thu được gồm: Cu, Fe và MgO
Tiến hành phản ứng khử oxit X thành kim loại bằng khí H2 (dư) theo sơ đồ hình vẽ dưới đây:
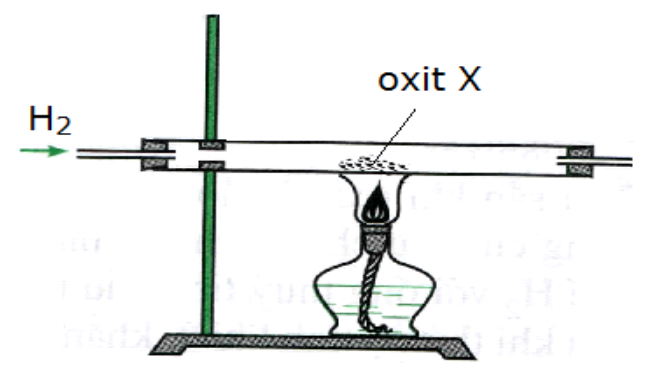
Oxit X là
H2/CO chỉ khử được các oxit của KL đứng sau Al trong dãy điện hóa → oxit X là CuO
PTHH: CuO + H2 \(\xrightarrow{{{t^o}}}\) Cu + H2O
Để điều chế Na người ta dùng phương pháp nào sau đây?
Phương pháp để điều chế Na là điện phân nóng chảy muối halogen hoặc hidroxit tương ứng của natri
2NaCl \[\xrightarrow{{dpnc}}\) 2Na + Cl2
Phản ứng nào sau đây mô tả quả trình điều chế kim loại bằng phương pháp nhiệt luyện?
Đáp án A: Phương pháp thủy luyện
Đáp án C: Phương pháp điện phân nóng chảy
Đáp án D: Phương pháp điện phân dung dịch
Trong công nghiệp, kim loại nào sau đây được điều chế bằng phương pháp nhiệt luyện?
Phương pháp nhiệt luyện dùng để điều chế các kim loại có tính khử trung bình yếu → Fe được điều chế bằng phương pháp này.

