Cho các phát biểu sau về phenol (C6H5OH):
(1) Phenol tan nhiều trong nước lạnh.
(2) Phenol có tính axit nhưng dung dịch phenol trong nước không làm đổi màu quỳ tím.
(3) Nguyên tử H ở nhóm OH ở phenol linh động hơn trong ancol.
(4) Nguyên tử H của vòng benzen trong phenol dễ bị thay thế hơn nguyên tử H trong benzen.
(5) Cho nước brom vào dung dịch phenol thấy xuất hiện kết tủa.
Số phát biểu đúng là
(1) sai, vì phenol tan ít trong nước lạnh.
(2) đúng, vì tính axit của phenol rất yếu nên không làm đổi màu quỳ tím
(3) đúng, vì ảnh hưởng của vòng benzen nên H ở nhóm OH của phenol linh động hơn so với ancol
(4) đúng, do ảnh hưởng của nhóm OH lên vòng benzen
(5) đúng
Vậy số phát biểu đúng là 4.
Cho các phát biểu sau:
(a) Phenol (C6H5-OH) là một ancol thơm.
(b) Phenol tác dụng với dung dịch natri hidroxit tạo thành muối tan và nước.
(c) Phenol tham gia phản ứng thế brom và thế nitro dễ hơn benzen.
(d) Dung dịch phenol làm quỳ tím hóa đỏ do nó có tính axit.
(e) Hợp chất C6H5-CH2-OH là phenol.
Số phát biểu đúng là:
(a) sai. C6H5OH có nhóm OH gắn trực tiếp với vòng thơm nên thuộc loại hợp chất phenol.
(b) đúng. PTHH: C6H5OH + Na → C6H5ONa (muối tan) + H2O
(c) đúng. Do ảnh hưởng của nhóm OH lên vòng benzen.
(d) sai vì phenol có tính axit rất yếu không làm đổi màu quỳ tím.
(e) sai vì C6H5CH2OH có nhóm OH không đính trực tiếp vào vòng benzen nên không phải phenol.
⟹ 2 phát biểu đúng
Phenol không tác dụng với
- Phenol không phản ứng với dung dịch HCl
- Phenol tác dụng với Br2, Na, NaOH theo các PTHH:
C6H5OH + 3Br2 → C6H2Br3OH ↓ + 3HBr
2C6H5OH + 2Na → 2C6H5ONa + H2
C6H5OH + NaOH → C6H5ONa + H2O
Cho các phát biểu sau:
(a) Phenol (C6H5-OH) là một ancol thơm.
(b) Phenol tác dụng với dung dịch natri hidroxit tạo thành muối tan và nước.
(c) Phenol tham gia phản ứng thế brom và thế nitro dễ hơn benzen.
(d) Dung dịch phenol làm quỳ tím hóa đỏ do nó có tính axit.
(e) Hợp chất C6H5-CH2-OH là phenol.
Số phát biểu sai là:
(a) sai. C6H5OH có nhóm OH gắn trực tiếp với vòng thơm nên thuộc loại hợp chất phenol.
(b) đúng. PTHH: C6H5OH + Na → C6H5ONa (muối tan) + H2O
(c) đúng. Do ảnh hưởng của nhóm OH lên vòng benzen.
(d) sai vì phenol có tính axit rất yếu không làm đổi màu quỳ tím.
(e) sai vì C6H5CH2OH có nhóm OH không đính trực tiếp vào vòng benzen nên không phải phenol.
⟹ 3 phát biểu sai
Cho các phát biểu sau về phenol C6H5OH:
(1) Phenol vừa tác dụng với dung dịch NaOH vừa tác dụng được với Na.
(2) Phenol có tính axit nhưng dung dịch phenol trong nước không làm đổi màu quỳ tím.
(3) Nguyên tử H ở nhóm OH của phenol linh động hơn trong ancol.
(4) Dung dịch natriphenolat tác dụng với CO2 tạo thành Na2CO3.
(5) Cho nước brom vào dung dịch phenol thấy xuất hiện kết tủa.
Số phát biểu đúng là
Các phát biểu đúng là (1), (2), (3), (5) (có 4 phát biểu đúng)
Phát biểu (4) sai vì: phản ứng tạo thành NaHCO3.
\({C_6}{H_5}ONa{\text{ }} + {\text{ }}C{O_2} + {\text{ }}{H_2}O{\text{ }} \to {\text{ }}{C_6}{H_5}OH{\text{ }} + {\text{ }}NaHC{O_3}\)
Vào năm 1832, phenol (C6H5OH) lần đầu tiên được tách ra từ nhựa than đá. Phenol rất độc. Khi con người ăn phải thức phẩm có chứa phenol có thể bị ngộ độc cấp, tiêu chảy, rối loạn ý thức, thậm chí tử vong. Phenol không có phản ứng với:
- Phenol có thể phản ứng với: K, nước Br2, dd NaOH.
2C6H5OH + 2K → 2C6H5OK + H2
C6H5OH + 3Br2 → C6H2Br3OH ↓ + 3HBr
C6H5OH + NaOH → C6H5ONa + H2O
- Phenol không phản ứng được với KCl.
Có 2 lọ dung dịch mất nhãn là etanol và phenol. Dùng hóa chất nào sau đây để nhận biết 2 lọ trên ?
Để nhận biết etanol và phenol ta dùng dung dịch brom. Etanol không phản ứng, phenol làm mất màu dung dịch, tạo kết tủa trắng.
X và Y là 2 hợp chất hữu cơ thơm có công thức là C7H8O, đều không làm mất màu dung dịch brom. X chỉ tác dụng với Na, không tác dụng với dung dịch NaOH, Y không tác dụng với Na và NaOH. Vậy X và Y lần lượt là
X chỉ tác dụng với Na, không tác dụng với dung dịch NaOH => X không phải là phenol => X là ancol C6H5CH2OH
Y không tác dụng với Na và NaOH => Y là ete C6H5OCH3
Nếu cho cùng một lượng chất tác dụng với Na hoặc với NaOH thì số mol X phản ứng bằng số mol NaOH và bằng số mol H2 sinh ra. X là
Số mol X bằng số mol NaOH phản ứng => X chứa 1 nhóm –OH phenol
Số mol X bằng số mol H2 sinh ra => X chứa 2 nhóm –OH trong phân tử
=> X chứa 1 nhóm –OH phenol và 1 nhóm –OH ancol
Phát biểu nào sau đây về phenol là sai?
Phát biểu sai là: Phenol thuộc loại ancol thơm, đơn chức vì phenol không phải ancol thơm.
Cho các phát biểu sau về phenol:
(a) phenol tan nhiều trong nước lạnh;
(b) phenol có tính axit nhưng phenol không làm đổi màu quỳ tím;
(c) phenol được dùng để sản xuất phẩm nhuộm, chất diệt nấm mốc;
(d) nguyên tử H trong benzen dễ bị thế hơn nguyên tử H trong vòng benzen của phenol;
(e) cho nước brom vào phenol thấy xuất hiện kết tủa.
Số phát biểu đúng là
Các phát biểu đúng là:
(b) phenol có tính axit nhưng phenol không làm đổi màu quỳ tím;
(c) phenol được dùng để sản xuất phẩm nhuộm, chất diệt nấm mốc;
(e) cho nước brom vào phenol thấy xuất hiện kết tủa.
Cho 6,04 gam hỗn hợp X gồm phenol và ancol etylic tác dụng với Na dư thu được 1,12 lít H2 (đktc). Khi cho hỗn hợp X vào dung dịch Br2 dư thì thu được bao nhiêu gam kết tủa?
Gọi ${n_{{C_6}{H_5}OH}} = \,x\,\,mol;\,\,\,{n_{{C_2}{H_5}OH}}\, = \,y\,\,mol$
→ mhỗn hợp X = 94x + 46y = 6,04 (1)
C6H5OH + Na $\xrightarrow{{}}$ C6H5ONa + $\frac{1}{2}$ H2↑
x mol → 0,5x mol
C2H5OH + Na $\xrightarrow{{}}$ C2H5ONa + $\frac{1}{2}$ H2↑
y mol → 0,5y mol
→ ${n_{{H_2}}} = \,\,\,\frac{{1,12}}{{22,4}}\,\, = \,\,0,05\,mol$ → 0,5x + 0,5y = 0,05 (2)
Từ (1) và (2) → $\left\{ \begin{gathered}0,5x + 0,5y\, = 0,05 \hfill \\94x + 46y = 6,04 \hfill \\ \end{gathered} \right.\,\,\, \to \,\,\,\left\{ \begin{gathered}x = 0,03 \hfill \\ y = 0,07 \hfill \\ \end{gathered} \right.$
Hỗn hợp X + dung dịch Br2 dư :
C6H5OH + 3Br2 → C6H2Br3OH↓ + 3HBr
0,03 → 0,03
→ ${m_ \downarrow } = {m_{{C_6}{H_3}B{r_3}O}} = 0,03.331 = 9,93\,\,gam$
Cho 15,8 gam hỗn hợp gồm CH3OH, C6H5OH tác dụng với dung dịch brom dư, thì làm mất màu vừa hết 48 gam Br2. Nếu đốt cháy hoàn toàn hỗn hợp trên thì thể tích CO2 thu được ở điều kiện tiêu chuẩn là
${n_{B{r_2}}} = \,\frac{{48}}{{160}}\, = 0,3\,mol$
C6H5OH + 3Br2 → C6H2Br3OH↓ + 3HBr
0,1 mol ← 0,3 mol
→ ${m_{{C_6}{H_5}OH}} = \,0,1.94 = 9,4\,gam$→ ${m_{C{H_3}OH}} = \,15,8 - 9,4 = 6,4\,gam$ → ${n_{C{H_3}OH}} = \frac{{6,4}}{{32}} = 0,2\,mol$
Bảo toàn nguyên tố C:
→ ${n_{C{O_2}}} = {n_{C{H_3}OH}} + \,6.{n_{{C_6}{H_5}OH}} = 0,2 + 6.0,1 = 0,8\,mol$
→ ${V_{C{O_2}(\,ktc)}} = 0,8.22,4 = 17,92\,$ lít
Đốt cháy hoàn toàn hỗn hợp X gồm phenol và etanol (tỉ lệ mol là 1:3) rồi hấp thụ toàn bộ sản phẩm cháy vào bình đựng dung dịch nước vôi trong thì thu được 15 gam kết tủa. Lọc bỏ kết tủa, lấy dung dịch thu được tác dụng với dung dịch NaOH dư thì thấy xuất hiện 7,5 gam kết tủa nữa. Khối lượng hỗn hợp X là
Gọi ${n_{{C_6}{H_5}OH}} = \,x\,\,mol\, \to \,{n_{{C_2}{H_5}OH}} = 3x\,\,mol$ (vì tỉ lệ mol là 1:3)
Áp dụng đinh luật bảo toàn nguyên tử:
${n_{C{O_2}}} = \,\,2{n_{{C_2}{H_5}OH}}\,\, + \,\,6{n_{{C_6}{H_5}OH}}\, = \,\,2.3x\, + \,6x\,\, = \,\,12x$ mol
${n_{{H_2}O}} = \,\,3{n_{{C_2}{H_5}OH}} + \,\,3{n_{{C_6}{H_5}OH}} = 3.3x\, + \,3x\,\, = \,\,12x$ mol
Khi cho sản phẩm cháy vào bình đựng dung dịch nước vôi trong xảy ra các phản ứng:
CO2 + Ca(OH)2 $ \to $ CaCO3 ↓ + H2O (1)
2CO2 + Ca(OH)2 $ \to $ Ca(HCO3)2 (2)
Ta có:${n_{CaC{O_3}(1)}} = \frac{{15}}{{100}} = 0,15\,\,mol$
Dung dịch sau phản ứng tác dụng với NaOH dư xảy ra phương trình hóa học sau:
$Ca{(HC{O_3})_2}\, + \,2NaOH \to \,Ca\,C{O_3} \downarrow \, + \,N{a_2}C{O_3} + {H_2}O\,\,\,(3)$
→ ${n_{Ca{{(HC{O_3})}_2}(2)}} = {n_{CaC{O_3}(3)}} = \frac{{7,5}}{{100}} = 0,075\,mol$
→ $\sum {n_{C{O_2}}} = {n_{C{O_2}(1)}} + {n_{C{O_2}(2)}} = {n_{CaC{O_3}(1)}} + 2{n_{Ca{{(HC{O_3})}_2}(2)}} = 0,15 + \,\,2.0,075$= 0,3 mol
Mà ${n_{C{O_2}}}$= 12x → 12x = 0,3 → x = 0,025 mol
→ mhỗn hợp X =${m_{{C_6}{H_5}OH}} + {m_{{C_2}{H_5}OH}}$ = 94.0,025 + 46.3.0,025 = 5,8 gam.
Cho m gam hỗn hợp X gồm phenol và etanol phản ứng hoàn toàn với Na dư thu được 2,24 lít khí H2 (đktc). Mặt khác, m gam hỗn hợp X phản ứng vừa đủ với 100 ml dung dịch NaOH 1M. Giá trị của m là
${n_{{H_2}}} = \frac{{2,24}}{{22,4}} = 0,1\,mol$, nNaOH = 1.0,1 = 0,1 mol
C6H5OH + Na $ \to $ C6H5ONa + $\frac{1}{2}$ H2
C2H5OH + Na $ \to $ C2H5ONa + $\frac{1}{2}$ H2
→ ${n_{{C_6}{H_5}OH}}\, + \,{n_{{C_2}{H_5}OH}}\, = \,2{n_{{H_2}}} = \,2.0,1 = 0,2\,mol$
C6H5OH + NaOH $ \to $ C6H5ONa + H2O
0,1 mol ← 0,1 mol
→ ${n_{{C_2}{H_5}OH}} = \,0,2 - {n_{{C_6}{H_5}OH}}\, = \,0,2 - 0,1 = 0,1\,mol$
→ $m = {m_{{C_6}{H_5}OH}} + {m_{{C_2}{H_5}OH}} = 0,1.94 + 0,1.46 = 14\,\,gam$
Cho dung dịch chứa m gam hỗn hợp gồm phenol (C6H5OH) và axit clohiđric (HCl) tác dụng vừa đủ với nước brom, thu được dung dịch X và 33,1 gam kết tủa. Trung hòa hoàn toàn X cần vừa đủ 500ml dung dịch NaOH 1M. Giá trị của m là
${n_{{C_6}{H_3}B{r_3}O}} = \frac{{33,1}}{{331}} = 0,1\,mol$
Khi cho hỗn hợp C6H5OH và HCl tác dụng với nước brom thì chỉ có phenol phản ứng theo phương trình:
C6H5OH + 3Br2 → C6H2Br3OH↓ + 3HBr
0,1 ← 0,1 → 0,3
→ Dung dịch X: HCl; HBr (0,3 mol)
Khi trung hòa hỗn hợp X bằng dung dịch NaOH:
${n_{{\text{HCl}}}}\, + {n_{HBr}} = {n_{NaOH}} = 1.0,5 = 0,5\,mol$
→ ${n_{{\text{HCl}}}} = \,0,5 - {n_{HBr}} = 0,5 - 0,3 = 0,2\,\,mol$
→ $m = {m_{{C_6}{H_5}OH}} + {m_{HCl}} = O,1.94 + 0,2.36,5 = 16,7$ gam
Đốt cháy 21 gam chất X là dẫn xuất benzen (CTPT trùng với CTĐGN), thu được 23,52 lit CO2 (đktc) và 10,8 gam H2O. Mặt khác, 21 gam X tác dụng vừa đủ với dung dịch NaOH thu được 27,6 gam muối. Số CTCT của X là:
Vì đốt cháy X thu được CO2 và H2O → trong X chứa C, H và có thể có O
${n_{C{O_2}}} = \frac{{23,52}}{{22,4}}= 1,05\,mol;\,{n_{{H_2}O}} = \frac{{10,8}}{{18}} = 0,6\,\,mol$
Áp dụng định luật bảo toàn khối lượng: ${m_X} + {m_{{O_2}}} = {m_{C{O_2}}} + {m_{{H_2}O}}$
→ ${m_{{O_2}}}$ = 1,05.44 + 0,6.18 – 21 = 36 gam → ${n_{{O_2}}}$ = 1,125 mol
Nhận thấy: $2.{n_{{O_2}}} < 2.{n_{C{O_2}}} + {n_{{H_2}O}}$→ trong X chứa O
Áp dụng định luật bảo toàn nguyên tử:
nO trong X = $2.{n_{C{O_2}}} + {n_{{H_2}O}} - 2.{n_{{O_2}}}$= 2.1,05 + 0,6 – 2.1,125 = 0,45 mol
nC trong X = ${n_{C{O_2}}}$= 1,05 mol
nH trong X = 2.${n_{{H_2}O}}$= 1,2 mol
→ nC : nH : nO = 1,05 : 1,2 : 0,45 = 7 : 8 : 3 → CTĐGN của X là C7H8O3
Vì CTPT của X trùng với CTĐGN → CTPT của X là C7H8O3
${n_{{C_7}{H_8}{O_3}}} = \,\,\frac{{21}}{{140}}\,\, = \,\,0,15\,\,mol$
X tác dụng với dung dịch NaOH:
Cứ thay thế 1 nguyên tử H bằng 1 nguyên tử Na thì khối lượng tăng: 23 – 1 = 22
Mà theo bài, khối lượng tăng 27,6 – 21 = 6,6 gam
+)số mol NaOH phản ứng là: nNaOH = $\frac{{6,6}}{{22}}$ = 0,3 mol
→ ${n_{{C_7}{H_8}{O_3}}} = 2{n_{NaOH}}$ → trong X có 2 nhóm -OH tác dụng với NaOH
→ X có 2 nhóm -OH phenol và 1 nhóm -OH ancol hoặc X có 2 nhóm -OH phenol và 1 nhóm ete
Các CTCT của X là
TH1
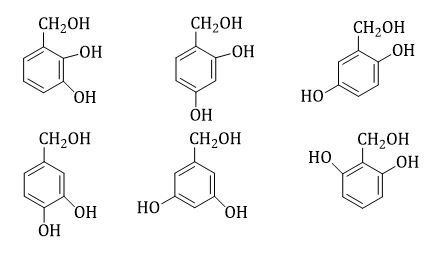
TH2: Thay -CH2OH bằng -OCH3 (6 công thức)
Phản ứng giữa CO2 với dung dịch C6H5ONa xảy ra theo phương trình hóa học sau:
CO2 + H2O + C6H5ONa → C6H5OH + NaHCO3.
Phản ứng xảy ra được là do phenol có:
Dựa vào tính chất: axit mạnh hơn đẩy axit yếu hơn ra khỏi muối tạo thành muối mới và axit mới yếu hơn axit ban đầu.
Do đó axit cacbonic có tính axit mạnh hơn phenol.
Cho 11,28 gam phenol tác dụng với lượng dư dung dịch Br2, sau phản ứng kết thúc thu được m gam kết tủa trắng. Giá trị của m là:
C6H5OH + 3Br2 →C6H2Br3OH + 3HBr
Ta có: nC6H2Br3OH = nphenol = 11,28 : 94 = 0,12 mol → mC6H2Br3OH = 0,12. 331 = 39,72 gam
Để thu được 22,9 gam axit picric cần m gam phenol. Giá trị của m là ? Biết hiệu suất phản ứng đạt 94%.
nax picric = 22,9 : 229 = 0,1 (mol)
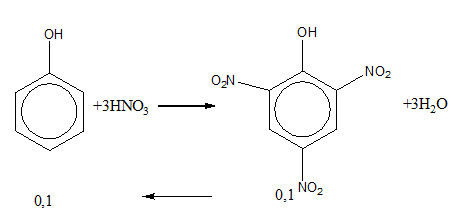 => mC6H5OH lí thuyết = 0,1. 94 = 9,4 (g)
=> mC6H5OH lí thuyết = 0,1. 94 = 9,4 (g)
Vì %H = 94% => mC6H5OH thực tế = mC6H5OH lí thuyết . 100% : %H = 9,4.100% : 94% = 10 (g)

