Thứ tự tăng dần nhiệt độ sôi của các chất HCHO, C2H5OH, H2O là
Anđehit có nhiệt độ sôi thấp hơn ancol có khối lượng phân tử tương đương nhưng cao hơn so với hiđrocacbon có cùng số nguyên tử C trong phân tử.
=> thứ tự tăng dần nhiệt độ sôi: HCHO < C2H5OH < H2O
Oxi hóa 1,2 gam CH3OH bằng CuO đun nóng, sau một thời gian thu được hỗn hợp sản phẩm X gồm HCHO, H2O và CH3OH dư. Cho toàn bộ X tác dụng với dung dịch AgNO3/NH3 dư thu được 12,96 gam Ag. Hiệu suất của phản ứng oxi hóa là
nHCHO = nAg / 4 = 0,03 mol
=> nCH3OH phản ứng = nHCHO = 0,03 mol
=> H = nCH3OH phản ứng / nCH3OH ban đầu = 80%
Chất nào sau đây có nhiệt độ sôi thấp nhất ?
Chất có nhiệt độ sôi thấp nhất là metan.
Oxi hóa không hoàn toàn 4,6 gam một ancol no, đơn chức bằng CuO đun nóng thu được 6,2 gam hỗn hợp X gồm anđehit, nước và ancol dư. Cho toàn bộ hỗn hợp X phản ứng hoàn toàn với lượng dư dung dịch AgNO3 trong NH3 đun nóng thu được m gam Ag. Giá trị của m là
RCH2OH + [O] → RCHO + H2O
Bảo toàn khối lượng: mancol + mO = mhỗn hợp X => nO phản ứng = (6,2 – 4,6) / 16 = 0,1 mol
=> nRCH2OH phản ứng = 0,1 mol => nRCH2OH ban đầu > 0,1 mol
=> Mancol < 4,6 / 0,1 = 46 => ancol là CH3OH => anđehit tạo ra là HCHO
nAg = 4.nHCHO = 0,4 mol => mAg = 43,2 gam
Fomalin hay fomon (dùng để bảo quản xác động vật chống thối rữa) là
Dung dịch nước của anđehit fomic được gọi là fomon. Dung dịch bão hòa của anđehit fomic (có nồng độ 37-40%) được gọi là fomlin.
Hỗn hợp X gồm 1 ancol và 2 sản phẩm hợp nước của propen. Tỉ khối hơi của X so với hiđro bằng 23. Cho m gam X đi qua ống sứ đựng CuO dư nung nóng. Sau khi các phản ứng xảy ra hoàn toàn thu được hỗn hợp Y gồm 3 chất hữu cơ và hơi nước, khối lượng ống sứ giảm 3,2 gam. Cho Y tác dụng hoàn toàn với lượng dư dung dịch AgNO3/NH3 tạo ra 48,6 gam Ag. Phần trăm khối lượng của propan-1-ol trong X là
X chứa C3H7OH và có M = 46 => ancol còn lại là CH3OH
Gọi nCH3CH2CH2OH = a mol; nCH3CH(OH)CH3 = b mol => nCH3OH = a + b mol
=> nO = a + b + a + b = 0,2 (1)
Y gồm CH3CH2CHO (a mol) ; CH3-CO-CH3 (b mol) và HCHO (a + b) mol
=> nAg = 2.nCH3CH2CHO + 4.nHCHO = 2a + 4.(a + b) = 0,45 (2)
Từ (1) và (2) => a = 0,025; b = 0,075
=> %mCH3CH2CH2OH = 16,3%
Đốt hoàn toàn m gam hỗn hợp X gồm hai anđehit cần dùng vừa hết 0,375 mol O2 sinh ra 0,3 mol CO2 và 0,3 mol H2O. Mặt khác, nếu cho m gam hỗn hợp X tác dụng với lượng dư dung dịch AgNO3/NH3 thu được a gam kết tủa. Miền giá trị của a là ?
Đốt anđehit thu được nCO2 = nH2O
=> 2 anđehit là anđehit no, đơn chức, mạch hở
nO (X) = 2nCO2 + nH2O – 2nO2 = 2.0,3 + 0,3 – 2.0,375 = 0,15 mol
=> n anđehit = 0,15 mol
Ctb = 0,3 : 0,15 = 2
=> 1 anđehit là HCHO và anđehit còn lại có số C ≥ 3
+ Do hỗn hợp chứa 1 anđehit đơn chức thông thường và HCHO
=> nAg < 4 n anđehit = 0,6 mol => a < 64,8
+ Giả sử:
HCHO (a mol)
CnH2nO (b mol)
a + b = 0,15 (1)
a + nb = nCO2 = 0,3 (2)
nAg = 4a + 2b = 2a + 2(a + b) = 2a + 2.0,15 = 2a + 0,3
Từ (1) và (2)
=> \(a = \frac{{0,15n - 0,3}}{{n - 1}} = 0,15 - \frac{{0,15}}{{n - 1}}\)
Thay vào số mol Ag ta có: \({n_{Ag}} = 0,6 - \frac{{0,3}}{{n - 1}}\)
Mà n ≥ 3 => nAg ≥ 0,45 mol
=> a ≥ 48,6 gam
Vậy 48,6 ≤ a < 64,8
Cho 8,04 gam hỗn hợp hơi gồm CH3CHO và C2H2 tác dụng hoàn toàn với dung dịch AgNO3/NH3 thu được 55,2 gam kết tủa. Cho kết tủa này vào dung dịch HCl dư, sau khi kết thúc các phản ứng thu được m gam chất rắn không tan. Giá trị của m là
Gọi nCH3CHO = a mol; nC2H2 = b mol
=> 44a + 26y = 8,04 (1)
Kết tủa thu được gồm Ag và Ag2C2
nAg = 2.nCH3CHO = 2a mol; nAg2C2 = nC2H2 = b mol
=> 2a.108 + 240b = 55,2 (2)
Từ (1) và (2) => a = 0,1 mol; b = 0,14 mol
Cho Ag và Ag2C2 vào HCl dư => thu được chất rắn gồm Ag và AgCl
Bảo toàn Ag: nAgCl = 2.nAg2C2 = 0,28 mol
=> m = 108.0,1.2 + 143,5.0,28 = 61,78 gam
Đốt cháy m gam anđehit đơn chức mạch hở X (phân tử chứa không quá 4 nguyên tử cacbon), thu được 6,72 lít CO2 (đktc) và 1,8 gam nước. Mặt khác, khi cho 1,8 gam X phản ứng tối đa với a mol AgNO3 trong NH3. Giá trị của a là
nCO2 = 0,3 mol; nH2O = 0,1 mol
Giả sử công thức phân tử của anđehit là CnH2n+2-2kO
CnH2n+2-2kO → nCO2 + (n+1-k)H2O
0,3 0,1
=> 0,1n = 0,3(n+1-k) => 2n = 3k-3
=> \(k = \frac{{2n + 3}}{3}\)
Do anđehit không chứa quá 4C nên thay các giá trị n = 1, 2, 3, 4 vào thu được nghiệm thỏa mãn là n = 3, k = 3
Vậy CTPT của anđehit là C3H2O, CTCT là CH≡C-CHO
- Cho 1,8 gam X tác dụng với AgNO3: nX = 1,8/54 = 1/30 mol
Cấu tạo của X là CH≡C-CHO: CH≡C- tác dụng với 1 AgNO3; CHO tác dụng với 2 AgNO3
=> 1 X tác dụng với tối đa 3 AgNO3
=> nAgNO3 = 3nX = 0,1 mol
Cho 0,2 mol một anđehit đơn chức, mạch hở X phản ứng vừa đủ với 300 ml dung dịch chứa AgNO3 2M trong NH3. Sau khi phản ứng xảy ra hoàn toàn thu được 87,2 gam kết tủa. Công thức phân tử của anđehit là:
Có nAgNO3 = 0,6 mol = 3nX
Mà X đơn chức => X phải chứa liên kết ba C≡C– ở đầu mạch và có 1 nhóm CHO
Đặt CT của X là CH≡C–R–CHO
=> Lượng kết tủa bao gồm \(\left\{ \begin{array}{l}0,2{\rm{ }}mol{\rm{ }}AgC \equiv C-R-COON{H_4}\\0,4{\rm{ }}mol{\rm{ }}Ag\end{array} \right.\)
=> mkết tủa = 0,2.(194 + R) + 0,4.108 = 87,2 gam
=> R = 26 (C2H2)
=> X là C4H3CHO
Hợp chất hữu cơ X mạch hở có dạng CnHmO. Đốt cháy hết 0,04 mol X bằng 0,34 mol khí O2 thu được 0,44 mol hỗn hợp các khí và hơi. Mặt khác 0,05 mol X tác dụng với lượng dư dung dịch AgNO3 trong NH3 sau phản ứng hoàn toàn thu được khối lượng kết tủa vượt quá 10,8 gam. Biết n nhỏ hơn m. Số đồng phân cấu tạo của X là
Ta có:
Gọi n CO2, n H2O lần lượt là x, y mol
=> x + y = 0,44 (I)
Áp dụng định luật bảo toàn nguyên tố oxi
=> n X + 2. n O2 = 2 . x + y (II)
Từ (I) và (II) => x = 0,28 ; y = 0,16
Số nguyên tử C có trong X là:
n CO2 : n X = 0,28 : 0,04 = 7
Số nguyên tử H có trong X là:
n H2O : n X = 0,16 . 2 : 0,04 = 8
=> CTPT của X là C7H8O
Theo đề bài, 0,05 mol X tác dụng với AgNO3/NH3 thu được kết tủa có khối lượng lớn hơn 10,8 : 108 = 0,1 mol Ag
=>Trong X có chứa 1 nhóm –CHO và 1 liên kết 3 ở đầu mạch
Các công thức cấu tạo của X là:
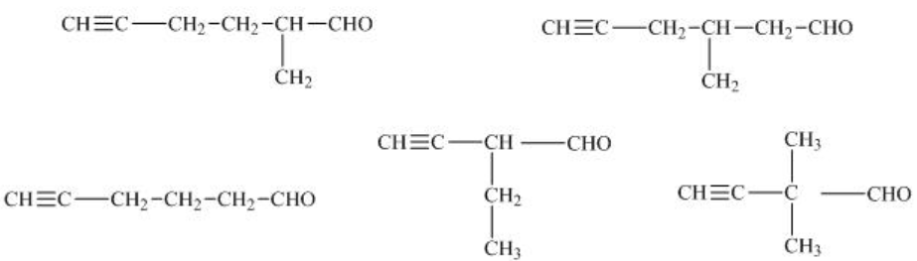
Hỗn hợp X gồm hai chất hữu cơ Y và Z (đều là chất khí ở điều kiện thường, chất có phân tử khối nhỏ Y có phần trăm số mol không vượt quá 50%) có tỉ khối so với H2 là 14. Đốt cháy hoàn toàn hỗn hợp X chỉ thu được CO2 và H2O. Khi cho 4,48 lít hỗn hợp X (đktc) tác dụng vừa đủ với 600 ml dung dịch AgNO3 1M trong NH3 dư thì thu được hỗn hợp kết tủa. Phần trăm thể tích của Y trong hỗn hợp X là
X gồm hai chất có khả năng tác dụng với dung dịch AgNO3/NH3, khi đốt cháy sinh ra CO2 và H2O có MX = 28
=> trong X có C2H2 (Y)
Z có thể là ankin hoặc anđehit
Gọi nY = x mol; nZ = y mol => x + y = 0,2 (1)
nX / nAgNO3 = 0,6 / 0,2 = 3
Như vậy Z phản ứng với AgNO3 có thể theo tỉ lệ 1 : 4 => 2x + 4y = 0,6 (2)
Từ (1), (2) => x = y = 0,1
=> M = (26.0,1 + 0,1.MZ) / 0,2 = 28 => MZ = 30
=> Z là HCHO
%VY = 50%

