Lên men m gam glucozơ với hiệu suất 90%, lượng khí CO2 sinh ra hấp thụ hết vào dung dịch nước vôi trong, thu được 10 gam kết tủa. Khối lượng dung dịch sau phản ứng giảm 3,4 gam so với khối lượng dung dịch nước vôi trong ban đầu. Giá trị của m là
CO2 + Ca(OH)2 → CaCO3 + H2O
a → a → a
CO2 + CaCO3 + H2O → Ca(HCO3)2
b → b → b
Kết tủa tạo ra là : CaCO3 = (a - b).100 = 10 => a - b = 0,1 mol (1)
mdung dịch giảm = m kết tủa - mCO2 = 10 – 44.(a + b) = 3,4 => a + b = 0,15 mol (2)
Từ (1) và (2) => a = 0,125 và b = 0,025 mol
=> nCO2 = 0,125 + 0,025 = 0,15 mol
Phản ứng lên men :
C6H12O6 → 2CO2 + 2C2H5OH
0,075 ← 0,15 mol
Khối lượng C6H12O6 cần cho phản ứng lên men là : 0,075.180 = 13,5 gam
Do hiệu suất là 90% => mmC6H12O6 = 13,5.100/90 = 15 gam
Hỗn hợp A gồm rượu đơn chức no X và H2O. Cho 21 gam A tác dụng Na được 7,84 lít H2 (đktc). Mặt khác, đốt cháy hoàn toàn 21 gam A và cho sản phẩm hấp thụ hết vào dung dịch Ca(OH)2 dư. Khối lượng kết tủa tạo ra trong bình chứa Ca(OH)2 là
GỌi CTPT của X có dạng CnH2n+2O (a mol) và H2O (b mol)
CnH2n+1OH + Na → ½ H2
a → ½ a
H2O + Na → ½ H2
b → ½ b
=> ½ a + ½ b = 0,35
=> a + b = 0,7
CnH2n+2O → nCO2
Ta có: $\left\{ \begin{gathered}\left( {14n{\text{ }} + {\text{ }}18} \right)a{\text{ }} + {\text{ }}18b{\text{ }} = {\text{ }}21 \hfill \\a + b = 0,7 \hfill \\ \end{gathered} \right.\,\, = > \,\,na = 0,6\,\, = {n_{C{O_2}}}$
=> mCaCO3 = 0,6.100 = 60 gam
Cho m gam tinh bột lên men thành ancol etylic với hiệu suất 81%. Toàn bộ lượng CO2 sinh ra được hấp thụ hoàn toàn vào dung dịch Ca(OH)2 thu được 550 gam kết tủa và dung dịch X. Đun kĩ dung dịch X thu thêm được 100 gam kết tủa. Giá trị của m là:
Các phản ứng:
(C6H10O5)n + nH2O → nC6H12O6
C6H12O6→ 2C2H6O + 2CO2
CO2 + Ca(OH)2 → CaCO3 + H2O
2CO2 + Ca(OH)2 + H2O → Ca(HCO3)2
Ca(HCO3)2→ CO2 + CaCO3 + H2O
${n_{C{O_2}}} = \frac{{550 + 2.100}}{{100}} = 7,5mol$
=> ${n_{{C_6}{H_{12}}{O_6}}} = \frac{{{n_{C{O_2}}}}}{2}$ = 3,75 mol
=> m = 3,75 . 162 . 100/81 = 750g
Cho 20,7 gam một ancol đơn chức X tác dụng với CuO dư, nung nóng thu được hỗn hợp Y gồm anđehit, nước và ancol dư. Cho Y tác dụng với Na dư thu được 5,04 lít khí H2 (đktc). Biết H = 88,89%. Ancol X và khối lượng anđehit trong Y là
Gọi công thức của ancol X là RCH2OH có số mol ban đầu là x mol.
Gọi số mol X phản ứng là a mol
RCH2OH + CuO → RCHO + Cu + H2O
a → a → a → a → a mol
→ Hỗn hợp Y gồm $\left\{ \begin{gathered}RCHO\,\,:\,\,\,a\,mol \hfill \\{H_2}O\,\,\,\,\,\,\,\,:\,\,\,a\,mol \hfill \\RC{H_2}OH\,:\,\,(x - a)\,\,mol \hfill \\ \end{gathered} \right.$
RCH2OH + Na $\xrightarrow[{}]{}$ RCH2ONa + $\frac{1}{2}$H2
H2O + Na $\xrightarrow[{}]{}$ NaOH +$\frac{1}{2}$ H2
+) ${n_{RC{H_2}OH}}\,\, + \,\,{n_{{H_2}O}}$= x – a + a = 0,225.2 → MX = $\frac{{20,7}}{{0,45}}\,\, = \,\,46$
→ X là C2H5OH → anđehit trong Y là C2H4O
+) H = 88,89% → a = 0,8889x = 0,8889.0,45 = 0,4 mol
→ manđehit = 0,4.44 = 17,6 gam.
Lên men m gam tinh bột thành ancol etylic. Toàn bộ khí CO2 sinh ra trong quá trình này được hấp thụ hoàn toàn vào dung dịch Ca(OH)2, tạo ra 330 gam kết tủa và dung dịch X. Khối lượng dung dịch X giảm đi so với khối lượng nước vôi trong ban đầu là 132 g. Nếu hiệu suất quá trình lên men tạo thành ancol etylic là 90% thì giá trị của m là
(C6H10O5)n $\xrightarrow{{}}$ 2nC2H5OH + 2nCO2
2,25/n mol 4,5 mol
+) mdung dịch giảm = mkết tủa - mCO2 => mCO2 = 330 – 132 = 198 gam
+) Khối lượng tinh bột phản ứng là : 162n .$\frac{{2,25}}{n}$ = 364,5 gam
Vì H = 90% nên m =$\frac{{364,5.100}}{{90}}$=405 gam
Cho các chất sau: (1) ancol etylic, (2) metan, (3) đimetyl ete, (4) propanol. Dãy sắp xếp theo chiều giảm dần nhiệt độ sôi là
Ancol có nhiệt độ sôi lớn nhất và tăng theo phân tử khối => (4) > (1)
Ankan có nhiệt độ sôi thấp nhất => (2) thấp nhất
=> thứ tự đúng là (4) > (1) > (3) > (2)
Dãy các chất nào sau đây không tan trong nước?
- Ancol tan tốt trong nước => metanol và propanol tan tốt trong nước
=> loại A, C và D
Trong phòng thí nghiệm, khí Y được điều chế và thu vào ống nghiệm theo hình vẽ bên.
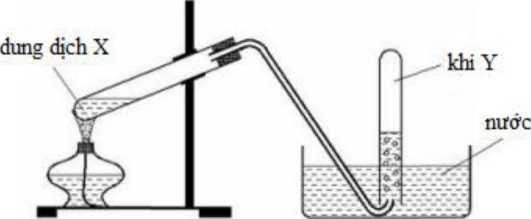
Khí Y được tạo ra từ phản ứng hóa học nào sau đây?
Từ hình vẽ ta thấy:
Khí Y không tan hoặc ít tan trong nước và không có phản ứng với nước
Mà khí Y lại được điều chế từ dd X → dd X là C2H5OH và khí Y là C2H4
Cho biết X mạch hở. Đốt cháy a mol X thu được 4a mol CO2 và 4a mol H2O. Nếu cho a mol X tác dụng hết với Na thu được a mol H2. Số CTCT thỏa mãn của X là
Ta có: Số C = nCO2 : nX = 4a : a = 4;
Số H = 2nH2O : nX = 2.4a : a = 8
→ X có công thức C4H8Ox
Cứ a mol X phản ứng với Na sinh ra 0,5ax mol H2 → 0,5ax = a → x = 2
Vậy X có công thức C4H8O2 có số liên kết π + vòng = 1
Các đồng phân cấu tạo ancol đa chức, mạch hở của X là:
HO-CH2-CH(OH)-CH =CH2
CH2OH-CH =CH-CH2OH
CH2 =C(CH2OH)-CH2OH
Vậy X có 3 CTCT thỏa mãn.
Đốt cháy hoàn toàn x gam ancol X rồi cho các sản phầm cháy vào bình đựng dung dịch Ca(OH)2 dư thấy khối lượn bình tăng y gam và tạo z gam kết tủa. Biết 100y = 71z; 102z = 100(x + y). Có các nhận xét sau:
a. X có nhiệt độ sôi cao hơn ancol etylic
b. Từ etilen phải ít nhất qua 2 phản ứng mới tạo được X
c. X tham gia được phản ứng trùng ngưng
d. Ta không thể phân biệt được X với C3H5(OH)3 chỉ bằng thuốc thử Cu(OH)2
e. Đốt cháy hoàn toàn X thu được số mol nước lớn hơn số mol CO2
Số phát biểu đúng là
\(\left\{ \begin{gathered}100y = 71z \\102z = 100(x + y) \\\end{gathered} \right. \to \left\{ \begin{gathered}y = 0,71z\,(g) \\x = 0,31z\,(g) \\\end{gathered} \right.\)
Ta có a g X + O2 → CO2 + H2O
CO2 + Ca(OH)2 → CaCO3 + H2O
nCaCO3 = z : 100 = 0,01z mol → nCO2 = nCaCO3 = 0,01z (mol)
mbình tăng = mCO2 + mH2O = 44.0,01z + 18nH2O = y → nH2O = \(\frac{{y - 0,44z}}{{18}}\) mol
Bảo toàn C có nC(X) =nCO2 = 0,01z mol
Bảo toàn H có nH(X) = 2nH2O = \(2.\frac{{y - 0,44z}}{{18}} = 2.\frac{{0,71z - 0,44z}}{{18}} = 0,03z\)mol
Ta có mX = mC + mH + mO = x → 0,31z = 12.0,01z + 0,03z.1 + mO → mO = 0,16z → nO = 0,01z
→X có C : H : O = nC : nH : nO = 0,01z : 0,03z : 0,01z = 1:3 :1
→CTĐGN là CH3O→ CTPT là (CH3O)n thì 3n ≤ 2n+ 2→ n ≤ 2 → n = 2
→X là C2H6O2
a. Đúng
b. sai vì chỉ cần cho C2H4 +KMnO4 →C2H4(OH)2
c. đúng vì X là chất điều chế tơ lapsan
d. đúng vì cả hai đều tạo phức màu xanh lam
e. đúng
→ có 4 phát biểu đúng
Cho Na tác dụng vừa đủ với 1,24 gam hỗn hợp 3 ancol, thu được 336 ml khí H2 (đktc). Khối lượng muối natri thu được là:
Đặt công thức chung của 3 ancol là R(OH)x
R(OH)x + x Na → R(ONa)x + x/2 H2
Theo PTHH: nNa = 2.nH2 = 2. 0,336 : 22,4 = 0,03 mol
Áp dụng định luật bảo toàn khối lượng ta có:
mmuối natri = mancol + mNa – mH2 = 1,24 + 0,03.23 – 0,015.2 = 1,9 gam
Hỗn hợp X gồm metanol, etanol, propan -1-ol, và H2O. Cho m gam X tác dụng với Na dư thu được 15,68 lít khí H2 (đktc). Mặt khác đốt cháy hoàn toàn X thu được V lít CO2 (đktc) và 46,8 gam H2O. Giá trị của m và V lần lượt là
nH2(ĐKTC) = 15,68 :22,4 = 0,7 (mol); nH2O = 46,8 : 18 = 2,6 (mol)
nhh X = nOH- = 2nH2 = 2.0,7 = 1,4 (mol)
X toàn là chất no nên khi đốt cháy có: nX = nH2O – nCO2
=> 1,4 = 2,6 – nCO2
=> nCO2 = 1,2 (mol)
=> VCO2(đktc) = 1,2.22,4 = 26,88 (l)
BTKL ta có: mX = mC + mH + mO = 1,2.12 + 2,6.2 + 1,4.16 = 42 (g)

