Hòa tan 6g NaOH vào 44g nước được dd A có khối lượng riêng bằng 1,12g/ml. Cần lấy bao nhiêu ml A để có số mol ion OH– bằng 2.10–3 mol
\({m_{{\rm{dd}}}} = {m_{NaOH}} + {m_{{H_2}O}} = 6 + 44 = 50(g)\)
\( \to {V_{dd}} = m:d = 50:1,12 = \frac{{625}}{{14}}ml\)
\({n_{NaOH}} = \frac{6}{{40}} = 0,15(mol)\)
\( \to {C_{MNaOH}} = n:{V_{dd}} = \frac{{0,15}}{{\frac{{625}}{{14}}{{.10}^{ - 3}}}} = 3,36(M)\)
NaOH → Na+ + OH−
Theo pt: nNaOH = nOH- = 2.10-3 (mol)
⟹ Thể tích dd A cần lấy là: V = n : CM = 2.10-3 : 3,36 = 6.10-4 (l) = 0,6 (ml)
A là dung dịch HCl nồng độ 0,01M. Nồng độ của các ion trong dung dịch khi pha loãng A 100 lần là:
Khi pha loãng dung dịch 100 lần thì nồng độ các ion trong dung dịch cũng giảm 100 lần
HCl→H+ + Cl−
Trước khi pha loãng: $${\rm{[}}{{\rm{H}}^ + }{\rm{]}} = {\rm{[C}}{{\rm{l}}^ - }{\rm{]}} = 0,01M$$
Sau khi pha loãng: $${\rm{[}}{{\rm{H}}^ + }{\rm{]}} = {\rm{[C}}{{\rm{l}}^ - }{\rm{]}} = 1,{0.10^{ - 4}}M$$
Cho các chất sau tan trong nước: Na2CO3, CH3COOCH3, HCOOH, MgCl2, HF. Số chất điện li mạnh và điện li yếu lần lượt là:
- Chất điện li mạnh:
Na2CO3 → 2Na+ + CO32-
MgCl2 → Mg2+ + 2Cl-
- Chất điện li yếu:
HCOOH ⇄ HCOO- + H+
HF ⇄ H+ + F-
- Chất không điện li: CH3COOCH3
Cho các nhận xét sau:
(1) Những chất điện li mạnh là các axit mạnh như HCl, HNO3, H2SO4…; các bazơ mạnh như NaOH, KOH, Ba(OH)2… và hầu hết các muối.
(2) Dãy các chất H2S, H2CO3, H2SO3 là các chất điện li yếu.
(3) Muối là hợp chất khi tan trong nước chỉ phân li ra cation kim loại và anion gốc axit.
(4) Nước cất có khả năng dẫn điện tốt do nước có thể phân li ra ion H+ và OH-.
Số nhận xét đúng là?
(1) đúng
(2) đúng
(3) sai. VD: (NH4)2CO3 là muối điện li ra ion NH4+ không phải là ion kim loại.
(4) sai vì nước cất không dẫn điện
→ Vậy có 2 nhận xét đúng
Tiến hành thí nghiệm như hình vẽ:
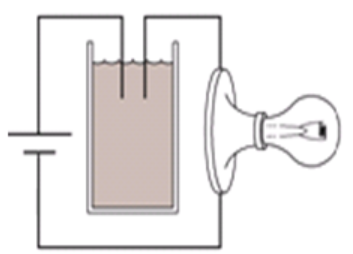
Ban đầu trong cốc chứa nước vôi trong. Sục rất từ từ CO2 vào cốc cho tới dư. Hỏi độ sáng của bóng đèn thay đổi như thế nào?
+ Khi CO2 vào thì ban đầu nước vôi trong dư so với CO2 nên ion Ca2+ dần đến hết vì bị kết tủa thành CaCO3
⟹ lượng ion trong dung dịch giảm dần về 0
+ Khi CO2 dư thì kết tủa lại bị hòa tan, tạo thành ion Ca2+ và HCO3-
⟹ lượng ion tăng dần
Vậy đèn có độ sáng giảm dần đến tắt rồi lại sáng tăng dần.
Đáp án A
Kết luận nào sau đây không đúng?
A, B, C đúng
D sai vì chất điện li mạnh là chất khi tan trong nước phân li hoàn toàn thành ion
Cho các nhận xét sau:
(1) Những chất điện li mạnh là các axit mạnh như HCl, HNO3, H2SO4…; các bazơ mạnh như NaOH, KOH, Ba(OH)2… và hầu hết các muối.
(2) Dãy các chất H2S, H2CO3, H2SO3 là các chất điện li yếu.
(3) Muối là hợp chất khi tan trong nước chỉ phân li ra cation kim loại và anion gốc axit.
(4) Nước cất có khả năng dẫn điện tốt do nước có thể phân li ra ion H+ và OH-.
Số nhận xét đúng là?
(1) đúng.
(2) đúng.
(3) sai. VD: (NH4)2CO3 là muối điện li ra ion NH4+ không phải là ion kim loại.
(4) sai, vì nước cất không dẫn điện
→ Vậy có 2 nhận xét đúng.