Đốt cháy hoàn toàn hỗn hợp X gồm hai hiđrocacbon kế tiếp nhau trong dãy đồng đẳng, thu được 2,24 lít khí CO2 (đktc) và 3,24 gam H2O. Hai hiđrocacbon trong X là
nCO2 = 0,1 mol ; nH2O = 0,18 mol => nH2O > nCO2 => 2 hiđrocacbon là ankan
=> nankan = nH2O – nCO2 = 0,18– 0,1 = 0,08 mol
\( = > \,\,\bar C = \dfrac{{{n_{C{O_2}}}}}{{{n_{ankan}}}} = \dfrac{{0,1}}{{0,08}} = 1,25\)
=> có 1 ankan có số C < 1 và 1 ankan có số C > 1
=> 2 ankan thỏa mãn là CH4 và C2H6
Đốt cháy 13,7 ml hỗn hợp A gồm metan, propan và cacbon (II) oxit, ta thu được 25,7 ml khí CO2 ở cùng điều kiện nhiệt độ và áp suất. Thành phần % thể tích propan trong hỗn hợp A và khối lượng phân tử trung bình của hỗn hợp A so với nitơ là :
Đặt số mol của metan, propan và cacbon (II) oxit lần lượt là x, y, z
Sơ đồ phản ứng :
CH4 CO2 (1) ; C3H8 3CO2 (2) ; CO CO2 (3)
x x y 3y z z
Từ (1), (2), (3) và giả thiết ta có hệ :
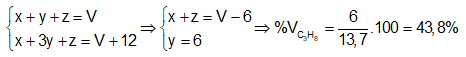
Khối lượng mol trung bình của hỗn hợp A là :
\({\overline M _A} = \dfrac{{16x + 44y + 28z}}{{x + y + z}} > \dfrac{{16(x + z) + 44y}}{{x + y + z}} = \dfrac{{16.7,7 + 44.6}}{{13,7}} = 28,3\,\,gam/mol\)
Mặt khác
\({M_{{N_2}}} = 28\,\,gam/mol\) nên suy ra khối lượng phân tử trung bình của A lớn hơn so với N2 hay \(\dfrac{{\overline M {}_A}}{{{M_{{N_2}}}}} > 1.\)
Nạp một hỗn hợp khí có V lít khí ankan A (CnH2n+2) và 4V lít khí O2 (dư) vào khí nhiên kế. Sau khi cho nổ rồi cho hơi nước ngưng tụ ở nhiệt độ ban đầu thì áp suất trong khí nhiên kế giảm đi 2 lần. Công thức phân tử của ankan A là :
Để đơn giản cho việc tính toán ta chọn số mol của A là 1 mol và của O2 là 4 mol
Phương trình phản ứng :
\({C_n}{H_{2n + 2}}\,\,\, + \,\,\,\,\,(\dfrac{{3n + 1}}{2})\,{O_2}\,\,\,\,\xrightarrow{{{t^o}}}\,\,\,nC{O_2}\,\,\,\, + \,\,\,\,(n + 1){H_2}O\)
bđ: 1 4 : mol
pư: 1 \((\dfrac{{3n + 1}}{2})\) n (n+1) : mol
spư: 0 4 -\((\dfrac{{3n + 1}}{2})\) n (n+1) : mol
Vì sau phản ứng hơi nước đã ngưng tụ nên chỉ có O2 dư và CO2 gây áp suất nên bình chứa.
Tổng số mol khí trước phản ứng : n1 = 1 + 4 = 5 mol
Tổng số mol khí sau phản ứng : n2 = 4 -\((\dfrac{{3n + 1}}{2})\)+ n = (3,5 – 0,5n) mol
Do nhiệt độ trước và sau phản ứng không đổi nên :
\(\dfrac{{{n_1}}}{{{n_2}}} = \dfrac{{{p_1}}}{{{p_2}}} \Rightarrow \dfrac{5}{{3,5 - 0,5n}} = \dfrac{{{p_1}}}{{0,5{p_1}}} = 2 \Rightarrow n = 2\)
Vậy A là C2H6
Cho 0,4 lít hỗn hợp khí M gồm CO2 và một hiđrocacbon X vào bình kín có chứa sẵn 1,5 lít O2. Bật tia lửa điện để phản ứng xảy ra hoàn toàn, thu được 0,6 lít CO2 và 0,6 lít H2O (hơi). Các thể tích khí đo ở cùng điều kiện nhiệt độ, áp suất. Công thức của X là
Ta thấy \(2{V_{C{O_2}}} + {V_{{H_2}O}} < 2{V_{{O_2}}}\) nên sau phản ứng O2 còn dư, X phản ứng hết.
Mặt khác, khi đốt X có \({V_{C{O_2}}} < {V_{{H_2}O}}\) => X là ankan
Gọi CTPT của X là CnH2n+2
Trong hỗn hợp khí M đặt \({V_{C{O_2}}} = a;{V_X} = b\)
=> a + b = 0,4 (1)
Ta có:
\({V_{C{O_2}}} = a + nb = 0,6\)
\({V_{{H_2}O}} = (n + 1)b = 0,6\)
Từ (1), (2), (3) ta được
a = b = 0,2; n=2
=> Công thức của X là C2H6
Khi đốt cháy hoàn toàn 3,60g ankan X thu được 5,60 lít khí CO2 (ở đktc). Công thức phân tử của X là trường hợp nào sau đây?
Ta có: nCO2 = 0,25 mol
Đặt công thức phân tử của ankan là CnH2n+2 có số mol là a mol
Ta có: mankan X = a. (14n+2) = 3,60 gam; nCO2 = an = 0,25 mol
Suy ra a = 0,05; n = 5
Vậy công thức phân tử của ankan X là C5H12.
Đốt cháy hoàn toàn hỗn hợp X gồm 2 hiđrocacbon A và B là đồng đẳng kế tiếp thu được 96,8 gam CO2 và 57,6 gam H2O. Công thức phân tử của A và B là:
Theo đề bài ta có: nCO2 = 2,2 mol; nH2O = 3,2 mol
Nhận thấy: nH2O > nCO2 => 2 hidrocacbon thuộc dãy đồng đẳng của ankan.
=> nankan = nH2O – nCO2 = 3,2 - 2,2 = 1 mol
=> Số C trung bình = nCO2 / nankan = 2,2
Do 2 ankan là đồng đẳng liên tiếp nên là C2H6 và C3H8.
Đốt cháy hoàn toàn 2,24 lít hỗn hợp A (đktc) gồm CH4, C2H6 và C3H8 thu được V lít khí CO2 (đktc) và 7,2 gam H2O. Giá trị của V là:
nH2O = 0,4 mol
Ta thấy tất cả các khí trong hỗn hợp đều là ankan.
=> nA = nH2O – nCO2 => nCO2 = nH2O – nA = 0,3 mol => V = 6,72 lít
Khi đốt cháy hoàn toàn 3,6g một ankan X thu được 5,6 lít khí CO2 (đktc). Công thức phân tử của X là:
Có : nC(X) = nCO2 = 0,25 mol
Mà mX = mC + mH => nH = 0,6 mol
=> nC : nH = 0,25 : 0,6 = 5 : 12
Vì CTTQ của ankan là CnH2n+2 => X là C5H12
Khi đốt cháy hoàn toàn V lít C2H6 (đktc) thu được 44 gam CO2 và 27 gam H2O. Giá trị của V là :
nCO2 = 1 mol ; nH2O = 1,5 mol
Áp dụng công thức : nankan = nH2O – nCO2 = 1,5 – 1 = 0,5 mol
=> VC2H6 = 0,5.22,4 = 11,2 lít
Khi đốt cháy hoàn toàn 7,84 lít hỗn hợp khí gồm CH4, C2H6, C3H8 (đktc) thu được 16,8 lít khí CO2 (đktc) và x gam H2O. Giá trị của x là :
nankan = 0,35 mol ; nCO2 = 0,75 mol
Áp dụng công thức : nankan = nH2O – nCO2 => nH2O = 0,75 + 0,35 = 1,1 mol
=> mH2O = 1,1.18 = 19,8 gam
Đốt cháy hoàn toàn m gam hỗn hợp X gồm CH4, C3H6 và C4H10 thu được 17,6 gam CO2 và 10,8 gam H2O. Giá trị của m là
- nCO2 = 0,4 mol; nH2O = 0,6 mol
- Áp dụng định luật bảo toàn nguyên tố: nC = nCO2 = 0,4 mol; nH = 2.nH2O = 1,2 mol
- Bảo toàn khối lượng: mankan = mC + mH = 12.0,4 + 1.1,2 = 6 gam
Đốt cháy một hỗn hợp hiđrocacbon ta thu được 2,24 lít CO2 (đktc) và 2,7 gam H2O thì thể tích O2 đã tham gia phản ứng cháy (đktc) là :
nCO2 = 0,1 mol; nH2O = 0,15 mol
Bảo toàn nguyên tố O: $2.{{n}_{{{O}_{2}}}}=2.{{n}_{C{{O}_{2}}}}+{{n}_{{{H}_{2}}O}}=>\,\,{{n}_{{{O}_{2}}}}=\frac{2.{{n}_{C{{O}_{2}}}}+{{n}_{{{H}_{2}}O}}}{2}=\frac{2.0,1+0,15}{2}=0,175\,\,mol$
=> VO2 = 0,175.22,4 = 3,92 lít
Đốt cháy hoàn toàn m gam hỗn hợp X gồm hai hiđrocacbon thuộc cùng dãy đồng đẳng cần dùng 6,16 lít O2 và thu được 3,36 lít CO2 (các thể tích khí đo ở đktc). Giá trị của m là
nO2 = 0,275 mol ; nCO2 = 0,15 mol
Bảo toàn nguyên tố O : $2.{{n}_{{{O}_{2}}}}=2.{{n}_{C{{O}_{2}}}}+{{n}_{{{H}_{2}}O}}=>\,\,{{n}_{{{H}_{2}}O}}=2.{{n}_{{{O}_{2}}}}-2.{{n}_{C{{O}_{2}}}}=2.0,275-2.0,15=0,25mol$
Bảo toàn nguyên tố C và H : nC (trong X) = nCO2 = 0,15 mol ; nH (trong X) = 2.nH2O = 0,5 mol
Bảo toàn khối lượng : mX = mC (trong X) + mH (trong X) = 12.0,15 + 0,5 = 2,3 gam
Đốt cháy hoàn toàn 0,15 mol hỗn hợp 2 ankan thu được 9,45 gam H2O. Cho sản phẩm cháy vào dung dịch Ca(OH)2 dư thì khối lượng kết tủa thu được là
Đốt cháy ankan ta có nCO2 = nH2O – nankan = 0,525 – 0,15 = 0,375 mol
=> mkết tủa = 0,375.100= 37,5 gam
Đốt cháy hoàn toàn 0,2 mol hiđrocacbon X. Hấp thụ toàn bộ sản phẩm cháy vào nước vôi trong được 20 gam kết tủa. Lọc bỏ kết tủa rồi đun nóng phần nước lọc lại có 10 gam kết tủa nữa. Vậy X không thể là :
CO2 + Ca(OH)2 → CaCO3↓ + H2O
2CO2 + Ca(OH)2 → Ca(HCO3)2
Ca(HCO3)2 → CaCO3↓ + CO2 + H2O
Từ các phản ứng, ta có: nCO2 sinh ra = nCaCO3 + 2.nCa(HCO3)2 = 0,2 + 2.0,1 = 0,4 mol
=> số C trong X = $\frac{{{n}_{C{{O}_{2}}}}}{{{n}_{ankan}}}=\frac{0,4}{0,2}=2$
=> X không thể là CH4
Đốt cháy hoàn toàn một hiđrocacbon X thu được 0,11 mol CO2 và 0,132 mol H2O. Khi X tác dụng với khí clo thu được 4 sản phẩm monoclo. Tên gọi của X là :
Vì đốt cháy hiđrocacbon X thu được nH2O > nCO2 => X là ankan
nX = nH2O – nCO2 = 0,132 – 0,11 = 0,022 mol
=> số C trong X = $\frac{{{n}_{C{{O}_{2}}}}}{{{n}_{ankan}}}$ = 5 => X là C5H12
C5H12 + Cl2 → 4 sản phẩm monoclo => X có CTCT: (CH3)2CH-CH2-CH3 (2-metylbutan)
Đốt cháy hoàn toàn một lượng hiđrocacbon X. Hấp thụ toàn bộ sản phẩm cháy vào dung dịch Ba(OH)2 dư tạo ra 29,55 gam kết tủa, dung dịch sau phản ứng có khối lượng giảm 19,35 gam so với dung dịch Ba(OH)2 ban đầu. Công thức phân tử của X là
mdung dịch giảm = mkết tủa – (mCO2 + mH2O)
=> mCO2 + mH2O = mkết tủa - mdung dịch giảm = 29,55 – 19,35 = 10,2 gam
Bảo toàn nguyên tố C: nC = nCO2 = nBaCO3 = 0,15 mol
=> mH2O = 10,2 – mCO2 = 10,2 – 0,15.44 = 3,6 gam => nH2O = 0,2 mol
Bảo toàn nguyên tố H: nH = 2nH2O = 2.0,2 = 0,4 mol
=> nC : nH = 0,15 : 0,4 = 3 : 8 => X là C3H8
Đốt cháy hoàn toàn một hiđrocacbon A. Sản phẩm thu được hấp thụ hoàn toàn vào 200 ml dung dịch Ca(OH)2 0,2M thấy thu được 3 gam kết tủa. Lọc bỏ kết tủa, cân lại phần dung dịch thấy khối lượng tăng lên so với ban đầu là 0,28 gam. Hiđrocacbon trên có CTPT là
Theo giả thiết ta có : Do đó có hai trường hợp xảy ra :
TH1: Ca(OH)2 dư, chỉ xảy ra phản ứng tạo kết tủa :
CO2 + Ca(OH)2 → CaCO3 + H2O (1)
0,03 0,03 0,03
mdung dịch tăng = ${{m}_{{{H}_{2}}O}}+{{m}_{C{{O}_{2}}}}-{{m}_{CaC{{O}_{3}}}}=0,28\,\,gam\Rightarrow {{m}_{{{H}_{2}}O}}=0,28+3-0,03.44=\,\,1,96\,\,gam$
$\Rightarrow {{n}_{{{H}_{2}}O}}=0,1088\,\,mol\Rightarrow {{n}_{H}}=0,217\,\,mol\Rightarrow {{n}_{C}}:{{n}_{H}}=0,03:0,217=1:7,3\,\,(loại).$
TH2 : Ca(OH)2 phản ứng hết :
CO2 + Ca(OH)2 → CaCO3 + H2O (1)
0,03 0,03 0,03
2CO2 + Ca(OH)2 → Ca(HCO3)2 (2)
0,02 0,01
$\Rightarrow {{n}_{C{{O}_{2}}}}=0,05\,\,mol.$
mdung dịch tăng = ${{m}_{{{H}_{2}}O}}+{{m}_{C{{O}_{2}}}}-{{m}_{CaC{{O}_{3}}}}=0,28\,\,gam\Rightarrow {{m}_{{{H}_{2}}O}}=0,28+3-0,05.44=\,\,1,08\,\,gam$
$\Rightarrow {{n}_{{{H}_{2}}O}}=0,06\,\,mol\Rightarrow {{n}_{H}}=0,12\,\,mol\Rightarrow {{n}_{C}}:{{n}_{H}}=0,05:0,12=5:12\,$
Vậy CTPT của ankan là C5H12
Trộn 2 thể tích bằng nhau của C3H8 và O2 rồi bật tia lửa điện đốt cháy hỗn hợp. Sau phản ứng làm lạnh hỗn hợp (để hơi nước ngưng tụ) rồi đưa về điều kiện ban đầu. Thể tích hỗn hợp sản phẩm khi ấy (V2) so với thể tích hỗn hợp ban đầu (V1) là :
Phương trình phản ứng :
$\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,{{C}_{3}}{{H}_{8}}\,\,\,+\,\,\,\,\,5{{O}_{2}}\,\,\,\xrightarrow{{{t}^{o}}}\,\,\,\,\,3C{{O}_{2}}\,\,\,\,\,\,\,+\,\,\,\,\,\,4{{H}_{2}}O\,\,\,\,\,\,\,\,\,(1)$
$bđ\,(lit):\,\,\,\,\,\,\,\,x\,\,\,\,\,\,\,\to \,\,\,\,\,x\,\,\,\,\,\,\,\,\,\,\,\,\,\,$
$pứ\,(lit):\,\,\,\,\,\,\,\,\frac{x}{5}\,\,\,\,\,\leftarrow \,\,\,\,\,x\,\,\,\,\,\,\,\,\,\,\,\to \,\,\,\,\frac{3x}{5}\,\,\,\,\,\,\,\to \,\,\,\,\,\,\,\,\frac{4x}{5}$
$spứ\,(lit):\,\,\,\,\,\frac{4x}{5}\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,0\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\frac{3x}{5}\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\frac{4x}{5}$
Sau phản ứng hơi nước bị ngưng tụ nên hỗn hợp khí còn lại gồm C3H8 và CO2 sinh ra sau phản ứng. Ta có :
${{V}_{1}}={{V}_{C{}_{3}{{H}_{8}}}}+{{V}_{{{O}_{2}}}}=2x\,\,\,l\acute{i}t;\,\,{{V}_{2}}={{V}_{C{}_{3}{{H}_{8}}\,\,dư}}+{{V}_{C{{O}_{2}}}}=\frac{4x}{5}\,+\frac{3x}{5}=\frac{7x}{5}\,\,l\acute{i}t\Rightarrow \frac{{{V}_{2}}}{{{V}_{1}}}=\frac{7}{10}.$
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (ở đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là :
${{n}_{C{{O}_{2}}}}=\frac{7,84}{22,4}=0,35\,\,mol;\,\,{{n}_{{{H}_{2}}O}}=\frac{9,9}{18}=0,55\,\,mol.$
Bảo toàn nguyên tố O: 2.nO2 = 2.nCO2 + nH2O => 2x = 0,35.2 + 0,55 => x = 0,625
Thể tích không khí cần dùng là nhỏ nhất => oxi trong không khí phản ứng vừa đủ
$=>{{V}_{O{}_{2}\,\,(đktc)}}=0,625.22,4=14\,\,l\acute{i}t\Rightarrow {{V}_{Không \,Khí\,\,(đktc)}}=5.14\,\,=70\,\,l\acute{i}t.$

