Sự điện li là quá trình
Sự điện li là quá trình phân li ra ion của các chất trong nước.
Dung dịch thu được khi trộn lẫn 200 ml dung dịch NaCl 0,2M và 300 ml dung dịch Na2SO4 0,2M có nồng độ cation Na+ là bao nhiêu?
nNaOH = 0,04 mol và nNa2SO4 = 0,12 mol
Phương trình phân li: NaOH → Na+ + OH-
0,04 → 0,04 mol
Na2SO4 → 2Na+ + SO42-
0,06 → 0,12 mol
→ nNa+ = 0,16 mol → [Na+] = 0,16 : 0,5 = 0,32 M
Dung dịch X chứa hỗn hợp axit H2SO4 1,5M và HCl 1M. Số mol của ion H+ trong 300 ml dung dịch X là (coi như H2SO4 điện li hoàn toàn):
Ta có: nH2SO4 = 1,5.0,3 = 0,45 mol; nHCl = 1.0,3 = 0,3 mol
PT điện li:
H2SO4 → 2H+ + SO42-
HCl → H+ + Cl-
⟹ nH+ = 2nH2SO4 + nHCl = 2.0,45 + 0,3 = 1,2 mol
Chất không điện li là
A: CH3OH là chất không điện li
B: CH3COOH là chất điện li yếu
C: NaF là chất điện li mạnh.
D: HF là chất điện li yếu.
Chất không điện li là
A: CH3OH là chất không điện li
B: CH3COOH là chất điện li yếu
C: NaF là chất điện li mạnh.
D: HF là chất điện li yếu.
Dung dịch K2SO4 0,05M có nồng độ mol ion K+ bằng
Phương trình điện ly: \({K_2}S{O_4} \to 2{K^ + } + SO_4^{2 - }\)
Theo phương trình điện ly: \({\rm{[}}{{\rm{K}}^ + }{\rm{]}} = 2.{\rm{[}}{K_2}S{O_4}{\rm{] = 2}}{\rm{.0,05 = 0,1}}\,\,{\rm{M}}\)
Chất không điện li là
A: CH3OH là chất không điện li
B: CH3COOH là chất điện li yếu
C: NaF là chất điện li mạnh.
D: HF là chất điện li yếu.
Chất nào là chất điện ly mạnh nhất trong số các chất sau?
H2SO4 là axit mạnh nên là chất điện ly mạnh
H2CO3, H2O, H3PO4 là các chất điện ly yếu
Vậy H2SO4 là chất điện ly mạnh nhất
Dãy gồm các chất nào sau đây đều có khả năng dẫn điện được?
A. Khí HCl không có khả năng dẫn điện.
B. Cả 4 chất đều không có khả năng dẫn điện.
C. Cả 4 chất đều không có khả năng dẫn điện.
D. Cả 4 chất đều dẫn điện được.
Trường hơp nào sau đây dẫn điện được:
A. Loại vì nước cất phân li ra ion rất ít, lượng ion này không đủ để dung dịch dẫn được điện.
B. Loại vì NaOH rắn khan tồn tại dưới dạng tinh thể ion.Tinh thể ion rất bền vững vì lực hút tĩnh điện giữa các ion ngược dấu trong tinh thể ion rất lớn. Các ion K+" style="box-sizing: border-box;" id="MathJax-Element-1-Frame">K+, OH- chỉ dao động tại các đầu nút của mạng tinh thể (không chuyển dịch tự do) vì vậy, NaOH rắn khan không dẫn điện.
C. Loại vì khí hiđroclorua tồn tại dạng phân tử, không phân li ra ion, do đó không dẫn được điện.
D. Thỏa mãn vì nước biển có thành phần chính là NaCl phân li ra ion Na+ và Cl-chuyển động tự do nên dẫn được điện.
Trộn 150 ml dung dịch MgCl2 0,5M với 50 ml dung dịch NaCl 1M thì nồng độ ion Cl- trong dung dịch mới là
nMgCl2 = 0,15.0,5 = 0,075 mol; nNaCl = 0,05.1 = 0,05 mol
MgCl2 và NaCl là các chất điện li mạnh, khi hòa tan vào nước phân li hoàn toàn thành các ion:
MgCl2 → Mg2+ + 2Cl-
0,075 → 0,15 (mol)
NaCl → Na+ + Cl-
0,05 → 0,05 (mol)
=> nCl- = 0,15 + 0,05 = 0,2 mol
=> [Cl-] = n : V = 0,2 : (0,15 + 0,05) = 1M
Cho các chất dưới đây: H2O, HCl, NaOH, NaCl, CH3COOH, CuSO4, HgCl2, Al(OH)3. Các chất điện li yếu là:
Các chất điện li yếu là: H2O, CH3COOH, HgCl2, Al(OH)3.
H2O \( \rightleftarrows \) H+ + OH-
CH3COOH \( \rightleftarrows \) CH3COO- + H+
HgCl2 \( \rightleftarrows \) Hg2+ + 2Cl-
Al(OH)3 \( \rightleftarrows \) Al3+ + 3OH‑
Phương trình điện li nào sau đây viết đúng?
A. Sai vì H2SO4 là axit mạnh do đó phương trình điện li: H2SO4 → H+ + HSO4-
B. Đúng
C. Sai, sửa H2SO3 \( \rightleftarrows \) 2H+ + SO32-
D. Sai, Na2S → 2Na+ + S2-
Có 4 dung dịch: NaCl, C6H12O6 (glucozơ), CH3COOH, K2SO4 đều có nồng độ 0,1 mol/lít. Dung dịch chứa chất tan có khả năng dẫn điện tốt nhất là
- NaCl là chất điện li mạnh, điện li hoàn toàn thành ion => Tổng nồng độ ion là 0,1 + 0,1 = 0,2M
- C6H12O6 (glucozơ) không phân li nên nồng độ ion bằng 0
- CH3COOH là chất điện li yếu => Tổng nồng độ ion nhỏ hơn 0,2M
- K2SO4 là chất điện li mạnh, điện li hoàn toàn thành ion => Tổng nồng độ ion là 0,2 + 0,1 = 0,3M
Vậy dung dịch dẫn điện tốt nhất trong các dung dịch cùng nồng độ trên là K2SO4.
Dung dịch nào sau đây dẫn điện tốt nhất? Biết chúng đều có cùng nồng độ mol là 0,1M.
A. KOH là chất điện li mạnh nên phân li hoàn toàn ⟹ Tổng nồng độ ion là 0,2M
B. BaCl2 là chất điện li mạnh nên phân li hoàn toàn ⟹ Tổng nồng độ ion là 0,3M
C. H2S là chất điện li yếu nên phân li không hoàn toàn ⟹ Tổng nồng độ ion nhỏ hơn 0,3M
D. HF là chất điện li yếu nên phân li không hoàn toàn ⟹ Tổng nồng độ ion nhỏ hơn 0,2M
Trong các dung dịch trên thì dung dịch BaCl2 là dung dịch dẫn điện tốt nhất.
Phương trình điện li viết đúng là
A sai do phân li ra Na+
B sai do C2H5OH không điện li
C sai do phản ứng hai chiều
D đúng
Các chất dẫn điện là:
Chất dẫn điện là: KCl nóng chảy, dung dịch NaOH
Cho các chất sau: C2H5OH, C12H22O11, C2H5COOH, C2H5NH3Cl, H3PO4, NaClO, BaSO4, Fe(OH)3. Số chất điện li yếu là
Các chất điện li yếu là: C2H5COOH, H3PO4, Fe(OH)3 ⟹ có 3 chất
Cho các nhận định sau:
(a) Sự điện li của chất điện li yếu là thuận nghịch.
(b) Chỉ có hợp chất ion mới có thể điện li được trong nước.
(c) Chất điện li phân li thành ion khi tan vào nước hoặc tại trạng thái nóng chảy.
(d) Nước là dung môi phân cực, có vai trò quan trọng trong quá trình điện li.
Số nhận định đúng là:
Các nhận định đúng là: a, c, d
Trong dung dịch axit axetic (bỏ qua sự phân li của H2O) có những phần tử nào?
Phương trình phân li của CH3COOH: CH3COOH 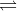 CH3COO- + H+
CH3COO- + H+
Vậy dung dịch CH3COOH nếu bỏ qua sự phân li của nước gồm có:
CH3COOH, H+, CH3COO-, H2O.

