Khử hoàn toàn 32 gam CuO bằng khí CO dư, thu được m gam kim loại. Giá trị của m là
nCuO = 32 : 80 = 0,4 (mol)
PTHH: CuO + CO \(\buildrel {{t^0}} \over\longrightarrow \) Cu + CO2
0,4 → 0,4 (mol)
=> mCu = 0,4.64 = 25,6 (g)
Cho 3,36 lít khí CO (đktc) phản ứng vừa đủ với 20 gam hỗn hợp X gồm CuO và MgO. Phần trăm khối lượng của MgO trong X là
nCO(đktc) = 3,36 :22,4 = 0,15 (mol)
Khi cho CO qua hỗn hợp CuO và MgO chỉ có CuO phản ứng
CO + CuO \(\xrightarrow{{{t^0}}}\) Cu + H2O
0,15 → 0,15 (mol)
nCuO = 0,15 (mol) => mCuO = 0,15.80 = 12 (g)
%CuO = (mCuO : mhh).100% = (12 : 20).100% = 60%
=> %MgO = 100% -%CuO = 40%.
Dẫn khí CO dư qua ống sứ đựng 8 gam bột CuO nung nóng, thu được hỗn hơp khí X, Cho toàn bộ khí X vào nước vôi trong dư, thu được m gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
Ta có nCuO = 0,1 mol
PTHH : CO + CuO → Cu + CO2
CO2 + Ca(OH)2 → CaCO3 + H2O
→ nCaCO3 = nCuO = 0,1 mol → mCaCO3 = 0,1 .100 =10 g
Cho luồng khí CO dư qua ống sứ đựng 5,36 gam hỗn hợp FeO và Fe2O3 (nung nóng), sau một thời gian thu được m gam chất rắn và hỗn hợp khí X. Dẫn X vào dung dịch Ca(OH)2 dư, thu được 9 gam kết tủa.Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
CO + (FeO và Fe2O3) → CO2 + Fe
=> Hỗn hợp khí X thu được là CO2 và CO dư.
Cho hh X này vào Ca(OH)2 dư chỉ có CO2 pư
CO2 + Ca(OH)2 → CaCO3↓ + H2O
=> nCO2 = nCaCO3 = 9 : 100 = 0,09 (mol)
Ta có: nO(oxit) = nCO2 = 0,09 (mol) => mO(oxit) = 0,09.16 = 1,44 (g)
=> m = mFe = 5,36 - 1,62 = 3,92 (g)
Cho 4,48 lít khí CO đktc phản ứng với 8 gam một oxit kim loại, sau phản ứng hoàn toàn, thu được m gam kim loại và hỗn hợp khí có tỉ khối so với H2 là 20. Giá trị của m là
CO + oxit → kim loại + CO2
Trong hỗn hợp khí sau phản ứng đặt nCO = x mol và nCO2 =y mol
Bảo toàn C có x + y = 0,2 mol
Tỉ khối hỗn hợp khí so với H2 là 20 nên =40
→ x = 0,05 mol và y =0,15 mol
Bảo toàn khối lượng có mCO + moxit = m + mkhí → 0,2.28 + 8 = m + 0,05.28 + 0,15.44 → m =5,6g
Dẫn khí CO dư qua ống sứ đựng 8 gam bột CuO nung nóng, thu được hỗn hợp khí X. Cho toàn bộ X vào nước vôi trong dư, thu được m gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
nCuO = 8 : 80 = 0,1 (mol)
CO + CuO \(\xrightarrow{{{t^0}}}\) Cu + CO2
0,1 → 0,1 (mol)
Hỗn hợp khí X có CO2 và CO dư, khi cho qua dung dịch nước vôi trong dư chỉ có CO2 tham gia phản ứng
CO2 + Ca(OH)2 → CaCO3↓ + H2O
0,1 → 0,1 (mol)
=> mkết tủa = mCaCO3 = 0,1.100 = 10 (g)
Khử hoàn toàn 1 lượng Fe3O4 bằng H2 dư thu được chất rắn X và m gam H2O. Hòa tan hết X trong dung dịch HCl dư thu được 1,008 lít khí H2 (đktc). Giá trị của m là:
(1) Fe3O4 + 4H2 \(\buildrel {{t^0}} \over\longrightarrow \) 3Fe + 4H2O
(2) Fe + 2HCl → FeCl2 + H2
Từ PTHH (2) => nH2 = nFe = 0,045 mol
Từ PTHH (1) => nH2O = 4/3.nFe = 0,06 mol
=> m = mH2O = 0,06.18 = 1,08g
Dẫn luồng khí CO dư qua hỗn hợp Al2O3; CuO; MgO; Fe2O3 nung nóng. Sau khi các phản ứng xảy ra hoàn toàn thu được chất rắn là
CO khử được các oxit CuO, Fe2O3 nên sau phản ứng thu được chất rắn là: Al2O3, Cu, MgO, Fe.
Dẫn luồng khí CO qua hỗn hợp Al2O3, CuO, MgO, Fe2O3 đun nóng, sau khi phản ứng xảy ra hoàn toàn thu được chất rắn là:
- CuO và Fe2O3 bị CO khử ở nhiệt độ cao theo PTHH:
CuO + CO → Cu + CO2
Fe2O3 + 3CO → 2Fe + 3CO2
- Al2O3 và MgO không bị CO khử ở nhiệt độ cao.
Như vậy chất rắn thu được sau phản ứng gồm: Al2O3, Cu, MgO, Fe
Cho V lít đktc hỗn hợp khí gồm CO và H2 phản ứng với một lượng dư hỗn hợp rắn gồm CuO và Fe3O4 nung nóng. Sau khi các phản ứng xảy ra hoàn toàn, khối lượng hỗn hợp rắn giảm 0,32 gam. Giá trị của V là
Khối lượng rắn giảm chính là khối lượng oxi trong oxit => mO(oxit) = 0,32 (g)
=> nhh CO+ H2 = nO(oxit) = 0,32 : 16 = 0,02 (mol)
=> Vhh CO+H2 = 0,02.22,4 = 0,448 (l)
Cho hơi nước đi qua than nóng đỏ thu được 78,4 lít hỗn hợp khí X (đktc) gồm khí CO, CO2, H2. Khử hết 1/2 hỗn hợp X bằng CuO dư nung nóng được chất rắn Y. Hòa tan hoàn toàn Y trong dung dịch HNO3 loãng thu được 22,4 lít (đktc) khí NO (sản phẩm khử duy nhất của N+5). Phần trăm thể tích khí CO trong X là
nX = 3,5 mol → n1/2 X = 1,75 mol
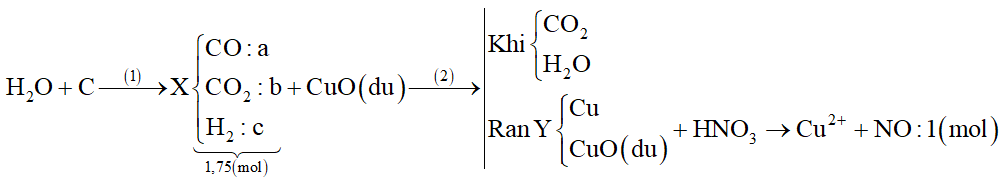
+) n1/2 X = a + b + c = 1,75 (1)
+) Áp dụng bảo toàn e cho quá trình (1): 2nCO + 4nCO2 = 2nH2 → 2a + 4b = 2c (2)
+) Áp dụng bảo toàn e cho quá trình (2): 2nCO + 2nH2 = 3nNO → 2a + 2c = 3.1 (3)
Giải (1) (2) (3) được a = 0,5; b = 0,25; c = 1
→ %VCO = (0,5/1,75).100% = 28,57%
Khử hoàn toàn hỗn hợp gồm m gam FeO, Fe2O3, Fe3O4 bằng CO dư ở nhiệt độ cao. Sau phản ứng thu được 33,6 g chất rắn. Dẫn hỗn hợp khí sau phản ứng vào dung dịch Ca(OH)2 dư thu được 80g kết tủa . Giá trị của m là :
Tổng quát: Gọi công thức oxit là FexOy
FexOy + yCO → xFe + yCO2
CO2 + Ca(OH)2 → CaCO3 + H2O
Ta có : nCaCO3 = 80 : 100 = 0,8 mol = nCO2 = nO( Oxit pứ)
Bảo toàn khối lượng : mOxit = mrắn + mO pứ = 33,6 + 16.0,8 = 46,4g
Khử hoàn toàn 4 gam hỗn hợp gồm CuO và PbO bằng khí CO dư ở nhiệt độ cao. Khí sinh ra được dẫn vào bình đựng nước vôi trong dư thu được 10 gam kết tủa. Khối lượng Cu và Pb thu được là:
Ta có: (1) CO + O → CO2
(2) CO2 + Ca(OH)2 → CaCO3 + H2O
Theo (2): nCO2 = nCaCO3 = 0,1 mol
Theo (1): nO = nCO2 = 0,1 mol
Bảo toàn khối lượng có: mkim loại = moxit - mO = 4 - 0,1.16 = 2,4 gam
Dẫn a mol hỗn hợp X (gồm hơi nước và khí CO2) qua cacbon nung đỏ, thu được 1,75a mol hỗn hợp Y gồm CO, H2 và CO2. Cho Y hấp thụ vào dung dịch Ca(OH)2 dư, sau khi phản ứng xảy ra hoàn toàn thu được 0,75 gam kết tủa. Giá trị của a là
nC phản ứng = nY - nX = 0,75a (BTC)
Bảo toàn electron: 4nC phản ứng = 2nCO + 2nH2 => nCO + nH2 = 1,5a
=> nCO2(Y) = nY - (nCO + nH2) = 0,25a
Ca(OH)2 dư nên nCO2 (Y) = nCaCO3 = 0,0075
=> 0,25a = 0,0075 => a = 0,03
Dẫn 0,02 mol hỗn hợp X (gồm hơi nước và khí CO2) qua cacbon nung đỏ, thu được 0,035 mol hỗn hợp Y gồm CO, H2 và CO2. Cho Y đi qua ống đựng 10 gam hỗn hợp gồm Fe2O3 và CuO (dư, nung nóng), sau khi các phản ứng xảy ra hoàn toàn, thu được m gam chất rắn. Giá trị của m là
\(0,02(mol)X\left\{ \matrix{
{H_2}O \hfill \cr
C{O_2} \hfill \cr} \right.\buildrel { + C} \over
\longrightarrow 0,035(mol)Y\left\{ \matrix{
CO \hfill \cr
{H_2} \hfill \cr
C{O_2} \hfill \cr} \right. + 10(g)\left\{ \matrix{
F{e_2}{O_3} \hfill \cr
CuO \hfill \cr} \right. \to m(g)\,chat\,ran = ?\)
Nhận thấy, C là nguyên nhân làm cho số mol hỗn hợp khí tăng lên => nC = 0,035 - 0,02 = 0,015 mol
Sau khi cho Y tác dụng với Fe2O3, CuO dư tạo thành H2O, CO2 nên ta có thể coi hỗn hợp Y gồm {H2O, CO2, C} như vậy ta thấy chỉ có C có phản ứng: C + 2O → CO2
=> nO(pư) = 2nC = 0,03 mol
=> m chất rắn = mFe2O3, CuO - mO(pư) = 10 - 0,03.16 = 9,52 gam
Cho 3,36 lít khí CO (đktc) phản ứng vừa đủ với 20 gam hỗn hợp X gồm CuO và MgO. Phần trăm khối lượng của MgO trong X là
nCO(đktc) = 3,36 :22,4 = 0,15 (mol)
Khi cho CO qua hỗn hợp CuO và MgO chỉ có CuO phản ứng
CO + CuO \(\buildrel {{t^0}} \over\longrightarrow \) Cu + H2O
0,15 → 0,15 (mol)
nCuO = 0,15 (mol) => mCuO = 0,15.80 = 12 (g)
%CuO = (mCuO : mhh).100% = (12 : 20).100% = 60%
=> %MgO = 100% -%CuO = 40%.
Khử hoàn toàn 14 gam hỗn hợp X gồm CuO và một oxit sắt bằng CO thu được 10,32 gam hỗn hợp Y gồm 2 kim loại. Thể tích CO (đktc) đã dùng cho quá trình trên là:
Oxit + CO → KL + CO2
Đặt nCO = nCO2 = x mol
BTKL: m oxit + mCO = mKL + mCO2
→ 14 + 28x = 10,32 + 44x
→ x = 0,23 mol
→ VCO = 0,23.22,4 = 5,152 lít
Trộn 20 gam bột CuO và một lượng C rồi đem nung nóng, sau một thời gian phản ứng thấy có 3,36 lít khí thoát ra khỏi bình. Khối lượng chất rắn thu được là
CuO + C $\xrightarrow{{{t}^{o}}}$ Cu + CO
nCO = 3,36 / 22,4 = 0,15 mol => nCuO phản ứng = 0,15 mol
=> mCuO dư = 20 – 0,15.80 = 8 gam
nCu tạo thành = nCuO phản ứng = 0,15 mol => mCu = 0,15.64 = 9,6 gam
=> mchất rắn sau phản ứng = 8 + 9,6 = 17,6 gam
Cho luồng khí CO dư đi qua 9,1 gam hỗn hợp CuO và Al2O3, nung nóng đến khi phản ứng hoàn toàn thu được 8,3 gam chất rắn. Khối lượng CuO có trong hỗn hợp ban đầu là
Al2O3 không bị khử bởi CO
CO + CuO $\xrightarrow{{{t}^{o}}}$ Cu + CO2
x mol → x mol
=> mCuO – mCu = 9,1 – 8,3 = 0,8 => 80x – 64x = 0,8 => x = 0,05 mol
=> mCuO = 80.0,05 = 4 gam
Cho khí CO dư qua 18 gam oxit kim loại M thu được 14 gam kim loại. Công thức của oxit là
Bảo toàn khối lượng: moxit = mO + mkim loại => mO = 18 – 14 = 4 gam
=> nO trong oxit = 4 / 16 = 0,25 mol
Moxit = 18 : 0,25 = 72 g/mol (FeO)

