Khi tách nước từ một chất X có công thức phân tử C4H10O tạo thành 3 anken là đồng phân của nhau (tính cả đồng phân hình học). Công thức cấu tạo thu gọn của X là :
Loại dần đáp án không phù hợp; Loại B và C vì B, C không bị tách nước
Loại D do D chỉ có một hướng tách nên không thể tạo ra 3 anken
A đúng vì CH3CH(OH)CH2CH3 có 2 hướng tách và tạo đồng phân hình học
Khi thực hiện phản ứng tách nước đối với ancol X, chỉ thu được 1 anken duy nhất. Oxi hoá hoàn toàn một lượng chất X thu được 5,6 lít CO2 (đktc) và 5,4 gam H2O. Có bao nhiêu công thức cấu tạo phù hợp với X?
X bị tách nước tạo 1 anken => X là ancol no, đơn chức và chỉ có 1 hướng tách
Công thức phân tử của X là CnH2n+1OH ;
Có nancol = nH2O – nCO2 = $\frac{{5,4}}{{18}} - \frac{{5,6}}{{22,4}} = {\text{ }}0,05{\text{ }}mol$
Và n = $\frac{{0,25}}{{0,05}}$= 5 . Nên công thức phân tử của X là C5H11OH
Công thức cấu tạo của X là
CH3 – CH2 – CH2 – CH2 – CH2OH ; CH3 – CH(CH3) – CH2 – CH2OH
CH3 – CH2 – CH(CH3) – CH2OH .
Tách nước hoàn toàn từ hỗn hợp X gồm 2 ancol A, B ta được hỗn hợp Y gồm các olefin. Nếu đốt cháy hoàn toàn hỗn hợp X thì thu được 1,76 g CO2. Khi đốt cháy hoàn toàn Y thì tổng khối lượng nước và CO2 tạo ra là
Áp dụng định luật bảo toàn nguyên tố cacbon ta có
Lượng CO2 thu được khi đốt cháy Y bằng khi đốt cháy X = $\frac{{1,76}}{{44}}$ = 0,04 mol
Mà Y là hỗn hợp các olefin nên số mol H2O = số mol CO2 = 0,04 mol
Vậy tổng khối lượng CO2 và H2O thu được là : 0,04 . 18 + 1,76 = 2,48 g
Cho các ancol sau :
(1) CH3CH2OH (2) CH3CHOHCH3
(3) CH3CH2CH(OH)CH2CH3 (4) CH3CH(OH)C(CH3)3
Dãy gồm các ancol khi tách nước từ mỗi ancol chỉ cho 1 olefin duy nhất là
Các ancol khi tách nước từ mỗi ancol chỉ cho 1 olefin duy nhất là (1) CH3CH2OH; (2) CH3CHOHCH3; (4) CH3CH(OH)C(CH3)3
Cho dãy chuyển hoá sau : CH3CH2CH2OH $\xrightarrow{{{H}_{2}}S{{O}_{4}}đặc,{{t}^{o}}}$ X $\xrightarrow{+{{H}_{2}}\text{O},\,\,{{H}_{2}}S{{O}_{4}},loãng}$ Y
Biết X, Y là sản phẩm chính. Vậy công thức cấu tạo của X và Y lần lượt là
+ Nhóm - OH ưu tiên tách cùng H ở nguyên tử C bậc cao hơn bên cạnh để thành liên kết đôi $\mathrm{C}=\mathrm{C}$.
+ Khi cộng $\mathrm{H}-\mathrm{OH}$ vào $\mathrm{C}=\mathrm{C}, \mathrm{H}$ ưu tiên cộng vào $\mathrm{C}$ mang nhiều $\mathrm{H}$ hơn.
$\mathrm{CH}_{3} \mathrm{CH}_{2} \mathrm{CH}_{2} \mathrm{OH} \underset{170^{\circ} \mathrm{C}}{\stackrel{\mathrm{H}_{2} \mathrm{SO}_{4} d}{\longrightarrow}} \mathrm{CH}_{3} \mathrm{CH}=\mathrm{CH}_{2}+\mathrm{H}_{2} \mathrm{O} \\
\mathrm{CH}_{3} \mathrm{CH}=\mathrm{CH}_{2}+\mathrm{H}-\mathrm{OH} \stackrel{\mathrm{H}_{2} \mathrm{SO}_{4} \text { loang }}{\longrightarrow} \mathrm{CH}_{3} \mathrm{CH}(\mathrm{OH}) \mathrm{CH}_{3}$
Cho sơ đồ chuyển hoá sau :
Butan – 2 – ol $\xrightarrow{{{H_2}S{O_4}\,\,đặc,\,\,{180^oC}}}$ X $\xrightarrow{{HBr}}$ Y $\xrightarrow{{Mg,\,\,ete\,\,khan}}$ Z
Trong đó X, Y, Z là sản phẩm chính. Công thức của Z là
CH3-CH(OH)-CH2-CH3 $\xrightarrow{{{H_2}S{O_4}\,\,đặc,\,\,{180^oC}}}$ CH3-CH=CH-CH3 $\xrightarrow{{HBr}}$ CH3-CHBr-CH2-CH3 $\xrightarrow{{Mg,\,\,ete\,\,khan}}$ CH3-CH(MgBr)-CH2-CH3
Đun nóng hỗn hợp gồm 2 ancol đơn chức, mạch hở, kế tiếp nhau trong dãy đồng đẳng với H2SO4 đặc ở 140oC. Sau khi các phản ứng kết thúc, thu được 6 gam hỗn hợp 3 ete và 1,8 gam nước. Công thức phân tử của 2 ancol trên là
Ta có nancol = 2nnước = 2. $\frac{{1,8}}{{18}}$= 0,2 mol
Áp dụng định luật bảo toàn khối lượng có : mancol = mete + mnước = 6 + 1,8 = 7,8 gam
Gọi công thức chung của 2 ancol $\overline R OH$ . Suy ra ${\overline M _{ancol}} = \frac{{7,8}}{{0,2}} = 39\,\, = > \,\,\overline R = 39{\text{ }}-{\text{ }}17{\text{ }} = {\text{ }}22$
Mà 2 ancol là đồng đẳng liên tiếp nên 2 ancol phải là CH3OH và C2H5OH
Đun 132,8 gam hỗn hợp 3 ancol no, đơn chức với H2SO4 đặc, 140oC thu được hỗn hợp các ete có số mol bằng nhau và có khối lượng là 111,2 gam. Số mol của mỗi ete trong hỗn hợp là
Áp dụng định luật bảo toàn khối lượng ta có
mnước = mancol – mete = 132,8 – 111,2 = 21,6 gam; nnước = $\frac{{21,6}}{{18}}$ = 1,2 mol
Mặt khác nete = nnước = 1,2 mol
3 ancol tách nước thu được 6 ete và các ete có số mol bằng nhau
Vậy số mol mỗi ete là : = 0,2 mol.
Đun 2 ancol đơn chức với H2SO4 đặc ở 140oC thu được hỗn hợp 3 ete. Lấy 0,72 gam một trong 3 ete đem đốt cháy hoàn toàn thu được 1,76 gam CO2 và 0,72 gam nước. Hai ancol đó là
Vì ancol đơn chức tách nước cũng thu được ete đơn chức mà ete cháy cho số mol CO2 = số mol H2O nên công thức phân tử của ete là CnH2nO
Ta có sơ đồ CnH2nO $\xrightarrow{{{t^o}}}$ nCO2
$\frac{{0,04}}{n}$ 0,04 mol
Khối lượng ete là : $\frac{{0,04}}{n}$. (14n + 16) = 0,72 => n = 4
Vậy công thức phân tử của ete là C4H8O => Công thức phân tử của 2 ancol phải là CH3OH và CH2 = CH – CH2OH.
Cho V lít (đktc) hỗn hợp khí gồm 2 olefin liên tiếp nhau trong dãy đồng đẳng hợp nước (xúc tác H2SO4 đặc), thu được 12,9 gam hỗn hợp A gồm 3 ancol. Đun nóng hỗn hợp A trong H2SO4 đặc ở 140oC thu được 10,65 gam hỗn hợp B gồm 6 ete khan. Công thức phân tử của 2 anken là
Áp dụng định luật bảo toàn khối lượng ta có
mnước = mancol – mete = 12,9 – 10,65 = 2,25 gam; nnước = $\frac{{2,25}}{{18}}$ = 0,125 mol
Ta có nancol = 2nnước = 2. 0,125= 0,25 mol. Gọi công thức chung của 2 ancol là $\overline R OH$
Suy ra ${\overline M _{ancol}} = \frac{{12,9}}{{0,25}} = 51,6\,\, = > \,\,\overline R = 51,6{\text{ }}-{\text{ }}17{\text{ }} = {\text{ }}34,6$
Mà 2 anken là đồng đẳng liên tiếp nên 3 ancol có 2 ancol là đồng phân của nhau và cũng là các ancol đồng đẳng liên tiếp. Nên 3 ancol là C2H5OH và C3H7OH 2 anken là C2H4 và C3H6.
Đun 2 ancol no đơn chức với H2SO4 đặc ở 140oC thu được hỗn hợp 3 ete. Lấy một trong 3 ete đem đốt cháy hoàn toàn thu được 1,32 gam CO2 và 0,72 gam nước. Hai ancol đó là
Vì ancol đơn chức tách nước cũng thu được ete đơn chức mà ete cháy cho số mol CO2 < số mol H2O nên công thức phân tử của ete là CnH2n+2O
Ta có : nete = 0,04 – 0,03 = 0,01 mol => n =$\frac{{0,03}}{{0,01}}$ = 3
Vậy công thức phân tử của ete là C3H8O => Công thức phân tử của 2 ancol phải là CH3OH và CH3 – CH2OH.
Đốt cháy hoàn toàn một lượng hỗn hợp X gồm 3 ancol thuộc cùng dãy đồng đẳng thu được 6,72 lít CO2 (đktc) và 9,90 gam nước. Nếu đun nóng cũng lượng hỗn hợp X như trên với H2SO4 đặc ở nhiệt độ thích hợp để chuyển hết thành ete thì tổng khối lượng ete thu được là
+) Ta có nancol = $\frac{{9,9}}{{18}} - \frac{{6,72}}{{22,4}} = {\text{ }}0,25{\text{ }}mol$
Số nguyên tử $\overline C = \frac{{0,3}}{{0,25}}$ = 1,2 suy ra 3 ancol là no đơn chức ${C_{\bar n}}{H_{2\bar n + 1}}OH$
Nên khối lượng 3 ancol là : m3 ancol = $0,25.(14\overline n + {\text{ }}18) = 0,25{\text{ }}.\left( {14.1,2 + 18} \right) = 8,7{\text{ }}gam$
Mặt khác khi tách nước thì nnước = $\frac{1}{2}{n_{ancol}} = \frac{1}{2}.{\text{ }}0,25 = 0,125{\text{ }}mol$
Áp dụng định luật bảo toàn khối lượng có :
mancol = mete + mnước => mete = 8,7 – 0,125 . 18 = 6,45 g
Đun nóng một ancol đơn chức X với dung dịch H2SO4 đặc trong điều kiện thích hợp sinh ra chất hữu cơ Y, tỉ khối của X so với Y là 1,6428. Công thức phân tử của Y là
Vì dY/ X = $\frac{1}{{1,6428}}$< 1 nên Y là anken
Ta có sơ đồ CnH2n+1OH $\xrightarrow{{{H_2}S{O_4}\,\,đặc,\,\,{t^o}}}$ CnH2n
dY/ X = $\frac{{14n}}{{14n + 18}} = \frac{1}{{1,6428}}$ => n = 2. Vậy công thức phân tử của X là C2H6O.
Đun ancol X no đơn chức với H2SO4 đặc thu được hợp chất hữu cơ Y có dY/ X = 0,7. Công thức phân tử của X là
Vì dY/ X = 0,7 < 1 nên Y là anken
Ta có sơ đồ CnH2n+1OH $\xrightarrow{{{H_2}S{O_4}\,\,đặc,\,\,{t^o}}}$ CnH2n
dY/ X = $\frac{{14n}}{{14n + 18}} = 0,7$=> n = 3. Vậy công thức phân tử của X là C3H8O.
Đun ancol X đơn chức với H2SO4 đặc thu được hợp chất hữu cơ Y có dY/ X = 1,75. Công thức phân tử của X là
Vì dY/ X = 1,75 > 1 nên Y là ete
Ta có sơ đồ : 2ROH $\xrightarrow{{{H_2}S{O_4}\,\,đặc,\,\,{t^o}}}$ ROR
dY/ X = $\frac{{2R + 16}}{{R + 17}}$ = 1,75 => R = 55 (C4H7). Vậy công thức phân tử của X là C4H7OH
Đun ancol X no đơn chức với H2SO4 đặc thu được hợp chất hữu cơ Y có dY/ X = 1,7. Công thức phân tử của X là
Vì dY/ X = 1,7 > 1 nên Y là ete
Ta có sơ đồ 2ROH $\xrightarrow{{{H_2}S{O_4}\,\,đặc,\,\,{t^o}}}$ ROR
dY/ X = $\frac{{2R + 16}}{{R + 17}}$= 1,7 R = 43 (C3H7)
Một hh gồm C2H5OH và ankanol X mạch không phân nhánh. Đốt cháy cùng số mol mỗi ancol thì lượng H2O sinh ra từ ancol này bằng 5/3 lượng H2O sinh ra từ ancol kia. Nếu đun nóng hh trên với H2SO4 đặc ở 1700C thì chỉ thu được 2 anken. X có CTCT nào sau đây:
Theo bài ra X tạo 1 anken => X tách nước tạo anken không có đphh và MX > MC2H5OH
=> $\frac{{n + 1}}{3} = \frac{5}{3}$ => n = 4
=> X là CH3CH2CH2CH2OH
Chia hỗn hợp gồm hai rượu đơn chức X và Y (phân tử khối của X nhỏ hơn của Y) là đồng đẳng kế tiếp thành hai phần bằng nhau:
- Đốt cháy hoàn toàn phần 1 thu được 5,6 lít CO2 (đktc) và 6,3 gam H2O.
- Đun nóng phần 2 với H2SO4 đặc ở 1400C tạo thành 1,25 gam hỗn hợp ba ete. Hóa hơi hoàn toàn hỗn hợp ba ete trên, thu được thể tích bằng thể tích của 0,42 gam N2 (trong cùng điều kiện nhiệt độ, áp suất).
Hiệu suất của phản ứng tạo ete của X, Y lần lượt là:
nCO2 = 0,25 ; nH2O = 0,35 ; nN2 = 0,015 = nete
Ta thấy nH2O > nCO2 → rượu no, đơn →nrượu = 0,35 – 0,25 = 0,1
→ C trung bình = nCO2 / nrượu =0,25/0,2 = 2,5
Vì 2 rượu liên tiếp → số mol 2 rượu bằng nhau và = 0,1/2 = 0,05
Trong pứ ete hóa thì số mol rượu = 2 lần số mol ete → số mol rượu tham gia pứ ete hóa = 0,015.2 = 0,03 → vậy tổng hiệu suất tạo ete của 2 rượu = 0,03/0,05 .100% = 60%
+ Giả sử chỉ C2H5OH tạo ete → mete thu được = 0,015.(2.46 - 18) = 1,11 gam
+ Giả sử chỉ C3H7OH tạo ete → mete thu được = 0,015.(2.60 – 18) = 1,53
Dựa vào khối lượng ete thu được thực tế và giả sử, áp dung quy tắc đường chéo tính được tỉ lệ C2H5OH/C3H7OH = 2/1 → hiệu suất tạo ete lần lượt của 2 rượu = 40% và 20%
Thực hiện thí nghiệm như hình vẽ bên. Khi đun nóng bình cầu ở nhiệt độ ≥ 170oC thì hiện tượng xảy ra trong ống nghiệm đựng dung dịch brom là
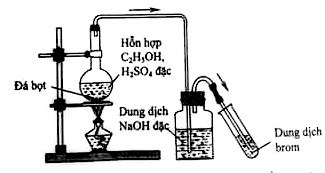
C2H5OH \(\xrightarrow{{{H_2}S{O_4}dac,{t^o} \geqslant {{170}^o}C}}\) C2H4 + H2O
C2H4 + Br2 → C2H4Br2
⟹ Hiện tượng: dung dịch brom bị nhạt màu.

