Hấp thụ toàn bộ 0,896 lít CO2 vào 3 lít dung dịch Ca(OH)2 0,01M thu được?
nCO2 = 0,896 : 22,4 = 0,04 mol; nOH- = 2nCa(OH)2 = 2.3.0,01 = 0,06 mol; nCa2+ = nCa(OH)2 = 0,03 mol
Ta có: \(1 < \dfrac{{{n_{O{H^ - }}}}}{{{n_{C{O_2}}}}} = \dfrac{{0,06}}{{0,04}} = 1,5 < 2\) => Tạo muối CO32- và HCO3-
Đặt n(CO3)2- = x (mol) và nHCO3- = y (mol)
CO2 + 2OH- → CO32- + H2O
x 2x x
CO2 + OH- → HCO3-
y y y
+ nCO2 = x + y = 0,04 (1)
+ nOH- = 2x + y = 0,06 (2)
Giải hệ (1) và (2) thu được x = 0,02 và y = 0,02
Ca2+ + CO32- → CaCO3↓
BĐ: 0,03 0,02 (mol)
PƯ: 0,02 ← 0,02 → 0,02 (mol)
Khối lượng kết tủa thu được là: mCaCO3 = 0,02.100 = 2 gam
Sục 0,15 mol khí CO2 vào 200 ml dung dịch Ba(OH)2 1M, sau khi kết thúc phản ứng, thu được m gam kết tủa. Giá trị m là
nBa(OH)2 = 0,2.1 = 0,2 (mol)
Ta có: 1 < nBa(OH)2/nCO2 = 0,15/0,2 = 0,75 < 1 nên chỉ xảy ra tạo muối BaCO3. CO2 pư hết, Ba(OH)2 dư. Mọi tính toán theo số mol của CO2
CO2 + Ba(OH)2 → BaCO3↓ + H2O
0,15 → 0,15 (mol)
→ mBaCO3 = 0,15.197 = 29,55 (g)
Sục V lít khí CO2 (đktc) vào 2 lít dung dịch Ca(OH)2 0,05M, thu được 7,5 gam kết tủa. Các phản ứng xảy ra hoàn toàn. Trị số của V là
TH1: Ca(OH)2 dư, CO2 phản ứng hết, kết tủa không bị hòa tan
CO2 + Ca(OH)2 → CaCO3 + H2O
BTNT “C” ta có: nCO2 = nCaCO3 = 0,075 mol
=> V CO2 = 0,075.22,4 = 1,68 lít
TH2: Kết tủa bị hòa tan một phần
CO2 + Ca(OH)2 → CaCO3 + H2O
CO2 + CaCO3 + H2O → Ca(HCO3)2
nCaCO3 = 0,075 mol
BTNT “Ca” ta có: nCa(HCO3)2 = nCa(OH)2 – nCaCO3 = 0,1 – 0,075 = 0,025 mol
BTNT “C”: nCO2 = nCaCO3 + 2nCa(HCO3)2 = 0,075 + 0,025.2 = 0,125 mol
=> VCO2 = 0,125.22,4 = 2,8 lít
Thổi 0,5 mol khí CO2 vào dung dịch chứa 0,4 mol Ba(OH)2. Sau phản ứng thu được a mol kết tủa. Giá trị của a là
nCO2 = 0,5 mol; nOH- = 2nBa(OH)2 = 0,8 mol
\(1 < \dfrac{{{n_{O{H^ - }}}}}{{{n_{C{O_2}}}}} = \dfrac{{0,8}}{{0,5}} = 1,6 < 2\) => tạo 2 muối CO32- (x mol) và HCO3- (y mol)
BTNT “C” => nCO2 =\({n_{CO_3^{2 - }}} + {n_{HCO_3^ - }}\)
=> x + y = 0,5 (1)
BTĐT: 2nBa2+ = \({2n_{CO_3^{2 - }}} + {n_{HCO_3^ - }}\)
=> 2x + y = 0,8 (2)
Giải (1) và (2) thu được x = 0,3 và y = 0,2
nBa2+ (0,4 mol) > \({n_{CO_3^{2 - }}}\) (0,3 mol) => CO32- hết, Ba2+ dư
=> nBaCO3 = \({n_{CO_3^{2 - }}}\) = 0,3 mol
Hấp thụ hoàn toàn 2,24 lít khí CO2 (đktc) vào dung dịch nước vôi trong có chứa 0,075 mol Ca(OH)2. Sản phẩm thu được sau phản ứng gồm:
nOH- = 2nCa(OH)2 = 0,075.2 = 0,15 mol
nCO2 = 2,24 : 22,4 = 0,1 mol
Xét tỉ lệ: \(\frac{{{n_{O{H^ - }}}}}{{{n_{C{O_2}}}}}\,{\mkern 1mu} = \,{\mkern 1mu} \frac{{0.15}}{{0.1}}{\mkern 1mu} \, = {\mkern 1mu} \,1,5{\mkern 1mu}\)
\(\Rightarrow \,1 < \frac{{{n_{O{H^ - }}}}}{{{n_{C{O_2}}}}} < 2\)
=> Tạo 2 muối là CaCO3 và Ca(HCO3)2
Thổi 0,5 mol khí CO2 vào dung dịch chứa 0,4 mol Ba(OH)2. Sau phản ứng thu được a mol kết tủa. Giá trị của a là
\({n_{C{O_2}}} = 0,5mol\);\({n_{O{H^ - }}} = 2\times{n_{Ba{{(OH)}_2}}} = 0,8mol\)
\(1 < \dfrac{{{n_{O{H^ - }}}}}{{{n_{C{O_2}}}}} = \dfrac{{0,8}}{{0,5}} = 1,6 < 2\) => tạo 2 muối CO32- (x mol) và HCO3- (y mol)
BTNT “C” => \({{\text{n}}_{{\text{CO}}_{\text{2}}^{}}}{\text{ = }}{{\text{n}}_{{\text{CO}}_{\text{3}}^{{\text{2 - }}}}}{\text{ + }}{{\text{n}}_{{\text{HCO}}_{\text{3}}^{\text{ - }}}}\) => x + y = 0,5 (1)
BTĐT: \(2{{\text{n}}_{{\text{B}}{{\text{a}}^{{\text{2 + }}}}}}{\text{ = 2}}{{\text{n}}_{{\text{CO}}_{\text{3}}^{{\text{2 - }}}}}{\text{ + }}{{\text{n}}_{{\text{HCO}}_{\text{3}}^{\text{ - }}}}\)=> 2x + y = 0,8 (2)
Giải (1) và (2) thu được x = 0,3 và y = 0,2
\({{\text{n}}_{{\text{B}}{{\text{a}}^{{\text{2 + }}}}}}{\text{(0,4 mol) > }}{{\text{n}}_{{\text{CO}}_{\text{3}}^{{\text{2 - }}}}}{\text{ (0,3 mol)}}\) => \({\text{CO}}_{\text{3}}^{{\text{2 - }}}\) hết, Ba2+ dư
=> \({{\text{n}}_{{\text{BaCO}}_{\text{3}}^{}}}{\text{ = }}{{\text{n}}_{{\text{CO}}_{\text{3}}^{{\text{2 - }}}}}{\text{ = 0,3 mol}}\)
Khi sục từ từ đến dư khí CO2 vào dung dịch hỗn hợp chứa a mol Ca(OH)2 và b mol NaOH. Kết quả thí nghiệm được biểu diễn trên đồ thị sau:
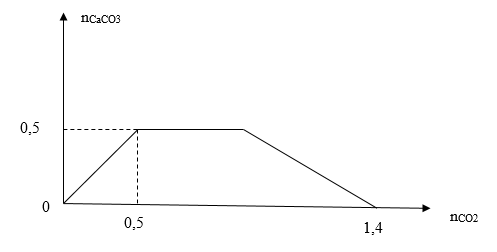
Tỉ lệ a: b là
+ Tại giai đoạn 1: đồ thị đi lên do xảy ra phản ứng:
CO2 + Ca(OH)2 → CaCO3↓ + H2O
→ nCaCO3 max = 0,5 (mol).
BTNT "Ca": nCa(OH)2 bđ = 0,5 (mol) = a
+ Tại giai đoạn 3: đồ thị đi xuống khi hòa tan hoàn toàn kết tủa
→ Muối thu được gồm: NaHCO3 và Ca(HCO3)2
BTNT "Ca": nCa(HCO3)2 = nCa(OH)2 = 0,5 (mol)
BTNT "C": nCO2 = nNaHCO3 + 2nCa(HCO3)2
→ 1,4 = b + 2.0,5 → b = 0,4 (mol)
Vậy a : b = 0,5 : 0,4 = 5 : 4
Hấp thụ hoàn toàn 0,4 mol CO2 vào dung dịch Ba(OH)2 lấy dư. Khối lượng kết tủa tạo ra có giá trị là:
CO2 + Ba(OH)2 → BaCO3↓ + H2O
0,4 → 0,4 (mol)
=> mBaCO3 = 0,4.197 = 78,8 (g)
Hỗn hợp X gồm Na, Ba, Na2O và BaO. Hòa tan hoàn toàn 21,9 gam X vào nước thu được 1,12 lít khí H2 và dung dịch Y có chứa 20,52 gam Ba(OH)2. Hấp thụ hoàn toàn 6,72 lít khí CO2 vào Y thu được m gam kết tủa. Biết thể tích các khí đo ở đktc. Giá trị gần nhất của m là
nBa(OH)2 = 20,52 : 171 = 0,12 mol; nH2 = 1,12 : 22,4 = 0,05 mol
Quy đổi hỗn hợp thành: Na (x mol); Ba (0,12 mol) và O (y mol)
+ mX = 23x + 137.0,12 + 16y = 21,9 (1)
+ BT electron: nNa + 2nBa = 2nO + 2nH2 => x + 2.0,12 = 2y + 2.0,05 (2)
Giải hệ (1) và (2) được x = y = 0,14 mol
Dung dịch Y gồm: Na+ (0,14 mol); Ba2+ (0,12 mol) và OH-
BTĐT => nOH- = nNa+ + 2nBa2+ = 0,14 + 2.0,12 = 0,38 mol
*Hấp thụ 0,3 mol CO2 vào dung dịch Y:
Tỉ lệ: 1 < nOH- : nCO2 = 0,38 : 0,3 = 1,27 < 2 => Tạo CO32- và HCO3-
CO2 + 2OH- → CO32- + H2O
a 2a a
CO2 + OH- → HCO3-
b b b
+ nCO2 = a + b = 0,3
+ nOH- = 2a + b = 0,38
Giải hệ được a = 0,08 và b = 0,22
So sánh thấy: \({n_{B{a^{2 + }}}} > {n_{CO_3^{2 - }}}\) nên Ba2+ dư so với CO32-
=> nBaCO3 = \({n_{CO_3^{2 - }}}\) = 0,08 mol => m kết tủa = 0,08.197 = 15,76 gam gần nhất với 15,5 gam
Hấp thụ hoàn toàn 3,36 lít khí CO2 (điều kiện tiêu chuẩn) vào dung dịch chứa 0,15 mol NaOH và 0,1 mol Ba(OH)2 thu được m gam kết tủa. Giá trị của m là
nOH- = nNaOH + 2nBa(OH)2 = 0,15 + 2.0,1 = 0,35 mol; nCO2 = 0,15 mol
\(\frac{{{n_{O{H^ - }}}}}{{{n_{C{O_2}}}}} = \frac{{0,35}}{{0,15}} = 2,33 > 2\) => OH- dư, chỉ tạo muối CO32-
*BTNT “C”: nCO3 2- = nCO2 = 0,15 mol
So sánh thấy: nBa2+ < nCO32- => Ba2+ hết, CO32- dư
=> nBaCO3 = nBa2+ = 0,1 mol
=> m BaCO3 = 0,1.197 = 19,7 gam
Hấp thụ hết 6,72 lít khí CO2 (đktc) vào 1,25 lít dung dịch Ba(OH)2 0,2M. Khối lượng kết tủa thu được là
nCO2 = 0,3 mol; nBa(OH)2 = 1,25.0,2 = 0,25 mol
=> nBa2+ = nBa(OH)2 = 0,25 mol; nOH- = 2nBa(OH)2 = 0,5 mol
Tỉ lệ: 1 < nOH- : nCO2 = 0,5 : 0,3 = 1,67 < 2 => Tạo muối CO32- và HCO3-
CO2 + 2OH- → CO32- + H2O
x 2x x
CO2 + OH- → HCO3-
y y y
nCO2 = x + y = 0,3
nOH- = 2x + y = 0,5
Giải hệ được x = 0,2; y = 0,1
So sánh: \({n_{B{a^{2 + }}}} > {n_{CO_3^{2 - }}}\) => Ba2+ dư so với CO32-
=> nBaCO3 = \({n_{CO_3^{2 - }}}\) = 0,2mol => m kết tủa = 0,2.197 = 39,4 gam
Sục V lít CO2(đkc) vào 100ml dung dịch Ca(OH)2 2M thu được 10 gam kết tủa.V có giá trị là:
TH1: Ca(OH)2 dư, kết tủa chưa bị hòa tan
BT “C”: nCO2 = nCaCO3 = 0,1 mol
=> VCO2 = 2,24 lít
TH2: Kết tủa bị hòa tan một phần
BT “Ca” => nCa(HCO3)2 = nCa(OH)2 – nCaCO3 = 0,2 – 0,1 = 0,1 mol
BT “C” => nCO2 = nCaCO3 + 2nCa(HCO3)2 = 0,1 + 2.0,1 = 0,3 mol
=> VCO2 = 6,72 lít
Cho 2,24 lít CO2 (đktc) vào 200 ml dung dịch Ca(OH)2 1M, khối lượng kết tủa thu được là
nOH- = 2nCa(OH)2 = 0,4 mol
nCO2 = 0,1 mol
Ta có nOH- /nCO2 = 4 => Ca(OH)2 dư, chỉ tạo muối trung hòa
nCaCO3 = nCO2 = 0,1 mol => mCaCO3 = 0,1.100 = 10 (g)
Hấp thụ hoàn toàn a mol khí CO2 vào dung dịch chứa b mol Ca(OH)2 thì thu được hỗn hợp 2 muối CaCO3 và Ca(HCO3)2. Quan hệ giữa a và b là
Sau phản ứng thu được 2 muối => nCO2 < nOH- < 2.nCO2 => a < 2b < 2a => b < a < 2b
Cho 5,6 lít CO2 (đktc) hấp thụ hoàn toàn trong dung dịch chứa 0,18 mol Ca(OH)2. Khối lượng kết tủa thu được là:
nCO2 = 0,25 mol; nOH- = 0,36 mol
Xét tỉ lệ: nOH- / nCO2 = 0,36 / 0,25 = 1,44 => sau phản ứng thu được 2 muối
Sử dụng công thức tính nhanh: \({n_{CO_3^{2 - }}} = {n_{O{H^ - }}} - {n_{C{O_2}}}\)= 0,36 – 0,25 = 0,11 mol
=> nCaCO3 = nCO3 = 0,11 mol => m = 11 gam
Cho 7,84 lít khí CO2 (đktc) tác dụng với 250 ml dung dịch KOH 2M sau phản ứng, cô cạn dung dịch thu được tổng khối lượng sản phẩm rắn là:
nKOH = 0,5 mol; nCO2 = 0,35 mol
Xét: nOH- / nCO2 = 0,5/0,35 = 10/7
=> Tạo 2 muối K2CO3 và KHCO3
Tuy nhiên khi cô cạn dung dịch thì muối KHCO3 bị nhiệt phân thành K2CO3
Bảo toàn K => nK2CO3 = 0,25 mol => m = 34,5g
Hấp thụ hết V (lít) khí CO2 (đktc) vào 200 ml dung dịch NaOH 1,5M. Cô cạn dung dịch sau phản ứng thu được 14,6 gam chất rắn khan. Giá trị của V là
nNaOH = 0,3 mol
TH1: Chất rắn chỉ gồm Na2CO3
Bảo toàn Na => nNa2CO3 = ½ nNaOH = 0,15 mol => m chất rắn = 15,9g > 14,6
TH2: Chất rắn gồm Na2CO3 (x mol) và NaOH (y mol)
=> mrắn khan = 106x + 40y = 14,6 (1)
Bảo toàn nguyên tố Na: nNaOH ban đầu = 2.nNa2CO3 + nNaOH dư => 2x + y = 0,3 (2)
Từ (1) và (2) => x = 0,1 và y = 0,1
Bảo toàn nguyên tố C: nCO2 = nNa2CO3 = 0,1 mol
TH3: Chất rắn gồm Na2CO3 (x mol) và NaHCO3 (y mol)
Bảo toàn nguyên tố Na: nNaOH ban đầu = 2.nNa2CO3 + nNaHCO3 => 2x + y = 0,3 (3)
mrắn khan = mNa2CO3 + mNaHCO3 => 106x + 84y = 14,6 (4)
Giả (3) và (4) ra nghiệm âm => loại trường hợp này
Thể tích CO2 (đktc) lớn nhất cần cho vào 2,0 lít dung dịch Ba(OH)2 0,1M để thu được 15,76 gam kết tủa là
nOH- = 0,4 mol; nBaCO3 = 0,08 mol
Thể tích khí CO2 cần dùng lớn nhất để thu được 15,76 gam kết tủa là khi tạo kết tủa tối đa sau đó hòa tan 1 phần
=> phản ứng thu được 2 muối BaCO3 và Ba(HCO3)2
Sử dụng công thức tính nhanh: nCO2 = nOH- - nBaCO3 = 0,4 – 0,08 = 0,32 mol
=> V = 7,168 lít
Cho 11,2 lít CO2 (đktc) hấp thụ hết trong dung dịch chứa a mol Ca(OH)2 và 0,2 mol NaOH. Xác định giá trị của a để sau phản ứng thu được 10 gam kết tủa:
nCO2 = 0,5 mol; nCaCO3 = 0,1 mol
TH1: thu được 1 muối CO32-
=> nCa2+ = nCaCO3 = 0,1 mol => a = 0,1
Kiểm tra lại:
nOH- = 2.nCa(OH)2 + nNaOH = 2.0,1 + 0,2 = 0,4 mol
Mà thu được muối CO32- thì nOH- \( \ge \) 2.nCO2 => 0,4\( \ge \) 2.0,5 (vô lí) => loại trường hợp này
TH2: thu được 2 muối HCO3- và CO32-
Sử dụng công thức tính nhanh: \({n_{CO_3^{2 - }}} = {n_{O{H^ - }}} - {n_{C{O_2}}}\)=> 2a + 0,2 – 0,5 = 0,1 => a = 0,2 mol
Sục khí CO2 vào 100 ml dung dịch X chứa đồng thời Ba(OH)2 0,5M và NaOH 0,8M. Xác định thể tích khí CO2 (đktc) để khi hấp thụ vào dung dịch X thu được kết tủa cực đại:
nOH- = 0,18 mol; nBa2+ = 0,05 mol
Xét tỉ lệ: nBa2+ = 0,05 mol < ½.nOH- => Kết tủa cực đại khi Ba2+ tạo hết thành kết tủa BaCO3
TH1: Thu được 1 muối CO32- => nCO2 = nCO32- = nBa2+ = 0,05 mol => V = 1,12 lít
TH2: Thu được 2 muối HCO3- và CO32-
=> nCO2 = nOH- - nCO32- = nOH- - nBa2+ = 0,18 – 0,05 = 0,13 mol => V = 2,912 lít

