Áp dụng quy tắc Mac-cốp-nhi-cốp vào trường hợp nào sau đây ?
Quy tắc Mac-côp-nhi-côp được dùng trong phản ứng cộng HX và anken bất đối xứng (xem ưu tiên X vào C nào…)
Khi cho but-1-en tác dụng với dung dịch HBr, theo qui tắc Mac-côp-nhi-côp sản phẩm nào sau đây là sản phẩm chính ?
But-1-en: CH2=CH–CH2–CH3
Quy tắc: Trong phản ứng cộng HX vào liên kết bội, nguyên tử H ưu tiên cộng vào nguyên tử Cacbon bậc thấp hơn, còn nguyên tử hay nhóm nguyên tử X ưu tiên cộng vào nguyên tử Cacbon bậc cao hơn.
=> cacbon số 1 bậc 2 còn cacbon số 2 bậc 3 => Br sẽ ưu tiên thế vào cacbon số 2
Anken hoạt động hóa học hơn ankan vì trong phân tử có chứa
Trong phân tử anken có chứa 1 liên kết đôi gồm 1 liên kết π và 1 liên kết σ.
Liên kết π kém bền hơn liên kết σ.
Theo quy tắc cộng Maccopnhicop, propen phản ứng với HCl, thu được sản phẩm chính là:
\({H_2}C = CH - C{H_3} + HCl \to {H_3}C - CHCl - C{H_3}\)
=> 2- clopropan
Số anken khí (ở nhiệt độ thường) khi tác dụng với HBr chỉ thu được một sản phẩm cộng duy nhất là
H2C=CH2 có 1 sản phẩm cộng
H2C=CH-CH3 có 2 sản phẩm cộng
H2C=CH-CH2-CH3 có 2 sản phẩm cộng
H3C-CH=CH-CH3 có 1 sản phẩm cộng
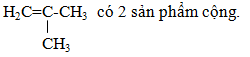
=> có 2 anken tác dụng với HBr chỉ thu 1 sản phẩm cộng.
Hiđro hóa hoàn toàn buta-1,3-đien, thu được:
\({H_2}C = CH - CH = C{H_2} + 2{H_2}\underrightarrow {{t^0},xt}{H_3}C - C{H_2} - C{H_2} - C{H_3}\)
Sản phẩm là butan.
Anken khi tác dụng với nước cho duy nhất một ancol là
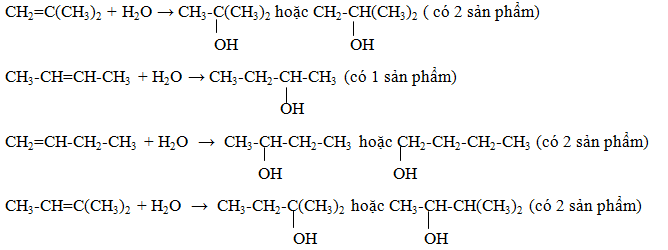
Hỗn hợp X gồm hai anken là chất khí ở điều kiện thường. Hiđrat hóa X thu được hỗn hợp Y gồm bốn ancol (không có ancol bậc III). Anken trong X là
CH2=CH2 + H2O → CH3-CH2-OH
CH2=CH-CH3 + H2O → CH2(OH)-CH2-CH3 hoặc CH3-CH(OH)-CH3
CH2=CH-CH2-CH3 + H2O → CH3-CH(OH)-CH2-CH3 hoặc CH2(OH)-CH2-CH2-CH3
CH3-CH=CH-CH3 + H2O → CH3-CH2-CH(OH)-CH3
=> hỗn hợp X gồm propilen và but-1-en thỏa mãn.
Để nhận biết 2 chất khí 1 ankan và 1 anken chỉ cần dùng một thuốc thử duy nhất. Thuốc thử đó không thể là
Anken có khả năng phản ứng với dung dịch Br2/CCl4 làm mất màu dung dịch.
Ankan không phản ứng với dung dịch Br2/CCl4.
Tiến hành trùng hợp 1 mol etilen ở điều kiện thích hợp, đem sản phẩm sau trùng hợp tác dụng với dung dịch brom dư thì lượng brom phản ứng là 36 gam. Hiệu suất phản ứng trùng hợp và khối lượng polietilen (PE) thu được là
\(n C{H_2} = C{H_2} \to {( - C{H_2} - C{H_2} - )_n}\)
\(C{H_2} = C{H_2} + B{r_2} \to C{H_2}Br - C{H_2}Br\)
=> \({n_{B{r_2}}} = {n_{{C_2}{H_4}du}} = \frac{{36}}{{160}} = 0,225mol\)
=> \({n_{{C_2}{H_4}pu}} = {n_{{C_2}{H_4}bd}} - {n_{{C_2}{H_4}du}}\)
\( = > {n_{{C_2}{H_4}pu}} = 1 - 0,225 = 0,775mol\)
\( = > H = \frac{{{n_{pu}}}}{{{n_{bd}}}}.100\% = \frac{{0,775}}{1}.100\% = 77,5\% \)
\({m_{PE}} = {m_{{C_2}{H_4}pu}} = 0,775.28 = 21,7g\)
Hidrocacbon X ở thể khí trong điều kiện thường. Cho X lội từ từ qua dung dịch Br2 dư thấy khối lượng bình đựng dung dịch Br2 tăng 2,6 gam và có 0,15 mol Br2 phản ứng. Tên gọi của X là ?
\(\begin{gathered}{n_{B{r_2}}} = {n_{lk\pi }} = {\text{ }}0,15{\text{ }}mol \hfill \\+ )\pi = 1 \hfill \\{n_X} = 0,15 = > {M_X} = \frac{{2,6}}{{0,15}} = 17,33 \hfill \\+ )\pi = 2 \hfill \\{n_X} = 0,075 = > {M_X} = \frac{{2,6}}{{0,075}} = 34,67 \hfill \\+ )\pi = 3 \hfill \\ {n_X} = 0,05 = > {M_X} = \frac{{2,6}}{{0,05}} = 52 \hfill \\ \end{gathered} \)
X là C4H4 có tên là vinyl axetilen.
Cho 4,48 lít hỗn hợp X gồm etan, propan và propen qua dung dịch brom dư, thấy khối lượng bình brom tăng 4,2 gam. Lượng khí còn lại thoát ra khỏi dung dịch đem đốt cháy hoàn toàn thu được 6,48 gam nước. Phần trăm thể tích các chất có trong hỗn hợp X lần lượt là
Khi cho hợp khí qua bình Brom chỉ có propen bị giữ lại
=> \({m_{B{r_2} \uparrow }} = {m_{propen}} = 4,2gam\)
\({n_{{C_3}{H_6}}} = \dfrac{{4,2}}{{42}} = 0,1mol\)
\(\% {V_{{C_3}{H_6}}} = \dfrac{{0,1}}{{0,2}}.100\% = 50\% \)
Gọi CTPT chung của etan và propan là \({C_{\overline n }}{H_{2\overline n + 2}}\)
\(\begin{gathered}{n_{{C_{\overline n }}{H_{2\overline n + 2}}}} = 0,1mol \hfill \\{C_{\overline n }}{H_{2\overline n + 2}} + {O_2} \to \overline n C{O_2} + (\overline n + 1){H_2}O \hfill \\{n_{{H_2}O}} = 0,1.(\overline n + 1) = 0,36 \hfill \\ \to \overline n = 2,6 \hfill \\\frac{{{n_{{C_2}{H_6}}}}}{{{n_{{C_3}{H_8}}}}} = \frac{{3 - 2,6}}{{2,6 - 2}} = \dfrac{2}{3} \hfill \\\to {n_{{C_2}{H_6}}} = \dfrac{{2.0,1}}{5} = 0,04mol \hfill \\\to {n_{{C_3}{H_8}}} = \dfrac{{3.0,1}}{5} = 0,06mol \hfill \\ \% {V_{{C_2}{H_6}}} = \dfrac{{0,04}}{{0,2}}.100\% = 20\% \hfill \\ \% {V_{{C_3}{H_8}}} = \frac{{0,06}}{{0,2}}.100\% = 30\% \hfill \\ \end{gathered} \)
Hiđrocacbon X cộng HCl theo tỉ lệ mol 1:1 tạo sản phẩm có hàm lượng clo là 55,04%. X có công thức phân tử là :
Gọi công thức phân tử của X là \({C_n}{H_{2n}}\)
=> công thức phân tử sản phẩm của X với HCl là \({C_n}{H_{2n + 1}}Cl\)
\(\frac{{35,5}}{{14n + 36,5}}.100\% = 55,04\% = > n \approx 2\)
Công thức phân tử của X là C2H4
Dẫn 3,36 lít (đktc) hỗn hợp X gồm 2 anken là đồng đẳng kế tiếp vào bình nước brom dư, thấy khối lượng bình tăng thêm 7,7 gam. Thành phần phần trăm về thể tích của hai anken là
Gọi công thức phân tử chung của anken là \({C_{\overline n }}{H_{2\overline n }}\)
\(\begin{gathered}{m_ \uparrow } = {m_X} = 7,7gam \hfill \\\overline M = \frac{{7,7}}{{0,15}} \approx 51,33 \hfill \\= > 14n = 51,33 = > n \approx 3,67 \hfill \\ \end{gathered} \)
Công thức của anken là C3H6 và C4H8
\(\begin{gathered} \frac{{{n_{{C_3}{H_6}}}}}{{{n_{{C_4}{H_8}}}}} = \frac{{3,67 - 3}}{{4 - 3,67}} = \frac{2}{1} \hfill \\ \% {V_{{C_3}{H_6}}} = \frac{2}{3}.100\% = 66,67\% \hfill \\ \% {V_{{C_4}{H_8}}} = 100\% - 66,67\% = 33,33\% \hfill \\ \end{gathered} \)
Một hỗn hợp gồm 1 ankan và 1 anken. Dẫn hỗn hợp đó qua 100 gam dung dịch brom 16% thấy brom mất màu và khối lượng bình tăng 2,8 gam, sau phản ứng thấy thoát ra 3,36 lít khí (đktc). Đốt cháy hoàn toàn hỗn hợp khí bay ra thu được 8,8 gam CO2 và 5,4 gam nước. Vậy công thức của anken và ankan lần lượt là
\(\begin{gathered}{n_{B{r_2}}} = \frac{{100.16\% }}{{160}} = 0,1mol \hfill \\{m_{binh \uparrow }} = {m_{anken(pu)}} = 2,8gam \hfill \\{n_{khi}} = 0,15mol;{n_{C{O_2}}} = 0,2mol;{n_{{H_2}O}} = 0,3mol \hfill \\ \end{gathered} \)
\(\begin{gathered}{n_{ankan}} = {n_{{H_2}O}} - {n_{C{O_2}}} = 0,1mol \hfill \\ = > {n_{anken}} = {n_{B{r_2}}} + (0,15 - 0,1) = 0,15mol \hfill \\ {M_{anken}} = \frac{{2,8}}{{0,1}} = 28 \hfill \\ \end{gathered} \)
=>Anken là C2H4
\({n_{C{O_2}(ankan)}} = 0,2 - 0,05.2 = 0,1mol\)
Số C trong ankan \( = \frac{{{n_{C{O_2}(ankan)}}}}{{{n_{ankan}}}} = 1\)
=> CTPT của ankan là CH4
Cho 2,24 lít hỗn hợp khí X (đktc) gồm 2 ankan là đồng đẳng kế tiếp nhau và propen sục qua nước brom dư thấy khối lượng bình đựng nước brom tăng 2,1 gam. Đốt cháy lượng khí còn lại thì thu được một lượng CO2 và 3,24 gam nước. Xác định công thức của hai ankan
Ta có khối lượng bình brom tăng lên 2,1 gam.
=> mpropen = 2,1 gam.
=> npropen =2,1/42=0,05 mol.
=> nankan = 0,05 mol.
Gọi CTPT chung của ankan là \({C_{\overline n }}{H_{2\overline n + 2}}\)
\(\begin{gathered}{C_{\overline n }}{H_{2\overline n + 2}} \to \overline n C{O_2} + (\overline n + 1){H_2}O \hfill \\\overline n + 1 = \frac{{{n_{{H_2}O}}}}{{{n_{ankan}}}} = 3,6 = > \overline n = 2,6 \hfill \\ \end{gathered} \)
Hai ankan là C2H6 và C3H8
Trộn 0,1 mol etilen với 0,1 mol H2 thu được hỗn hợp X. Cho hỗn hợp X qua Ni nung nóng thu được hỗn hợp Y. Tỷ khối của hỗn hợp X so với hỗn hợp Y là 0,6. Xác định hiệu suất của phản ứng hiđro hóa
Phản ứng:
C2H4 + H2\(\xrightarrow{{{t^o},Ni}}\) C2H6
Ban đầu (mol) 0,1 0,1
Sau phản ứng (mol) 0,1-x 0,1-x x
Tỷ khối X so với Y là 0,6
\(\begin{gathered}{M_X} = \frac{{0,1.28 + 0,1.2}}{{0,2}} = 15 \hfill \\{M_Y} = \frac{{(0,1 - x).28 + (0,1 - x).2 + 30x}}{{0,2 - x}} = \frac{3}{{0,2 - x}} \hfill \\{d_{X/Y}} = \frac{{15.(0,2 - x)}}{3} = 0,6 \hfill \\ \end{gathered} \)
=> x = 0,08
\(H = \frac{{0,08}}{{0,1}}.100\% = 80\% \)
Hỗn hợp khí X gồm H2 và C2H4 có tỉ khối so với He là 3,75. Dẫn X qua Ni nung nóng, thu được hỗn hợp khí Y có tỉ khối so với He là 5. Hiệu suất của phản ứng hiđro hoá là:
Đặt số mol ban đầu của X là 1 mol
\({d_{X/He}} = 3,75 = > {M_X} = 30\)
Số mol ban đầu của C2H4 là a mol
\(\frac{{28a + 2.(1 - a)}}{1} = 15 = > a = 0,5\)
C2H4 + H2\(\xrightarrow{{{t^o},Ni}}\) C2H6
Ban đầu (mol) 0,5 0,5
Sau phản ứng (mol) 0,5-x 0,5-x x
\(\begin{gathered}{d_{Y/He}} = 5 = > {M_Y} = 20 \hfill \\= > \frac{{28.(0,5 - x) + 2.(0,5 - x) + 30x}}{{1 - x}} = 20 \hfill \\= > x = 0,25 \hfill \\H = \frac{{0,25}}{{0,5}}.100\% = 50\% \hfill \\ \end{gathered} \)
Hấp thụ hoàn toàn một lượng anken X vào bình đựng nước brom thì thấy khối lượng bình tăng 5,6 gam và có 16 gam brom phản ứng. Số đồng phân cấu tạo của X là
Anken X có công thức phân tử là CnH2n ( n ≥2)
Ta có CnH2n + Br2 → CnH2nBr2
0,1 ← 0,1
→ Manken = 5,6 :0,1 =56 → 14n = 56 → n = 4
→ anken là C4H8
Các đồng phân cấu tạo là
CH2 = CH – CH2 – CH3
CH3 – CH = CH – CH3
CH3 – C(CH3) = CH2
Một hỗn hợp X gồm 0,1 mol C2H4; 0,15 mol C3H6 và 0,25 mol H2. Dẫn hỗn hợp X qua Ni nung nóng thu được hỗn hợp Y. Dẫn hỗn hợp Y qua dung dịch Br2 dư thấy khối lượng bình tăng 1,82 gam và có 8 gam brom đã tham gia phản ứng. Nếu gọi h1 và h2 là hiệu suất phản ứng hiđro hóa của etilen và propen. Hãy cho biết giá trị của h1 và h2
Vì \({n_{{C_2}{H_4}}} + {n_{{C_3}{H_6}}} = {n_{{H_2}}}\)
do đó hiệu suất có thể tính theo C2H4 và C3H6
C2H4 + H2 → C2H6
Phản ứng (mol) a a a
C3H6 + H2 → C3H8
Phản ứng (mol) b b b
Hỗn hợp Y gồm:
C2H4 : 0,1-a (mol); C3H6: 0,15-b (mol); H2: 0,25-a-b (mol); C2H6: a (mol); C3H8: b (mol)
Ta có
\(\begin{gathered}{m_{B{r_2}( \uparrow )}} = {m_{{C_2}{H_4}(du)}} + {m_{{C_3}{H_6}(du)}} = 1,82(gam) \hfill \\{n_{B{r_2}(pu)}} = {n_{{C_2}{H_4}(du)}} + {n_{{C_3}{H_6}(du)}} = 0,05(mol) \hfill \\ \to \left\{ \begin{gathered}28.(0,1 - a) + 42.(0,15 - b) = 1.82 \hfill \\ 0,1 - a + 0,15 - b = 0,05 \hfill \\ \end{gathered} \right. \hfill \\\to \left\{ \begin{gathered} a = 0,08(mol) \hfill \\b = 0,12(mol) \hfill \\ \end{gathered} \right. \hfill \\{h_1} = \frac{{0,08}}{{0,1}}.100\% = 80\% \hfill \\{h_2} = \frac{{0,12}}{{0,15}}.100\% = 80\% \hfill \\ \end{gathered} \)

