Cách nào sau đây dùng để điều chế etyl axetat ?
Cách dùng để điều chế etyl axetat là đun hồi lưu hỗn hợp etanol, axit axetic và axit sunfuric đặc. Không dùng giấm và rượu trắng vì độ tinh khiết không cao => hiệu suất thấp
Este phenyl axetat CH3COOC6H5 được điều chế bằng phản ứng nào ?
Các este chứa gốc phenyl không điều chế được bằng phản ứng của axit cacboxylic với phenol mà phải dùng anhiđrit axit hoặc clorua axit tác dụng với phenol.
(CH3CO)2O + C6H5OH → CH3COOC6H5 + CH3COOH
Cho phản ứng este hóa : RCOOH + R’OH $\overset{{}}{\leftrightarrows}$ R-COO-R’ + H2O
Để phản ứng chuyển dịch ưu tiên theo chiều thuận người ta thường :
Để tăng hiệu suất phản ứng thuận:
+ Tăng nồng độ chất tham gia.
+ Giảm nồng độ sản phẩm bằng cách: đun nóng để este bay hơi hoặc dùng H2SO4 đặc để hút nước. H2SO4 đặc vừa là xúc tác, vừa làm tăng hiệu suất phản ứng.
Dầu chuối là este có tên isoamyl axetat, được điều chế từ
Dầu chuối có CTCT: CH3COOCH2-CH2-CH(CH3)2
=> được điều chế từ CH3COOH và (CH3)2CH-CH2-CH2OH.
Đun nóng 24 gam axit axetic với lượng dư ancol etylic (xúc tác H2SO4 đặc), thu được 26,4 gam este. Hiệu suất của phản ứng este hóa là
CH3COOH + C2H5OH $\overset{{{H}_{2}}S{{O}_{4}}\,,{{t}^{o}}}{\leftrightarrows}$ CH3COOC2H5 + H2O
nCH3COOC2H5 theo pt = nCH3COOH = 0,4 mol
Mà nCH3COOC2H5 thực tế thu được = 0,3 mol
=> H = nCH3COOC2H5 thực tế thu được / nCH3COOC2H5 theo pt = 0,3 / 0,4 = 75%
Đun 12 gam axit CH3COOH với 13,8 gam C2H5OH (có xúc tác H2SO4 đặc) đến khi phản ứng đạt trạng thái cân bằng thu được 11 gam este. Hiệu suất của phản ứng este hoá là
Vì số mol ancol lớn hơn số mol axit nên ancol dư.
Số mol ancol pư = số mol axit = 0,2 mol
Áp dụng định luật bảo toàn khối lượng : mancol + maxit = meste + mnước
=> 0,2.46 + 12 = meste + 0,2.18 => meste = 17,6 gam
Nên H = $\frac{{11.100}}{{17,6}}$= 62,5%
Hỗn hợp X gồm axit HCOOH và axit CH3COOH (tỉ lệ mol 1:1). Lấy 5,3 gam hỗn hợp X tác dụng với 5,75 gam C2H5OH (có xúc tác H2SO4 đặc) thu được m gam hỗn hợp este (hiệu suất của các phản ứng este hoá đều bằng 80%). Giá trị của m là
Vì số mol ancol lớn hơn số mol 2 axit nên ancol dư.
Số mol ancol pư = số mol 2 axit = 0,1 mol. áp dụng định luật bảo toàn khối lượng có
mancol + maxit = meste + mnước => 0,1.46 + 5,3 = meste + 0,1.18 => meste = 8,10 gam
H = 80% nên meste thu được = $\frac{{8,10.80}}{{100}}$= 6,48 gam.
Cho 24,0 gam axit axetic tác dụng với 18,4 gam glyxerin (H2SO4 đặc và đun nóng) thu được 21,8 gam glixerin triaxetat. Hiệu suất của phản ứng là
3CH3COOH + C3H5(OH)3 $\overset{{}}{\leftrightarrows}$ (CH3COO)3C3H5 + 3H2O
0,4 mol 0,2 mol
Vì \(\frac{{0,4}}{3} < \frac{{0,2}}{1}\) => C3H5(OH)3 dư, hiệu suất tính theo CH3COOH
=> neste theo pt = 0,4 / 3 => meste theo pt = 218.0,4 / 3 = 436 / 15 gam
=> H = meste thực tế / meste theo pt$ = \frac{{21,8}}{{\frac{{436{\rm{ }}}}{{15}}}}.100\% = 75\% $
Cho 0,1 mol glixerol phản ứng với 0,15 mol axit axetic có H2SO4 đặc (H = 60%) thu được m gam este B. Giá trị m là
xCH3COOH + C3H5(OH)3 $\overset{{}}{\leftrightarrows}$ (CH3COO)xC3H5(OH)3-x + xH2O
0,15 0,1
Xét x = 1 => CH3COOH dư, C3H5(OH)3 hết
=> neste theo pt = nC3H5(OH)3 = 0,1 mol
=> neste thực tế = 0,1.0,6 = 0,06 mol => m = 0,06.134 = 8,04 gam
Xét x = 2 => CH3COOH hết, C3H5(OH)3 dư
=> neste theo pt = nCH3COOH / 2 = 0,075 mol
=> neste thực tế = 0,075.0,6 = 0,045 mol => m = 0,045.176 = 7,92 gam (đáp án D)
Xét x = 3 => CH3COOH hết, C3H5(OH)3 dư
=> neste theo pt = nCH3COOH / 3 = 0,05 mol
=> neste thực tế = 0,05.0,6 = 0,03 mol => m = 0,03.218 = 6,54 gam
Hỗn hợp A gồm axit axetic và etanol. Chia A thành ba phần bằng nhau.
+ Phần 1 tác dụng với Kali dư thấy có 3,36 lít khí thoát ra.
+ Phần 2 tác dụng với Na2CO3 dư thấy có 1,12 lít khí CO2 thoát ra. Các thể tích khí đo ở đktc.
+ Phần 3 được thêm vào vài giọt dung dịch H2SO4, sau đó đun sôi hỗn hợp một thời gian. Biết hiệu suất của phản ứng este hoá bằng 60%. Khối lượng este tạo thành là bao nhiêu?
Hỗn hợp A$\left\{ \begin{array}{l}C{H_3}COOH:a\,\,mol\\{C_2}{H_5}OH:b\,\,mol\end{array} \right.\,\, = > \,\,\left\{ \begin{array}{l}{n_A} = a + b = 2{n_{{H_2}}} = 0,3\,\,mol\\a = 2{n_{C{O_2}}} = 0,1\,\,mol\end{array} \right. = > \,\left\{ \begin{array}{l}a = 0,1\,\,mol\\b = 0,2\,\,mol\end{array} \right.$
Vì a < b => hiệu suất tính theo axit => số mol este thực tế thu được: n = 0,1.60% = 0,06 mol
Þ Khối lượng este thực tế thu được: m = 0,06.88 = 5,28 gam
Cho 0,3 mol axit X đơn chức trộn với 0,25 mol ancol etylic đem thực hiện phản ứng este hóa thu được thu được 18 gam este. Tách lấy lượng ancol và axit dư cho tác dụng với Na thấy thoát ra 2,128 lít H2 (đktc). Vậy công thức của axit và hiệu suất phản ứng este hóa là
nH2 = 0,095 mol => naxit và ancol dư = 0,19 mol
Gọi x là hiệu suất phản ứng
Do số mol ancol < số mol axit nên hiệu suất tính theo ancol
=> n axit và ancol dư = 0,3 – 0,25x + 0,25 – 0,25x = 0,19 => x = 0,72
=> neste = 0,25.0,72 = 0,18 mol => M = 100 => este là CH2=CH–COOC2H5
Chia 26,96 gam hỗn hợp X gồm 3 axit đơn chức thành 2 phần bằng nhau. Phần 1 cho tác dụng với NaHCO3 dư thu được 4,48 lít khí CO2 (đktc). Phần 2 cho tác dụng hết với etylen glicol chỉ thu được nước và m gam 3 este tạp chức. Giá trị của m là
m1 phần = 13,48 gam; nCO2 = 0,2 mol => naxit = nCO2 = 0,2 mol
Do tạo thành este tạp chức => axit phản ứng với C2H4(OH)2 theo tỉ lệ 1 : 1
=> nH2O = nC2H4(OH)2 = naxit = 0,2 mol
Bảo toàn khối lượng : maxit + mancol = meste + mH2O
=> meste = 13,48 + 0,2.62 – 0,2.18 = 22,28 gam
Oxi hoá anđehit OHCCH2CH2CHO trong điều kiện thích hợp thu được hợp chất hữu cơ X. Đun nóng hỗn hợp gồm 1 mol X và 1 mol ancol metylic với xúc tác H2SO4 đặc thu được 2 este Z và Q (MZ < MQ) với tỷ lệ khối lượng mZ : mQ = 1,81. Biết chỉ có 72% ancol chuyển thành este. Số mol Z và Q lần lượt là
n CH3OH pư = 0,72 mol
OHCCH2CH2CHO + O2 → HOOCCH2CH2COOH
HOOC-CH2CH2-COOH + CH3OH → HOOC-CH2CH2-COOCH3
x x x
HOOC-CH2CH2-COOH + 2CH3OH → CH3OOC-CH2CH2-COOCH3
y 2y y
72% ancol chuyển thành este => nancol phản ứng = x + 2y = 0,72 (1)
Mà theo đề MZ < MQ nên Z là este ở pt1 và Q là este ở pt2
$ = > {\rm{ }}\frac{{x.132}}{{y.146}} = 1,81{\rm{ }}\left( 2 \right)$
Từ (1) và (2) => x = 0,36; y = 0,18
Cho biết hằng số cân bằng của phản ứng este hoá:
CH3COOH + C2H5OH $\overset{{}}{\leftrightarrows}$ CH3COOC2H5 + H2O (KC = 4)
Nếu cho hỗn hợp cùng số mol axit và ancol tác dụng với nhau thì khi phản ứng đạt đến trạng thái cân bằng thì phần trăm ancol và axit đã bị este hoá là
CH3COOH + C2H5OH $\overset{{}}{\leftrightarrows}$ CH3COOC2H5 + H2O (KC = 4)
BĐ: 1 mol 1 mol
P/ứ: x → x → x → x
CB: 1 – x 1 – x x x
$ = > {\rm{ }}{K_C} = \frac{{{x^2}}}{{{{(1 - x)}^2}}} = 4\,\, = > \,\,x = 0,6667$
=> H = 0,6667 / 1 . 100% = 66,67%
CH3COOH + C2H5OH $\overset{{}}{\leftrightarrows}$ CH3COOC2H5 + H2O (KC = 4)
Khi cho 1 mol axit tác dụng với 1,6 mol ancol, khi hệ đạt đến trạng thái cân bằng thì hiệu suất của phản ứng là
CH3COOH + C2H5OH $\overset{{}}{\leftrightarrows}$ CH3COOC2H5 + H2O (KC = 4)
BĐ: 1 mol 1,6 mol
P/ứ: x → x → x → x
CB: 1 – x 1,6 – x x x
$ = > {\rm{ }}{K_C} = \frac{{{x^2}}}{{(1 - x).(1,6 - x)}} = 4\,\, = > \,\,x = 0,8$
Vì naxit < nancol => hiệu suất phản ứng tính theo axit
=> H = 0,8 / 1 . 100% = 80%
Khi thực hiện phản ứng este hoá 1 mol CH3COOH và 1 mol C2H5OH, lượng este lớn nhất thu được là 2/3 mol. Để đạt hiệu suất cực đại là 90% (tính theo axit) khi tiến hành este hoá 1 mol CH3COOH cần số mol C2H5OH là (biết các phản ứng este hoá thực hiện ở cùng nhiệt độ)
CH3COOH + C2H5OH $\overset{{}}{\leftrightarrows}$ CH3COOC2H5 + H2O
BĐ: 1 mol 1 mol
P/ứ: 2/3 2/3 2/3 2/3
CB: 1/3 1/3 2/3 2/3
$ = > {\rm{ }}{K_C} = \frac{{2/3.2/3}}{{1/3.1/3}} = 4$
Hiệu suất đạt cực đại H = 90% => nCH3COOH phản ứng = 1.90% = 0,9 mol
Gọi số mol C2H5OH cần dùng = x mol
CH3COOH + C2H5OH $\overset{{}}{\leftrightarrows}$ CH3COOC2H5 + H2O
BĐ: 1 mol x mol
P/ứ: 0,9 → 0,9 → 0,9 → 0,9
CB: 0,1 x – 0,9 0,9 0,9
Vì 2 phản ứng thực hiện ở cùng nhiệt độ => KC không đổi
$ = > {\rm{ }}{K_C} = \frac{{0,9.0,9}}{{0,1.(x-0,9)}} = 4\,\, = > \,\,x = 2,925$
X là axit đơn chức, mạch hở; Y là ancol đơn chức, mạch hở. Đung hỗn hợp X, Y với H2SO4 đặc thu được este Z. Biết trong Z có chứa 54,54% khối lượng cacbon. Số cặp chất phù hợp với X, Y là
Gọi công thức của este Z là: CxHyO2 (đk: y ≤ 2x +2; x ≥ 2 )
Ta có:
\(\begin{gathered}\% C = \frac{{12x}}{{12x + y + 32}}.100\% = 54,54\% \hfill \\\Rightarrow 10x = y + 32 \hfill \\ \end{gathered} \)
Chạy thấy giá trị x = 4 và y = 8 thỏa mãn
Vậy công thức của Z: C4H8O2
Các CTCT thỏa mãn là:
HCOOCH2CH2CH3
HCOOCH(CH3)CH3
CH3COOC2H5
C2H5COOCH3
=> Có 4 CTCT thỏa mãn
Tổng hợp 120 kg polimetylmetacrylat từ axit và ancol thích hợp, hiệu suất của phản ứng este hóa là 30% và phản ứng trùng hợp là 80%. Khối lượng của axit cần dùng là
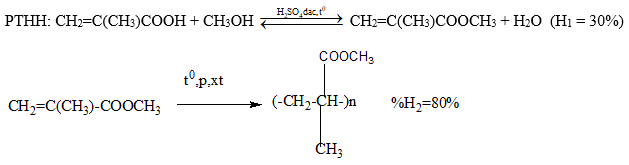
npolimetaacylat = 12:100 = 1,2 (mol)
=> nCH2=C(CH3)COOH lí thuyết = npolimetaacylat = 1,2 (mol)
=> nCH2=C(CH3)COOH thực tế = nCH2=C(CH3)COOH lí thuyết :%H2 : %H1 = 1,2 : 0,8 : 0,3 = 5 (mol)
=> mCH2=C(CH3)COOH thực tế = 5. 86 = 430 (kg)

