Đốt cháy hoàn toàn 6,72 lít (đktc) hỗn hợp gồm hai hiđrocacbon X và Y (MY > MX), thu được 11,2 lít khí CO2 (đktc) và 10,8 gam H2O. Công thức của X là:
${n_{hh}} = \dfrac{{6,72}}{{22,4}} = 0,3\,mol;\,\,\,{n_{C{O_2}}} = \dfrac{{11,2}}{{22,4}} = 0,5\,mol;\,\,\,{n_{{H_2}O}} = \dfrac{{10,8}}{{18}} = 0,6\,mol$
→$\overline C = \dfrac{{0,5}}{{0,3}} \approx 1,66$→ hỗn hợp có CH4. Mặt khác MY > MX → X là CH4
Đốt cháy hoàn toàn hỗn hợp M gồm một ankan X và một ankin Y, thu được số mol CO2 bằng số mol H2O. Thành phần phần trăm về số mol của X và Y trong hỗn hợp M lần lượt là:
Đốt cháy ankan: nankan = nH2O – nCO2
Đốt cháy ankin: nankin = nCO2 – nH2O
Trừ 2 phương trình ta có nankan - nankin = nH2O – nCO2 Mà nH2O = nCO2
=> nankan = nankin = 50%
Đốt cháy hoàn toàn 0,2 mol hỗn hợp X gồm một ankan và một anken, thu được 0,35 mol CO2 và 0,4 mol H2O. Phần trăm số mol của anken trong X là:
Đốt cháy ankan => ${n_{Ankan}} = {n_{{H_2}O}} - {n_{C{O_2}}}$
Đốt cháy anken => ${n_{{H_2}O}} = {n_{C{O_2}}}$
=> đốt cháy hỗn hợp ankan và anken thì: nankan = nH2O – nCO2 = 0,4 – 0,35 = 0,05 mol
=> nanken = nhh – nankan = 0,2 – 0,05 = 0,15 mol
→ % nanken $ = \dfrac{{0,15}}{{0,2}}.100\% = 75\% $
Đốt cháy hoàn toàn 1 lít hỗn hợp khí gồm C2H2 và hiđrocacbon X sinh ra 2 lít khí CO2 và 2 lít hơi H2O (các thể tích khí và hơi đo ở cùng điều kiện nhiệt độ, áp suất). Công thức phân tử của X là:
$\overline C = \dfrac{{{n_{C{O_2}}}}}{{{n_{hh}}}} = \dfrac{{{V_{C{O_2}}}}}{{{V_{hh}}}} = \dfrac{2}{1} = 2$ Mà C2H2 có 2 nguyên tử C nên X cũng có 2 nguyên tử C
Ta có: $\overline H = \dfrac{{2{n_{{H_2}O}}}}{{{n_{hh}}}} = \dfrac{{2{V_{{H_2}O}}}}{{{V_{hh}}}} = \dfrac{{2.2}}{1} = 4$ Mà C2H2 có 2 nguyên tử H nên X có 6 nguyên tử H
Vậy X là C2H6
Dẫn 1,68 lít hỗn hợp khí X gồm hai hiđrocacbon vào bình đựng dung dịch brom (dư). Sau khi phản ứng xảy ra hoàn toàn, có 4 gam brom đã phản ứng và còn lại 1,12 lít khí. Nếu đốt cháy hoàn toàn 1,68 lít X thì sinh ra 2,8 lít khí CO2. Biết các thể tích khí đều đo ở đktc. Công thức phân tử của hai hiđrocacbon là:
Ta có nX = 0,075 mol
Cho X qua brom khí không bị hấp thụ là ankan => nankan = 0,05 mol
=> nhiđrocacbon còn lại = 0,075 - 0,025 = 0,025 mol
Mà ${n_{B{r_2}}} = \dfrac{4}{{160}} = 0,025\,mol$
=> số pi trong hiđrocacbon là 1
=> Công thức là CnH2n
Sau khi phản ứng với Br2, khí thoát ra là ankan
$\overline C = \dfrac{{{V_{C{O_2}}}}}{{{V_X}}} = \dfrac{{2,8}}{{1,68}} \approx 1,67$ => Ankan là CH4
Tỉ lệ thể tích bằng tỉ lệ số mol
0,05 → 0,05
0,025 → 0,075
=> n =3
=> Công thức là C3H6
Hỗn hợp X có tỉ khối so với H2 là 21,2 gồm propan, propen và propin. Khi đốt cháy hoàn toàn 0,1 mol X, tổng khối lượng của CO2 và H2O thu được là:
X gồm C3H8, C3H6, C3H4
=> Gọi chung công thức X là C3Hx
\({d_{X/{H_2}}} = 21,2 \to {\bar M_X} = 21,2*2 = 42,4 = 12*3 + x\)
=> x = 6,4
=> Công thức X là C3H6,4
PTHH: C3H6,4 + 4,6 O2 $\xrightarrow{t_{{}}^{0}}$ 3CO2 + 3,2H2O
0,1 → 0,3 →0,32
$\to {m_{C{O_2}}} + {m_{{H_2}O}} = 0,3.44 + \dfrac{{0,64}}{2}.18 = 18,96\,g $
Cho hỗn hợp X gồm CH4, C2H4 và C2H2. Lấy 8,6 gam X tác dụng hết với dung dịch brom (dư) thì khối lượng brom phản ứng là 48 gam. Mặt khác, nếu cho 13,44 lít (ở đktc) hỗn hợp khí X tác dụng với lượng dư dung dịch AgNO3 trong NH3, thu được 36 gam kết tủa. Phần trăm thể tích của CH4 có trong X là:
Gọi số mol của CH4 và C2H4 lần lượt là a, là b (trong 8,6 gam X)
Xét 13,44 lít hỗn hợp khí X
${n_X} = 0,6\,mol$
\(\begin{array}{l}{n_ \downarrow } = {n_{{C_2}{H_2}}} = 0,15{\mkern 1mu} mol = \frac{1}{4}{n_X}{\mkern 1mu} \\ = > {n_{{C_2}{H_4}}} + {n_{C{H_4}}} = \frac{3}{4}{n_X}\\ = > \frac{{{n_{{C_2}{H_2}}}}}{{{n_{{C_2}{H_4}}} + {n_{C{H_4}}}}} = \frac{1}{3}\\ \Rightarrow {n_{{C_2}{H_2}(trong{\kern 1pt} 8,6{\kern 1pt} gam{\kern 1pt} X)}} = \frac{{a + b}}{3}{\mkern 1mu} mol\end{array}\)
Xét 8,6 gam hỗn hợp khí X => $16a + 28b + 26.\dfrac{{a + b}}{3} = 8,6$(1)
BT sô liên kết pi: \({n_{B{r_2} phản ứng}} = {n_{{C_2}{H_4}}} + {n_{{C_2}{H_2}}}*2 = b + \frac{{2(a + b)}}{3} = 0,3(2)\)
Từ (1) và (2) => a = 0,2 ; b = 0,1
$\% {V_{C{H_4}}} = \dfrac{{0,2}}{{0,2 + 0,1 + \dfrac{{0,2 + 0,1}}{3}}}.100\% = 50\% $
Hỗn hợp khí X gồm 0,3 mol H2 và 0,1 mol vinylaxetilen. Nung X một thời gian với xúc tác Ni thu được hỗn hợp khí Y có tỉ khối so với không khí là 1. Nếu cho toàn bộ Y sục từ từ vào dung dịch brom (dư) thì có m gam brom tham gia phản ứng. Giá trị của m là:
BT khối lượng: \({m_X} = {m_Y} = 0,3.2 + 0,1.52 = 5,8{\mkern 1mu} gam\)
=> \( {n_Y} = \frac{{5,8}}{{29}} = 0,2{\mkern 1mu} mol\)
PTHH: C4H4 +H2 → C4H6
C4H4 +H2 → C4H6
Ta thấy chênh lệch giữa 2 mol là số mol H2 phản ứng
${n_{{H_2}}}$phản ứng $ = {n_X} - {n_Y} = 0,1 + 0,3 - 0,2 = 0,2\,mol$
Bảo toàn liên kết π: Do H2 và Br2 đều phản ứng vào liên kết π nên => ${n_{B{r_2}}} = 3.{n_{{C_4}{H_4}}} - {n_{{H_2}}} = 0,1.3 - 0,2 = 0,1\,mol \to {m_{B{r_2}}} = 0,1.160 = 16\,gam$
Dẫn V lít (ở đktc) hỗn hợp X gồm axetilen và hiđro đi qua ống sứ nung nóng, thu được khí Y. Dẫn Y vào lượng dư AgNO3 (hoặc Ag2O) trong dung dịch NH3 thu được 12 gam kết tủa. Khí đi ra khỏi dung dịch phản ứng vừa đủ với 16 gam brom và còn lại khí Z. Đốt cháy hoàn toàn khí Z thu được 2,24 lít khí CO2 (ở đktc) và 4,5 gam nước. Giá trị của V bằng:
C2H2 + H2 thu được Y => Y gồm C2H2, C2H4, C2H6 và H2 dư.
Y tác dụng với AgNO3/NH3:
\({\rm{\;}}HC \equiv CH{\mkern 1mu} + {\mkern 1mu} 2AgN{O_3} + N{H_3} \to AgC \equiv CAg \downarrow {\rm{\;}} + N{H_4}N{O_3} + {H_2}O\)
\({n_{{C_2}{H_2}}} = {n_ \downarrow } = 0,05{\mkern 1mu} mol \Rightarrow {m_{{C_2}{H_2}}} = 1,3{\mkern 1mu} gam\)
=> Khí bay ra khỏi bình AgNO3/NH3 là C2H4, C2H6 và H2 dư
Cho qua bình đựng nước brom thì chỉ có C2H4 phản ứng được với brom
${n_{{C_2}{H_4}}} = {n_{B{r_2}}} = 0,1\,mol \Rightarrow {m_{{C_2}{H_4}}} = 0,1.28 = 2,8\,gam$
Sau cho bình brom còn lại Z gồm C2H6 và H2 dư
Trong Z có: \(\left\{ \begin{array}{l}{n_{C{O_2}}} = 0,1{\mkern 1mu} mol\\{n_{{H_2}O}} = 0,25{\mkern 1mu} mol\end{array} \right.\)
Bảo toàn nguyên tố C: \( \to {m_Z} = {m_C} + {m_H} = 0,1.12 + 0,25.2 = 1,7{\mkern 1mu} gam\)
${n_{{C_2}{H_2}}} = 0,05 + 0,1 + \dfrac{{0,1}}{2} = 0,2mol \to {m_C}_{_2{H_2}} = 0,2.26 = 5,2\,gam$
Bảo toàn khối lượng ban đầu:
${m_X} = 2,8 + 1,7 + 1,3 = 5,8\,gam \to {m_{{H_2}}} = 5,8 - 5,2 = 0,6\,gam \to {n_{{H_2}}} = \dfrac{{0,6}}{2} = 0,3\,mol$
Tổng thể tích khí: ${V_X} = 22,4.(0,2 + 0,3) = 11,2$ lít
Đun nóng hỗn hợp X gồm 0,06 mol C2H2 và 0,04 mol H2 với xúc tác Ni, sau một thời gian thu được hỗn hợp khí Y. Dẫn toàn bộ hỗn hợp Y lội từ từ qua bình đựng dung dịch brom (dư) thì còn lại 0,448 lít hỗn hợp khí Z (ở đktc) có tỉ khối so với O2 là 0,5. Khối lượng bình dung dịch brom tăng là:
Áp dụng bảo toàn khối lượng: mC2H2 +mH2 = 0,06*26 + 0,04*2 = 1,64 gam
Tỉ khối của Z so với O2 bằng 0,5
=> \({M_Z} = 0,5*32 = 16\) gam
=> mZ =n*M=\(\frac{{0,448}}{{22,4}}*16 = \) 0,32 gam
BT khối lượng => Khối lượng bình đựng brom tăng (m↑):
${m_ \uparrow } = {m_Y} - {m_Z} = 1,64 - 0,32 = 1,32\,gam$
Đốt cháy hoàn toàn 0,16 mol hỗn hợp X gồm CH4, C2H2, C2H4 và C3H6, thu được 6,272 lít CO2(đktc) và 6,12 gam H2O. Mặt khác 10,1 gam X phản ứng tối đa với a mol Br2 trong dung dịch. Giá trị của a là
nCO2 = 6,272 :22,4 = 0,28 (mol)
nH2O = 6,12 :18 = 0,34 (mol)
áp dụng công thức khi đốt cháy một hợp chất hữu cơ X có độ bất bão hòa k có:
\({n_X} = {{{n_{C{O_2}}} - {n_{{H_2}O}}} \over {k - 1}} \Rightarrow 0,16 = {{0,28 - 0,34} \over {k - 1}} \Rightarrow k = 0,625\)
Đặt công thức chung của X là: CxHy
\( \Rightarrow \left\{ \matrix{
x = {{{n_{C{O_2}}}} \over {{n_X}}} = {{0,28} \over {0,16}} = 1,75 \hfill \cr
y = {{2{n_{{H_2}O}}} \over {{n_X}}} = {{2.0,34} \over {0,16}} = 4,25 \hfill \cr} \right.\)
CTPT chung của X là: C1,75H4,25
Xét 10,1 g X hay 0,4 mol X phản ứng với a mol dd Br2
=> nBr2 = nliên kết pi bị phá vỡ = k.nX = 0,625.0,4 = 0,25 (mol)
Cho dãy các chất: CH4, C2H2, C2H4, C2H5OH, CH2=CH–COOH, C6H5NH2 (anilin), C6H5OH (phenol), C6H6 (benzen). Số chất trong dãy phản ứng được với nước brom là:
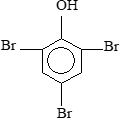
Các chất trong dãy phản ứng được với nước brom là: C2H2, C2H4, CH2=CH–COOH, C6H5NH2 (anilin), C6H5OH (phenol).
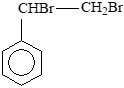
CH≡CH + 2Br2 → CHBr2−CHBr2
CH2=CH2 + Br2 → CH2Br−CH2Br
CH2=CH−COOH + Br2 → CH2Br−CHBr−COOH